Características moleculares y susceptibilidad a antibióticos de cepas de Staphylococcus aureus colonizantes de pacientes con patologías nasales procedentes de Cartagena (Colombia), 2015: estudio observacional
Oscar Montes, MS1*, Rosa Milanés, MD2*, Álvaro Alvarez, MS3*, Sandra Coronado, MS4*, Niradiz Reyes, PhD5*
1* Grupo Genética y Biología Molecular. Facultad de Medicina, Universidad de Cartagena, Cartagena, Colombia. Email: oscarbio2009@hotmail.com
2* Grupo Microbiología clínica y ambiental. Universidad de Cartagena, Cartagena, Colombia. Email: rosamilanesp@hotmail.com
3* Grupo Microbiología clínica y ambiental. Universidad de Cartagena, Cartagena, Colombia. Email: alalvcon@unicartagena.edu.co
4* Ciencias Básicas. Facultad de Medicina. Universidad de Cartagena, Cartagena, Colombia. Email: sandracoronado360@yahoo.com
5* PhD. Grupo Genética y Biología Molecular. Departamento de Ciencias Básicas, Facultad de Medicina, Universidad de Cartagena, Cartagena, Colombia. Corresponding author. Email: nreyesr@unicartagena.edu.co
1Archivos de Medicina (Manizales), Volumen 15 N° 2, Julio-Diciembre 2015, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Motes O.; Milanés R.; Ávarez A.; Coronado S.; Reyes N.
Recibido para publicación: 30-04-2015 - Versión corregida: 30-09-2015 - Aprobado para publicación: 10-11-2015
Resumen
Objetivo: staphylococcus aureus es uno de los principales patógenos causantes de infecciones tanto a nivel hospitalario como comunitario. El objetivo de este estudio fue determinar características moleculares y los perfiles de resistencia a antibióticos de aislamientos de Staphylococcus aureus colonizantes de pacientes con patología nasal atendidos en el servicio de Otorrinolaringología del Hospital Universitario del Caribe de la ciudad de Cartagena, Colombia. Métodos: los aislamientos de Staphylococcus aureus obtenidos de pacientes colonizados fueron sometidos a extracción de ADN y ensayos de PCR para determinar la presencia de los genes mecA y lukS/F-PV. Se determinó la pertenencia de las cepas a los complejos clonales CC5 y CC8, y se determinaron las relaciones clonales de los aislamientos mediante análisis de PFGE. A las cepas SARM se les tipificó y sub-tipificó el casete cromosomal estafilocócico SCCmec mediante PCR múltiple. Resultados: la prevalencia de colonización encontrada para Staphylococcus aureus fue 22.8% y 5.26% para SARM. Del total de aislamientos SARM, 33.3% estuvieron relacionados con el clon CC8-SARM-IVc y 22.28% con CC8-SARM-IVa. Los genes para la leucocidina PVL se identificaron en 66.7% de aislamientos SARM y 40% de aislamientos sensibles a meticilina (SASM). En cuanto a la distribución de los aislamientos SARM en complejos clonales, 41% pertenecieron al CC8 y 18% al CC5. Conclusiones: los clones CC8-SARM-IVc y CC8-SARM-IVa, ambos relacionados con el clon USA300, circulan en población con patología nasal de la ciudad de Cartagena de Indias.
Palabras clave: staphylococcus aureus resistente a meticilina, resistencia a la meticilina, infección hospitalaria, infecciones comunitarias adquiridas, factores de virulencia.
Montes O, Milanés R, Álvarez A, Cloronado S, Reyes N. Características moleculares y susceptibilidad a antibióticos de cepas de staphylococcus aureus colonizantes de pacientes con patologías nasales procedentes de Cartagena (Colombia), 2015: estudio observacional. Arch Med (Manizales) 2015; 15(2):226-40.
Molecular characterization and antibiotic susceptibility of Staphylococcus aureus strains colonizing patients with nasal pathology from Cartagena (Colombia), 2015: observational study
Summary
Objective: staphylococcus aureus is a major pathogen causing infections both at the hospital and community level. The objective of this study was to determine molecular features and the antibiotic resistance profiles of Staphylococcus aureus colonizing patients attending the Otolaryngology practice of the Hospital Universitario del Caribe in the city of Cartagena, Colombia. Methods: staphylococcus aureus isolates from carriers were subjected to DNA extraction and PCR assays to determine the presence of mecA and lukS/F-PV genes. Isolates were assigned to clonal complexes 5 (CC5) or 8 (CC8) and PFGE analysis was performed to determine the clonal relatedness of isolates. Typing and subtyping of the staphylococcal chromosomal cassette was performed for MRSA isolates using multiplex PCR. Results: overall prevalence for Staphylococcus aureus carriage in the study group was 22.8% and 5.26% for MRSA carriage. Among MRSA isolates, 33.3% belonged to clone CC8-MRSA-IVc and 22.2% to CC8-MRSA-IVa. The genes for PVL leukocidin were identified in 66.7% of MRSA isolates and 40% of MSSA (methicillin sensitive). 41% of isolates belonged to clonal complex 8 (CC8) and 18% to clonal complex 5 (CC5). Conclusions: CC8-MRSA-IVc and CC8-MRSA-IVa clones are related to USA300 clone, and they are currently colonizing patients with nasal pathology in the city of Cartagena, Colombia.
Keywords: methicillin-resistant staphylococcus aureus, methicillin resistance, cross infection, community-acquired infections, virulence factors.
Introducción
El Staphylococcus aureus meticilino resistente, tanto asociado a la comunidad (AC-SARM) como hospitales (AH-SARM), se ha convertido en un problema de salud pública a nivel mundial1. Las infecciones causadas por cepas AH-SARM, generalmente ocurren en personas con factores de riesgo como las cirugías o la presencia de dispositivos médicos, mientras que las infecciones por AC-SARM ocurren típicamente en individuos aparentemente sanos que no presentan factores de riesgo2. Aunque los registros de vigilancia de los clones SARM específicos de algunos países de América Latina son limitados, se ha establecido que en este continente los clones que causan infecciones pandémicas son habituales en los hospitales, mientras que en la comunidad su diseminación ha aumentado considerablemente3. En Colombia, se ha reportado el cambio en la distribución clonal de SARM. Durante la década de los noventa prevaleció el llamado clon Pediátrico4, el cual fue desplazado a finales de siglo por el clon chileno5, y a mediados de esta década inició el cambio por un clon relacionado con los clones USA300 circulantes en los Estados Unidos6.
En los últimos años se han observado cambios a nivel molecular en los aislamientos de S. aureus, tales como la adquisición de genes de virulencia y de resistencia a antibióticos, los cuales se ven reflejados en sus características epidemiológicas, al tiempo que cada vez se observan más infecciones en personas sanas y sin elementos de riesgo convencionales para su adquisición7. También se ha reportado que existen diferencias en la susceptibilidad antibiótica de las cepas de esta bacteria y que los cambios en los perfiles de resistencia se pueden producir progresivamente8. Diversos estudios han evaluado la epidemiología molecular de los clones SARM en América Latina, aunque se conoce que varios clones circulan en esta región, los cuales difieren en virulencia, perfil de resistencia y distribución geográfica9,10,11. Este estudio estuvo dirigido a determinar las características microbiológicas, moleculares, y el perfil de susceptibilidad a antibióticos de las cepas de S. aureus que colonizan pacientes con patologías nasales en un centro asistencial de Cartagena de Indias (Colombia).
Materiales y métodos
Diseño, Población de estudio, y criterios de inclusión
El presente fue un estudio observacional en el que se evalúan las características moleculares y perfiles de susceptibilidad a antibióticos de los aislamientos de S. aureus obtenidos de una población de 171 pacientes adultos afectados con patología nasal, atendidos en la consulta externa del Departamento de Otorrinolaringología (ORL) del Hospital Universitario del Caribe de Cartagena de Indias (Colombia), entre agosto/2012 a julio/2013. La técnica de muestreo fue secuencial por conveniencia y se tuvieron como criterios de exclusión la fibrosis quística, inmunodeficiencias, problemas mucociliares congénitos, micetomas no invasivos, micosis invasivas, adicción a la cocaína y neoplasias.
Toma y procesamiento de muestras
Para cada paciente se utilizó un único hisopo estéril para recolectar muestras de meato medio, rinofaringe, y secreciones nasales. Una vez tomadas las muestras, los hisopos se introdujeron en medio de transporte microbiológico Stuart, y se llevaron al laboratorio de Microbiología de la Universidad de Cartagena (Cartagena, Colombia), para su procesamiento dentro de 8 a 18 horas según protocolos previamente descritos12.
Pruebas de Susceptibilidad a Antibióticos
La susceptibilidad antibiótica de los aislamientos se realizó mediante el método de difusión en disco según las recomendaciones del CLSI (Clinical and Laboratory Standards Institute). Se evaluaron los antibióticos cefoxitina (30μg), oxacilina (1μg), eritromicina (15μg), clindamicina (2 mg), gentamicina (10μg), rifampicina (5μg), penicilina (10 μg), cloranfenicol (30ug), tetraciclina (30 μg), linezolida (30 μg), ciprofloxacina (5 μg ), ampicilina (10 μg ), levofloxacina (5 μg ), y cefalotina (30 μg). Para determinar la resistencia a clindamicina inducida por macrólidos, se utilizó la prueba D. La susceptibilidad a vancomicina para cepas SARM se evaluó mediante el método de microdilución en agar, usando concentraciones seriadas de 0,5 a 32 µg/ml.
Extracción de ADN Genómico
ADN genómico de cada aislamiento fue obtenido siguiendo el protocolo descrito previamente por Millar13 et al con algunas modificaciones. Brevemente, cada aislamiento fue sub-cultivado en agar nutritivo por 24 h a 37oC, y 3-5 colonias fueron suspendidas en 1ml de Tris 0.5M, centrifugado a 13,000 rpm x 5min. El sobrenadante fue descartado y el sedimento fue homogenizado en 500 ul de tampón TE (10mM Tris; 1mM EDTA, pH:8.0), calentado a 100ºC por 30min, enfriado a -35ºC por 20 minutos, descongelado a 65ºC y finalmente centrifugado a 13.000 rpm por 15 minutos. El sobrenadante con el ADN bacteriano fue recolectado y almacenado a -20ºC hasta su uso en ensayos de PCR.
Amplificación de los genes nuc, mec-A, y lukS/F-PV mediante ensayo de PCR múltiple
Se realizaron ensayos de PCR múltiple para la determinación en cada uno de los aislamientos de los genes lukS/F-PV, mecA, y nuc utilizando cebadores previamente descritos14,15,16. Las cepas de S. aureus ATCC 33591 (mecA +; nuc +; PVL -) y ATCC 25923 (mecA - ; nuc +; PVL +) fueron usadas como controles de la amplificación y como control negativo se utilizó agua pura. Todos los aislamientos fueron sometidos a PCR múltiple usando tres pares de cebadores previamente reportados: MecA1F – MecA2R que amplifica un fragmento de 147 pb del gen mecA; Nuc1F – Nuc2R que amplifica un fragmento de 300 pb del gen nuc específico del S. aureus, y LukPV1F – LukPV2R que amplifica un fragmento de 437 pb de los genes de la leucocidina PVL. La reacción de amplificación se llevó a cabo en un volumen de 25uL, que contenía 12.5uL de la mezcla de PCR (Go-Taq Green Master Mix; Promega®), 0.2 uM de cada primer y 5 uL de ADN molde.
Tipificación y subtipificación del elemento SCCmec mediante PCR múltiple
Todos los aislamientos confirmados como SARM fueron sometidos a tipificación y sub-tipificación del elemento SCCmec mediante ensayo de PCR múltiple siguiendo el protocolo descrito por Zhang et al16. Como controles se usaron las cepas de S. aureus NCTC10442 para SCCmec tipo I, N315 para SCCmec tipo II, y JCSC4744 para SCCmec tipo IV. A los aislamientos con SCCmec tipo IV se les determinó el subtipo mediante amplificación múltiple de fragmentos específicos de la región variable J1 usando cebadores para los subtipos SCCmec IV : (IVa, 278 pb), (IVb, 336 pb), y (IVc, 483 pb), y las cepas controles de referencia: MW2 (IVa), JCSC2172 (IVb), y JCSC4178 (IVc)17. Las condiciones fueron: un ciclo inicial de desnaturalización a 94°C por 4 min, seguido por 30 ciclos de 94°C por 30 seg , 53°C por 30 seg, y 72°C por 1 min, con un ciclo de extensión final a 72°C por 4 min. Los productos de la PCR se visualizaron en un gel de agarosa al 2% teñido con bromuro de etidio bajo iluminación UV.
Asignación a los complejos clónales (CC5) y (CC8)
Se utilizó el protocolo descrito por Escobar et al18, seguido de digestión con la enzima de restricción Hha-I, que permite diferenciar los tipos de secuencia 5 (ST5) y 8 (ST8) correspondientes a aislamientos SARM-AH y SARM-AC, respectivamente. Los cebadores amplifican un fragmento de 557 pb del gen gmk y después de la digestión con la enzima HhaI, se generan fragmentos de 429 y 124 pb para el ST5 mientras que para el ST8 se generan fragmentos de 323, 124, y 105 pb. Se usaron como controles las cepas de referencia: HDE3 (clon Pediátrico, ST5-SARM-IV) y USA300-0114 (ST8-SARM-IVa). Los productos de la PCR se sometieron a digestión con la enzima de restricción Hha-I a 37ºC por 2 horas.
Tipificación por Electroforesis en Gel por Campos Pulsados (PFGE)
Se suspendió una colonia de cada aislamiento puro de S. aureus en caldo tripticasa de soya (TSB), y se incubó en agitación a 200 rpm a 37ºC por 18hr. Se centrifugó a 4.000 rpm por 10 min a 4ºC, se descartó el sobrenadante y se resuspendió el sedimento en tampón de suspensión celular. Se centrifugó a 11.000 rpm por 10 minutos a 4 ºC, descartándose el sobrenadante y resuspendiendo el sedimento nuevamente en este mismo tampón, luego se sometió a digestión con lisostafina en moldes de agarosa al 2%, y tratamiento con Proteinasa K. Luego de ser lavados, los bloques fueron sometidos a restricción con la enzima SmaI. Se utilizó el sistema CHEF (BioRad) con parámetros: Angulo 120º, gradiente de voltaje 6.0 v/cm, temperatura de 14ºC. Se programaron 2 bloques de electroforesis en pulsos de la siguiente manera: Bloque 1: Pulso inicial de 5 seg; Pulso final de 15 seg; tiempo de corrido: 10 horas. Bloque 2: Pulso inicial de 15 seg; Pulso final de 60 seg; tiempo de corrido: 13 horas. Finalmente, el ADN fragmentado se sometió a tinción con bromuro de etidio durante una hora, y se visualizó en un transiluminador de luz UV.
Análisis de los datos de PFGE
Los geles fueron fotografiados y digitalizados en formato TIFF para análisis ulterior de los patrones de PFGE utilizando el programa computarizado BioNumerics versión 4.0 (Applied Maths, Sint-Martens-Latem, Belgium). La cepa de Staphylococcus aureus NCTC8325 fue utilizada como estándar de referencia para normalizar el gel. Las bandas fueron asignadas manualmente, el coeficiente de similitud de Dice fue aplicado para comparar los patrones de macrorestricción. Para visualizar mejor la relación existente entre los aislamientos se construyó un dendograma empleando el método de los promedios aritméticos no ponderados (UPGMA unweighted pair group method with arithmetic averages) utilizando un parámetro de optimización de 1,5% y 1,5% de tolerancia en la posición de las bandas. Un coeficiente de similitud de 80% fue seleccionado para definir los grupos de tipos PFGE.
Análisis estadístico
Microsoft Office Excel se utilizó para registrar resultados microbiológicos y moleculares de los aislamientos de las cepas en estudio y los datos se exportaron al software estadístico IBM SPSS v20 (IBM Corporation), y se determinó la distribución de frecuencias de variables medidas en escala nominal y numérica.
Ética
El presente estudio contó con el consentimiento informado de los participantes, y con la aprobación de los Comités de Ética de la Universidad de Cartagena y de la Institución Hospitalaria participante.
Resultados
La prevalencia de colonización de S. aureus encontrada en este estudio es del 22,8%, correspondiente a 39 aislamientos obtenidos de un total de 171 pacientes participantes. Un total de 9 aislamientos (23,1%) presentaron el gen mecA, característico de las cepas SARM. Los 30 aislamientos restantes tuvieron ausente este gen, por lo que fueron considerados como cepas SASM (76,9%), para una prevalencia de 17,5% (30 aislamientos de 171 pacientes). La prevalencia de SARM en la población estudiada fue de 5,26% (9 aislamientos de 171 pacientes).
La presencia de los genes para la leucocidina PVL se observa en 6 (66,7%) de los 9 aislamientos SARM y 12 (40%) de los 30 aislamientos SASM (Figura 1).
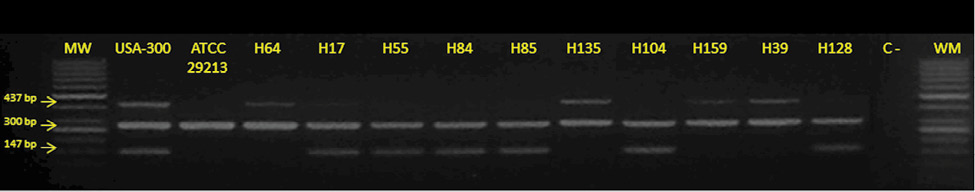
Figura 1. PCR para detección de nuc, mecA y PVL. PCR múltiple para la detección de los genes nuc, mecA y PVL para confirmar la especie Staphylococcus aureus (gen nuc, 300 bp), resistencia a la meticilina (gen mecA, 147 bp) y la presencia de los genes para PVL (gen lukS/lukF-PV, 437 bp). Carriles 1 y 15: MW (marcador de peso molecular de ADN). Carriles 2 y 3: cepa de referencia USA300 (nuc +, mecA +, PVL+) y la cepa de referencia ATCC 29213 (nuc +, mecA -, PVL-) respectivamente. Los carriles 4 a 13: aislamientos representativos del estudio. Carril 14: control negativo de la reacción de PCR.
Las pruebas de susceptibilidad a antibióticos realizadas para los 39 aislamientos se muestran en la Tabla 1. No se encuentran aislamientos con resistencia inducible a la clindamicina usando la prueba D. Para el antibiótico vancomicina, el MIC de todos los aislamientos de SARM fue ≤ 2 mg/ml.
Tabla 1. Sensibilidad antibiótica de los aislamientos de S. aureus (n=39)
|
S = susceptible I = resistencia intermedia R = resistente |
|||
|
ANTIBIOTICO |
S |
I |
R |
|
n (%) |
n (%) |
n (%) |
|
|
Ciprofloxacina |
37 (94,9) |
1 (2,6) |
1 (2,6) |
|
Linezolida |
37 (94,9) |
0 |
2 (5,1) |
|
Penicilina |
4 (10,3) |
0 |
35 (89,7) |
|
Clindamicina |
24 (61,5) |
7 (17,95) |
8 (20,5) |
|
Eritromicina |
13 (33,3) |
19 (48,7) |
7 (17,95) |
|
Cefoxitina |
30 (76,9) |
0 |
9 (23,1) |
|
Ampicilina |
7 (17,95) |
0 |
32 (82,05) |
|
Oxacilina |
31 (79,5) |
0 |
8 (20,5) |
|
Gentamicina |
38 (97,4) |
0 |
1 (2,6) |
|
Rifampicina |
33 (84,6) |
0 |
6 (15,4) |
|
Levofloxacina |
38 (97,4) |
0 |
1 (2,6) |
|
Cefalotina |
6 (15,4) |
6 (15,4) |
27 (69,2) |
|
Tetraciclina |
17 (43,6) |
1 (2,6) |
21 (53,8) |
|
Cloranfenicol |
35 (89,7) |
2 (5,1) |
2 (5,1) |
De los 9 aislamientos SARM, 66,7% se asignan al complejo clonal CC8 (6 de 9 SARM) y 33,3% al CC5 (3 de 9 SARM), mientras que de los 30 aislamientos SASM, 33,3% se asignan al CC8 (10 de 30 SASM), 13,3% al CC5 (4 de 30 SASM), y 53,3% no pertenecen a ninguno de estos dos complejos (16 de 30 SASM). La Figura 2 muestra la asignación a los complejos CC5 y CC8 de algunos aislamientos representativos del estudio.
Los aislamientos SARM se someten a tipificación SCCmec y aquellos que portan el tipo IV son sometidos a sub-tipificación de dicho elemento. De acuerdo a esto, se encuentra la siguiente distribución: 7 aislamientos portan SCCmec tipo IV y 2 portan SCCmec tipo I. Uno de los aislamientos con SCCmec tipo I pertenece al complejo clonal CC5 (CC5-SARM-I) y el otro aislamiento pertenece al complejo clonal CC8 (CC8-SARM-I). La Figura 3 muestra los tipos SCCmec de algunos aislamientos representativos.
En cuanto a los 7 aislamientos con SCCmec tipo IV, se encuentra que dos portan el subtipo IVa y pertenecen al complejo clonal CC8 (CC8-SARM-IVa). Los cinco restantes portan el subtipo IVc, tres de los cuales pertenecen al complejo clonal CC8 (CC8-SARM-IVc) y los otros dos al CC5 (CC5-SARM-IVc). La Figura 4 muestra los subtipos SCCmec de algunos aislamientos representativos.
La distribución de frecuencias de los aislamientos SARM con base en sus complejos clonales y tipificación SCCmec son: 33,3% CC8-SARM-IVc (n=3, variante USA300-LV); 22,2% CC8-SARM-IVa (n= 2, USA300-0114); 22,2% CC5-SARM-IVc (n=2, clon Pediátrico); 11,1% CC5-SARM-I (n=1, clon Chileno/Cordobés); y 11,1% CC8-SARM-I (n=1). (Tabla 2)

Figura 2. PCR para asignación a complejos clonales (CC5) y (CC8). PCR Múltiple para identificación de los complejos CC5 y CC8 de S. aureus. Carril 1: MW (marcador ADN de peso molecular). Carril 2: Clon chileno (CC5); Carril 3: Clon USA 300 (CC8); Carriles 4, 5, 6: aislamientos de S. aureus pertenecientes al CC8; Carriles 7 y 8: aislamientos de S. aureus pertenecientes al CC5; Carril 9: control negativo de la PCR.
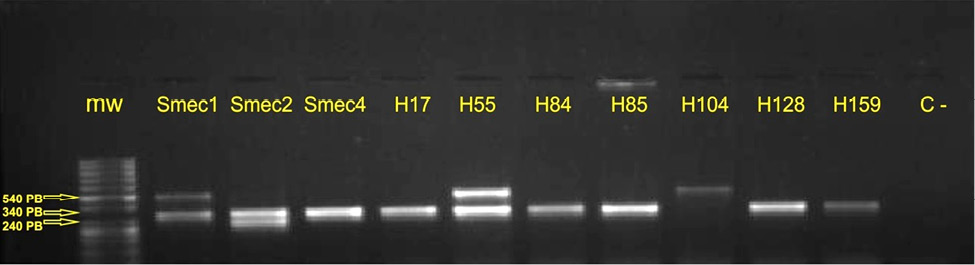
Figura 3. PCR múltiple para tipificación del elemento SCCmec. PCR múltiple se llevó a cabo para determinar los tipos de SCCmec de los aislamientos SARM. Carril 1: mw (marcador ADN de peso molecular). Carril 2: S. aureus ATCC 33591 (SCCmec tipo I). Carril 3: S. aureus N315 (SCCmec tipo II). Carril 4: S. aureus JCSC4744 (SCCmec tipo IV). Los carriles 5 a 11: aislamientos representativos del estudio. Carril 12: control negativo de la reacción de PCR.
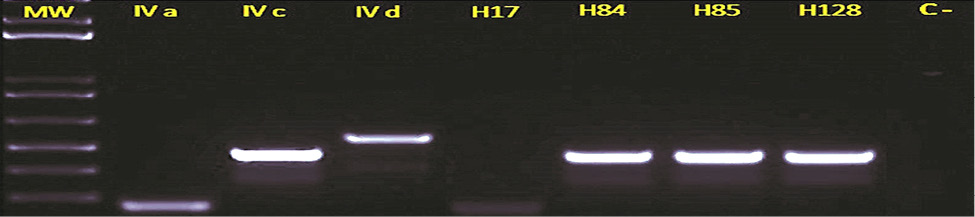
Figura 4. PCR múltiple para la subtipificación del elemento SCCmec IV. PCR múltiple fue realizada en un grupo de 5 aislamientos SARM con SCCmec tipo IV. Carril 1: MW (marcador ADN de peso molecular). Carriles 2-4: cepas de referencia MW2, Q2314 y JCSC4469, con subtipos IVa , IVc y IVd respectivamente. Carril 5: aislamiento con subtipo IVa. Carriles 6-8: aislamientos con subtipo IVc. Carril 9: control negativo de la reacción de PCR.
Tabla 2. Distribución de los aislamientos de S. aureus en complejos clonales
|
Aislamientos de S. aureus ( n = 39 ) |
|
|
SARM CC8 |
6 (15,38%) |
|
SASM CC8 |
10 (25,64%) |
|
sarm cc5 |
3 (7,69%) |
|
sasm cc5 |
4 (10,26%) |
|
SASM (CC no determinado) |
16 (41%) |
|
Distribución de los aislamientos SARM según el CC y subtipo SCCmec (n=9) |
|
|
CC8-SARM-IVc |
3 (33,3%) |
|
CC8-SARM-IVa |
2 (22,2%) |
|
CC5-SARM-IVc |
2 (22,2%) |
|
CC5-SARM-I |
1 (11,1%) |
|
CC8-SARM-I |
1 (11,1%) |
La Figura 5 muestra el análisis de patrones de bandas PFGE de 25 aislamientos, tanto SARM como SASM, en el que se encuentra un coeficiente de similitud de 82% con el clon USA300-0114 (CC8-SARM-IVa).

Figura 5. Dendrograma de patrones PFGE y características de los aislamientos de S. aureus (n=25). Electroforesis en gel de campo pulsado (PFGE) en el que se muestra la relación genética entre 25 aislamientos representativos de S. aureus obtenidos en el estudio. La línea discontinua corresponde a un coeficiente de similitud de 82% utilizado para definir clones relacionados por PFGE. Aislamientos: CC8-SCCmecIVc (H128, H84, H159); CC8-SCCmecIVa (H17, C30); CC5-SCCmecIVc (C9, H85); CC5-SCCmecI (H104); CC8-SCCmecI (H55). Cepas control: USA 300-0114 (CC8-SCCmecIVa); clon Chileno/Cordobés (CC5-SCCmecI); clon pediátrico (CC5-SCCmecIV).
Discusión
Staphylococcus aureus resistente a meticilina (SARM) representa una seria amenaza para la salud pública, debido a la diseminación de los clones SARM pandémicos con mayor virulencia y resistencia antimicrobiana. En América Latina estas cepas SARM son consideradas como causa principal de infecciones nosocomiales, a la vez que con más frecuencia se les implica como agentes causales de infecciones adquiridas en la comunidad3,10, por lo cual ya no se considera al SARM como patógeno nosocomial estricto19,20. En este estudio se observó una alta resistencia a los antibióticos penicilina (89,7%), ampicilina (82%) y cefalotina (69,2%). Además, 7 aislamientos (17,9%) fueron resistentes a más de 2 antibióticos. Como era de esperar, los aislamientos SARM tuvieron una alta resistencia a los β-lactámicos21. Uno de los principales elementos que actúa en la resistencia a la meticilina en S. aureus es la proteína de unión a penicilina, PBP2a. Esta proteína es insensible a los antibióticos β-lactámicos como la meticilina. Se ha planteado que PBP2a se hace cargo de la biosíntesis del peptidoglicano en presencia de niveles de otra manera letales de antibióticos β-lactámicos21,22.
Se encuentra una alta frecuencia de susceptibilidad en los aislamientos a antibióticos como gentamicina (97,4%), levofloxacina (97,4%) ciprofloxacina (94,9%), cloranfenicol (89,7%), linezolida (94,9%) y rifampicina (84,6%). En contraste, otros estudios reportan altas frecuencias de resistencia a estos antibióticos23-25. Estudios en Brasil evalúan la resistencia a gentamicina y aminoglucósidos relacionados en aislamientos de S. aureus 26. En el caso de las fluoroquinolonas levofloxacina y ciprofloxacina, los resultados en este estudio son similares a los reportados en Nigeria en el 2011, donde gran parte de los aislamientos fueron sensibles a estos antibacterianos27. Con relación al antibiótico vancomicina, donde la MIC de todos los aislamientos de S. aureus es ≤ 2 µg/ml, el presente estudio coincide con el reportado por Gregory Steinkraus et al entre los años 2001 y 2005 en el cual no se encuentra resistencia a la vancomicina28. Sin embargo, dos informes recientes de infecciones ocasionadas por S. aureus resistente a vancomicina (VRSA) son de gran preocupación, ya que reflejan tanto una resistencia total y un mecanismo diferente para su propagación29,30. La incidencia de S. aureus con resistencia intermedia a glicopéptidos y SARM hetero-resistente sugiere que la resistencia completa a glicopéptidos puede desplegarse ágilmente y restringir la utilidad de vancomicina, lo cual resalta la necesidad de contar con nuevos antibióticos31.
Diversos clones de S. aureus han surgido con una resistencia inducida a clindamicina seguida de una modificación del blanco ribosómico. La resistencia a clindamicina es inducida por macrólidos32. Las investigaciones en los Estados Unidos evidencian una alta resistencia inducida a clindamicina en las cepas de S. aureus (50% de cepas SARM y 60% de cepas SASM)33, aunque esto puede cambiar ya que el cambio clonal ha demostrado afectar a la resistencia inducida a clindamicina34.
El 2,6% de los aislamientos de este estudio presentaron resistencia a los antibióticos levofloxacina y ciprofloxacina, los cuales son fluoroquinolonas utilizados con frecuencia en el área de otorrinolaringología (ORL) del Hospital Universitario del Caribe (Cartagena, Colombia). En contraste, otros estudios reportan frecuencias más altas de resistencia a fluoroquinolonas en aislamientos de S. aureus35,36. Por otra parte, otros estudios que han evaluado la susceptibilidad a antibióticos de aislamientos colonizantes de S. aureus reportan que todas las cepas fueron sensibles a gentamicina37,38. En la literatura mundial, esta tasa de resistencia es mínima en algunos países, gracias a su utilización limitada y a las políticas de control diseñadas en las décadas de los setentas y ochentas39. Resulta relevante que se implementen a nivel local estrategias similares en las que se limite el uso del antibiótico gentamicina y determinar si el mismo representa una alternativa costo efectiva frente al S. aureus.
Los 9 aislamientos SARM se identifican mediante PCR múltiple, mostrando poseer el gen mecA, presente en estas cepas. Estos 9 aislamientos se confirman fenotípicamente mediante el uso del sensidisco cefoxitina, mostrando resistencia a este antibiótico. La cefoxitina es una cefamicina que funciona como un inductor más dinámico que la oxacilina sobre la síntesis de PBP2 en aislados de S. aureus que poseen el gen mecA. Por lo tanto, la cefoxitina parece más eficaz que la oxacilina en la identificación de la resistencia a meticilina40.
Las tasas de colonización encontradas para SARM (5,26%) y SASM (17,5%) en este estudio, pueden constituir un riesgo para la comunidad, teniendo en cuenta que estas bacterias son causa frecuente de infecciones41,42. El contacto cercano de estos pacientes con la comunidad pudiera facilitar la transmisión y propagación de estas cepas a individuos susceptibles de adquirir una infección por S. aureus. Aunque la función de PVL en la patogenesis y severidad de infecciones estafilocócicas es aún controversial, el hallazgo de los genes de la leucocidina PVL en 6 (66,7%) de 9 aislamientos SARM y 12 (40%) de 30 aislamientos SASM, pudiera representar un agravante y factor de riesgo relevante para las infecciones por S. aureus43, teniendo en cuenta que algunas investigaciones sugieren que la portación de los genes de la leucocidina PVL en las cepas de S. aureus aumenta su virulencia y es responsable de infecciones graves tales como las óseas, articulares y neumonía necrotizante15,44,45. Debido al S. aureus PVL+ asociado a la comunidad, la neumonía necrotizante es una infección procedente46. En Europa, la mayoría de los casos de neumonía necrotizante se deben a cepas SASM45.
En Colombia, varios estudios han identificado a cepas PVL+ de S. aureus, tanto SASM como SARM, como fuente importante de infecciones de diversa gravedad47,48, lo cual evidencia una vez más un serio problema de salud pública en Colombia y por lo tanto una alerta sobre el riesgo potencial para la introducción de estas cepas en el entorno sanitario.
Los aislamientos SARM que se observan en este estudio tienen diferentes tipos de SCCmec encontrados tanto a nivel nosocomial, como a nivel comunitario, lo cual demuestra la variedad de cepas SARM diseminadas localmente en la ciudad de Cartagena y sus alrededores. El SARM SCCmec tipo IV se puede identificar mediante la PCR múltiple en 7 cepas SARM; estas cepas son del tipo asociado a la comunidad (AC-SARM). Además se encuentran aislamientos que portan el SCCmec tipo I, el cual ha sido primordialmente asociado con al ámbito nosocomial49, lo que demuestra la versátil epidemiología y distribución de las cepas SARM en la comunidad de Cartagena de Indias.
En cuanto a lo encontrado en la tipificación PFGE de los aislamientos SARM, se evidencia que los aislamientos relacionados con los clones USA300 y su variante USA300-LV, predominan con una frecuencia de 55,5% (n=5), seguidos de un 22,2% (n=2) y 11,1% (n=1) de los clones pediátrico y chileno, respectivamente. En 2005, Cruz et al5 evaluaron 200 cepas SARM recolectadas entre 1996 y 2003 que procedían en gran parte de centros sanitarios asistenciales de las ciudades de Bogotá y Cali (Colombia), con 48% y 45%, respectivamente. En este caso los investigadores no identificaron cepas pertenecientes al clon pediátrico, el cual prevaleció a principios de los años 90; solo hallaron cepas correspondientes al clon chileno, convirtiéndose éste en el primer reporte del clon chileno en nuestro país, lo cual, según los autores, demostraba un cambio en la población genética de SARM en el país.
Álvarez et al.6 presentaron en el 2006 el primer reporte de AC-SARM en Colombia; posteriormente, Reyes et al50 en 2009, y Álvarez et al51 en 2010, reportaron el clon USA300 (ST8-MRSA-SCCmecIV) como causante de infecciones nosocomiales. Cabe resaltar que los aislamientos analizados estuvieron relacionados con la variante USA300-SCCmecIVc, el cual se encuentra asociado a la comunidad, lo que revela un desplazamiento de este tipo de SARM hacia el ambiente hospitalario, habiéndose convertido según reportes recientes en el principal causante de infecciones de S. aureus asociadas al cuidado de la salud47,50,52-54.
Es relevante citar que estas cepas relacionadas con la variante USA300-SCCmec-IVc difieren del prototipo de cepas USA300-0114 en que alojan el SCCmec IVc en lugar del IVa, aunque comparten características similares con el USA300. Esta variante latinoamericana (USA300-LV), que presenta ausencia del elemento móvil catabólico de arginina (ACME) y alta prevalencia de resistencia a la tetraciclina fue recientemente descrita55. El alto índice de cepas con el casete cromosómico tipo IV pudiera deberse a las propiedades que este tipo de casete le aporta a la bacteria, tales como: 1) Su dimensión pequeña, que le permite transferirse de forma más simple y tener una mayor rapidez de replicación; 2) Un número pequeño de genes de resistencia a fármacos, en contraste con los presentados por las cepas que portan los SCCmec tipo I, II o III, y 3) Una tasa de crecimiento mayor, que representa una ventaja sobre otras bacterias en cuanto a la colonización exitosa56,57.
En el presente estudio se encuentran cepas SARM portadoras de los elementos SCCmecI y SCCmecIV, que a su vez son asignadas al complejo clonal CC5, las cuales se encuentran colonizando pacientes que acuden a la consulta externa del Hospital Universitario del Caribe de la ciudad de Cartagena, Colombia. Los clones SARM nosocomiales, como el Pediátrico (ST5-SCCmecIV) y Chileno/cordobés (ST5-SCCmecI), han ido reemplazando a los clones tradicionales de AH-SARM. En Colombia se han identificado estos clones hospitalarios principalmente en hospitales de tercer nivel en Bogotá4. Sin embargo, estudios más recientes han reportado que cepas asociadas a AC-SARM han comenzado a remplazar las cepas tradicionales de AH-SARM54,58, lo cual se ha visto en países como Estados Unidos y Taiwán, donde la prevalencia de AC-SARM es alta, describiéndose un aumento en su incidencia en el ámbito hospitalario.
En este estudio se encuentra una mayor frecuencia del complejo clonal CC8, el cual es el cuarto complejo clonal más común en la mayoría de países de Europa, así como en Argentina, Canadá y los Estados Unidos, representando en este país a la mayoría de aislamientos USA300 AC-SARM1. También es el principal tipo según la tipificación spa, asociado con USA300-LV, que se ha reportado en varios países fuera de América Latina, entre ellos España, Italia, Bélgica, los Países Bajos, el Reino Unido y Australia 55. Por el contrario, el complejo clonal (CC5), asociado principalmente con el SCC mec tipo I, es uno de los tipos spa más comunes en América del Sur, incluyendo Argentina, Brasil, Chile y Paraguay, y se relaciona con el clon Chileno/Cordobés59,60, el cual fue encontrado con una menor frecuencia en este estudio. Considerando la naturaleza cambiante de los clones SARM y su importancia en la vigilancia local, es necesario hacer estudios longitudinales que describan el comportamiento en el tiempo de los clones SARM en los hospitales locales y clínicas de la ciudad, en los cuales SARM es prevalente.
Existen varios estudios a nivel de Colombia y Latinoamérica con relación a la infección y colonización nasal con S. aureus11,61-63. Sin embargo, no existen estudios específicos de colonización en pacientes con patologías nasales en la ciudad de Cartagena, por lo tanto, resulta relevante un estudio de este tipo, los cuales pudieran servir de base para el diseño de estrategias dirigidas a optimizar el tratamiento antibiótico frente a las múltiples patologías nasales, y así lograr un control racional de los mismos.
Los cambios constantes en la epidemiología del S. aureus confirman que esta bacteria sigue siendo una importante amenaza para la salud pública humana, de allí la importancia de la vigilancia local y la difusión de los resultados, sobre todo en países en desarrollo como Colombia, donde el conocimiento de la epidemiología y la dinámica de la transmisión de S. aureus aún es limitada. La principal limitación del presente estudio fue que no se pudo determinar la asociación entre las variables clínicas de los pacientes y las características moleculares que presentaron los aislamientos, por lo cual no es posible establecer y documentar el vínculo entre las patologías nasales y la colonización por esta bacteria.
Agradecimientos: Los autores agradecen a la Universidad de Cartagena y al Hospital Universitario del Caribe por su apoyo en la realización de este estudio. Especial agradecimiento al Laboratorio de Genética Molecular Bacteriana de la Universidad El Bosque por asesoría en los ensayos de tipificación por PCR múltiple y a Juan Rebollo por asistencia técnica en la realización y análisis de PFGE.
Conflictos de interés: Los autores declaran no tener conflicto de intereses en relación al tema tratado en el artículo.
Fuentes de financiación: Universidad de Cartagena Proyecto #RES 4776-2010 (Grupo Genética y Biología Molecular) y Proyecto #RES 01297-2012 ( Grupo Microbiología Clínica y Ambiental).
Literatura citada
1. Deurenberg RH, Stobberingh EE. The evolution of Staphylococcus aureus. Infect Genet Evol 2008; 8(6):747-63.
2. DeLeo FR, Otto M, Kreiswirth BN, Chambers HF. Community-associated meticillin-resistant Staphylococcus aureus. Lancet 2010; 375(9725):1557-68.
3. Guzman-Blanco M, Mejia C, Isturiz R, Alvarez C, Bavestrello L, Gotuzzo E, et al. Epidemiology of methicillin-resistant Staphylococcus aureus (MRSA) in Latin America. Int J Antimicrob Agents 2009; 34(4):304-8.
4. Gomes AR, Sanches IS, Aires de Sousa M, Castaneda E, de Lencastre H. Molecular epidemiology of methicillin-resistant Staphylococcus aureus in Colombian hospitals: dominance of a single unique multidrug-resistant clone. Microb Drug Resist 2001; 7(1):23-32.
5. Cruz C, Moreno J, Renzoni A, Hidalgo M, Reyes J, Schrenzel J, et al. Tracking methicillin-resistant Staphylococcus aureus clones in Colombian hospitals over 7 years (1996-2003): emergence of a new dominant clone. Int J Antimicrob Agents 2005; 26(6):457-62.
6. Alvarez CA, Barrientes OJ, Leal AL, Contreras GA, Barrero L, Rincon S, et al. Community-associated methicillin-resistant Staphylococcus aureus, Colombia. Emerg Infect Dis 2006; 12(12):2000-1.
7. Chambers HF. The changing epidemiology of Staphylococcus aureus?. Emerg Infect Dis 2001; 7(2):178-82.
8. Goff DA, Dowzicky MJ. Prevalence and regional variation in meticillin-resistant Staphylococcus aureus (MRSA) in the USA and comparative in vitro activity of tigecycline, a glycylcycline antimicrobial. J Med Microbiol 2007; 56(Pt 9):1189-93.
9. Aires De Sousa M, Miragaia M, Sanches IS, Avila S, Adamson I, Casagrande ST, et al. Three-year assessment of methicillin-resistant Staphylococcus aureus clones in Latin America from 1996 to 1998. J Clin Microbiol 2001; 39(6):2197-205.
10. Rodriguez-Noriega E, Seas C. The changing pattern of methicillin-resistant Staphylococcus aureus clones in Latin America: implications for clinical practice in the region. Braz J Infect Dis 2010;14 (Suppl) 2:S87-96.
11. Rodriguez-Noriega E, Seas C, Guzman-Blanco M, Mejia C, Alvarez C, Bavestrello L, et al. Evolution of methicillin-resistant Staphylococcus aureus clones in Latin America. Int J Infect Dis 2010; 14(7):e560-6.
12. Bettin A, Causil C, Reyes N. Molecular identification and antimicrobial susceptibility of Staphylococcus aureus nasal isolates from medical students in Cartagena, Colombia. Braz J Infect Dis 2012; 16(4):329-34.
13. Millar BC, Jiru X, Moore JE, Earle JA. A simple and sensitive method to extract bacterial, yeast and fungal DNA from blood culture material. J Microbiol Methods 2000; 42(2):139-47.
14. Brakstad OG, Aasbakk K, Maeland JA. Detection of Staphylococcus aureus by polymerase chain reaction amplification of the nuc gene. J Clin Microbiol 1992; 30(7):1654-60.
15. Lina G, Piemont Y, Godail-Gamot F, Bes M, Peter MO, Gauduchon V, et al. Involvement of Panton-Valentine leukocidin-producing Staphylococcus aureus in primary skin infections and pneumonia. Clin Infect Dis 1999; 29(5):1128-32.
16. Zhang K, McClure JA, Elsayed S, Louie T, Conly JM. Novel multiplex PCR assay for characterization and concomitant subtyping of staphylococcal cassette chromosome mec types I to V in methicillin-resistant Staphylococcus aureus. J Clin Microbiol 2005; 43(10):5026-33.
17. Milheirico C, Oliveira DC, de Lencastre H. Multiplex PCR strategy for subtyping the staphylococcal cassette chromosome mec type IV in methicillin-resistant Staphylococcus aureus: ‘SCCmec IV multiplex’. J Antimicrob Chemother 2007; 60(1):42-8.
18. Escobar JA, Gomez IT, Murillo MJ, Castro BE, Chavarro B, Marquez RA, et al. Design of two molecular methodologies for the rapid identification of Colombian community-acquired methicillin-resistant Staphylococcus aureus isolates. Biomedica 2012; 32(2):214-23.
19. Maltezou HC, Giamarellou H. Community-acquired methicillin-resistant Staphylococcus aureus infections. Int J Antimicrob Agents 2006; 27(2):87-96.
20. Otter JA, French GL. Community-associated meticillin-resistant Staphylococcus aureus strains as a cause of healthcare-associated infection. J Hosp Infect 2011; 79(3):189-93.
21. Lim D, Strynadka NC. Structural basis for the beta lactam resistance of PBP2a from methicillin-resistant Staphylococcus aureus. Nat Struct Biol 2002; 9(11):870-6.
22. Pinho MG, de Lencastre H, Tomasz A. An acquired and a native penicillin-binding protein cooperate in building the cell wall of drug-resistant staphylococci. Proc Natl Acad Sci U S A 2001; 98(19):10886-91.
23. Diekema DJ, Pfaller MA, Schmitz FJ, Smayevsky J, Bell J, Jones RN, et al. Survey of infections due to Staphylococcus species: frequency of occurrence and antimicrobial susceptibility of isolates collected in the United States, Canada, Latin America, Europe, and the Western Pacific region for the SENTRY Antimicrobial Surveillance Program, 1997-1999. Clin Infect Dis 2001; 32 Suppl 2:S114-32.
24. Holmes RL, Jorgensen JH. Inhibitory activities of 11 antimicrobial agents and bactericidal activities of vancomycin and daptomycin against invasive methicillin-resistant Staphylococcus aureus isolates obtained from 1999 through 2006. Antimicrob Agents Chemother 2008; 52(2):757-60.
25. Huang H, Flynn NM, King JH, Monchaud C, Morita M, Cohen SH. Comparisons of community-associated methicillin-resistant Staphylococcus aureus (MRSA) and hospital-associated MSRA infections in Sacramento, California. J Clin Microbiol 2006; 44(7):2423-7.
26. Freitas FI, Guedes-Stehling E, Siqueira-Junior JP. Resistance to gentamicin and related aminoglycosides in Staphylococcus aureus isolated in Brazil. Lett Appl Microbiol 1999; 29(3):197-201.
27. Nwankwo EO, Nasiru MS. Antibiotic sensitivity pattern of Staphylococcus aureus from clinical isolates in a tertiary health institution in Kano, Northwestern Nigeria. Pan Afr Med J 2011; 8:4.
28. Steinkraus G, White R, Friedrich L. Vancomycin MIC creep in non-vancomycin-intermediate Staphylococcus aureus (VISA), vancomycin-susceptible clinical methicillin-resistant S. aureus (MRSA) blood isolates from 2001-05. J Antimicrob Chemother 2007; 60(4):788-94.
29. Gobernado M. [Staphylococcus aureus resistance. Now vancomycin]. Rev Esp Quimioter 2002; 15(3):211-4.
30. Park KH, Kim ES, Kim HS, Park SJ, Bang KM, Park HJ, et al. Comparison of the clinical features, bacterial genotypes and outcomes of patients with bacteraemia due to heteroresistant vancomycin-intermediate Staphylococcus aureus and vancomycin-susceptible S. aureus. J Antimicrob Chemother 2012; 67(8):1843-9.
31. Schito GC. The importance of the development of antibiotic resistance in Staphylococcus aureus. Clin Microbiol Infect 2006; 12 (Suppl 1):3-8.
32. Fiebelkorn KR, Crawford SA, McElmeel ML, Jorgensen JH. Practical disk diffusion method for detection of inducible clindamycin resistance in Staphylococcus aureus and coagulase-negative staphylococci. J Clin Microbiol 2003; 41(10):4740-4.
33. Patel M, Waites KB, Moser SA, Cloud GA, Hoesley CJ. Prevalence of inducible clindamycin resistance among community- and hospital-associated Staphylococcus aureus isolates. J Clin Microbiol 2006; 44(7):2481-4.
34. Chavez-Bueno S, Bozdogan B, Katz K, Bowlware KL, Cushion N, Cavuoti D, et al. Inducible clindamycin resistance and molecular epidemiologic trends of pediatric community-acquired methicillin-resistant Staphylococcus aureus in Dallas, Texas. Antimicrob Agents Chemother 2005; 49(6):2283-8.
35. Cheng H, Yuan W, Zeng F, Hu Q, Shang W, Tang D, et al. Molecular and phenotypic evidence for the spread of three major methicillin-resistant Staphylococcus aureus clones associated with two characteristic antimicrobial resistance profiles in China. J Antimicrob Chemother 2013; 68(11):2453-7.
36. Karlowsky JA, Adam HJ, Desjardins M, Lagace-Wiens PR, Hoban DJ, Zhanel GG. Changes in fluoroquinolone resistance over 5 years (CANWARD 2007-11) in bacterial pathogens isolated in Canadian hospitals. J Antimicrob Chemother 2013; 68( Suppl 1):i39-46.
37. Hussain FM, Boyle-Vavra S, Daum RS. Community-acquired methicillin-resistant Staphylococcus aureus colonization in healthy children attending an outpatient pediatric clinic. Pediatr Infect Dis J 2001; 20(8):763-7.
38. Onanuga A, Temedie TC. Nasal carriage of multi-drug resistant Staphylococcus aureus in healthy inhabitants of Amassoma in Niger delta region of Nigeria. Afr Health Sci 2011; 11(2):176-81.
39. Aubry-Damon H, Legrand P, Brun-Buisson C, Astier A, Soussy CJ, Leclercq R. Reemergence of gentamicin-susceptible strains of methicillin-resistant Staphylococcus aureus: roles of an infection control program and changes in aminoglycoside use. Clin Infect Dis 1997; 25(3):647-53.
40. Cauwelier B, Gordts B, Descheemaecker P, Van Landuyt H. Evaluation of a disk diffusion method with cefoxitin (30 microg) for detection of methicillin-resistant Staphylococcus aureus. Eur J Clin Microbiol Infect Dis 2004; 23(5):389-92.
41. Adler A, Temper V, Block CS, Abramson N, Moses AE. Panton-Valentine leukocidin-producing Staphylococcus aureus. Emerg Infect Dis 2006; 12(11):1789-90.
42. Labandeira-Rey M, Couzon F, Boisset S, Brown EL, Bes M, Benito Y, et al. Staphylococcus aureus Panton-Valentine leukocidin causes necrotizing pneumonia. Science 2007; 315(5815):1130-3.
43. Cupane L, Pugacova N, Berzina D, Cauce V, Gardovska D, Miklasevics E. Patients with Panton-Valentine leukocidin positive Staphylococcus aureus infections run an increased risk of longer hospitalisation. Int J Mol Epidemiol Genet 2012; 3(1):48-55.
44. Bocchini CE, Hulten KG, Mason EO, Jr., Gonzalez BE, Hammerman WA, Kaplan SL. Panton-Valentine leukocidin genes are associated with enhanced inflammatory response and local disease in acute hematogenous Staphylococcus aureus osteomyelitis in children. Pediatrics 2006; 117(2):433-40.
45. Gillet Y, Vanhems P, Lina G, Bes M, Vandenesch F, Floret D, et al. Factors predicting mortality in necrotizing community-acquired pneumonia caused by Staphylococcus aureus containing Panton-Valentine leukocidin. Clin Infect Dis 2007; 45(3):315-21.
46. Zetola N, Francis JS, Nuermberger EL, Bishai WR. Community-acquired meticillin-resistant Staphylococcus aureus: an emerging threat. Lancet Infect Dis 2005; 5(5):275-86.
47. Alvarez-Olmos MI, Enriquez SP, Perez-Roth E, Mendez-Alvarez S, Escobar J, Vanegas N, et al. Pediatric cases from Colombia caused by a Panton-Valentine Leukocidin-positive community-acquired methicillin-resistant Staphylococcus aureus ST8-SCCmecIVc clone. Pediatr Infect Dis J 2009; 28(10):935.
48. Jimenez JN, Ocampo AM, Vanegas JM, Rodriguez EA, Garces CG, Patino LA, et al. Characterisation of virulence genes in methicillin susceptible and resistant Staphylococcus aureus isolates from a paediatric population in a university hospital of Medellin, Colombia. Mem Inst Oswaldo Cruz 2011; 106(8):980-5.
49. Qi W, Ender M, O’Brien F, Imhof A, Ruef C, McCallum N, et al. Molecular epidemiology of methicillin-resistant Staphylococcus aureus in Zürich, Switzerland (2003): prevalence of type IV SCCmec and a new SCCmec element associated with isolates from intravenous drug users. J Clin Microbiol 2005; 43(10):5164-70.
50. Reyes J, Rincon S, Diaz L, Panesso D, Contreras GA, Zurita J, et al. Dissemination of methicillin-resistant Staphylococcus aureus USA300 sequence type 8 lineage in Latin America. Clin Infect Dis 2009; 49(12):1861-7.
51. Alvarez CA, Yomayusa N, Leal AL, Moreno J, Mendez-Alvarez S, Ibanez M, et al. Nosocomial infections caused by community-associated methicillin-resistant Staphylococcus aureus in Colombia. Am J Infect Control 2010; 38(4):315-8.
52. Denis O, Deplano A, De Ryck R, Nonhoff C, Struelens MJ. Emergence and spread of gentamicin-susceptible strains of methicillin-resistant Staphylococcus aureus in Belgian hospitals. Microb Drug Resist 2003; 9(1):61-71.
53. Donnio PY, Preney L, Gautier-Lerestif AL, Avril JL, Lafforgue N. Changes in staphylococcal cassette chromosome type and antibiotic resistance profile in methicillin-resistant Staphylococcus aureus isolates from a French hospital over an 11 year period. J Antimicrob Chemother 2004; 53(5):808-13.
54. Popovich KJ, Weinstein RA, Hota B. Are community-associated methicillin-resistant Staphylococcus aureus (MRSA) strains replacing traditional nosocomial MRSA strains? Clin Infect Dis 2008; 46(6):787-94.
55. Nimmo GR. USA300 abroad: global spread of a virulent strain of community-associated methicillin-resistant Staphylococcus aureus. Clin Microbiol Infect 2012; 18(8):725-34.
56. D’Agata EM, Webb GF, Horn MA, Moellering RC, Jr., Ruan S. Modeling the invasion of community-acquired methicillin-resistant Staphylococcus aureus into hospitals. Clin Infect Dis 2009; 48(3):274-84.
57. Okuma K, Iwakawa K, Turnidge JD, Grubb WB, Bell JM, O’Brien FG, et al. Dissemination of new methicillin-resistant Staphylococcus aureus clones in the community. J Clin Microbiol 2002; 40(11):4289-94.
58. Huang YH, Tseng SP, Hu JM, Tsai JC, Hsueh PR, Teng LJ. Clonal spread of SCCmec type IV methicillin-resistant Staphylococcus aureus between community and hospital. Clin Microbiol Infect 2007; 13(7):717-24.
59. Arias CA, Rincon S, Chowdhury S, Martinez E, Coronell W, Reyes J, et al. MRSA USA300 clone and VREF--a U.S.-Colombian connection? N Engl J Med 2008; 359(20):2177-9.
60. Becker AP, Santos O, Castrucci FM, Dias C, D’Azevedo PA. First report of methicillin-resistant Staphylococcus aureus Cordobes/Chilean clone involved in nosocomial infections in Brazil. Epidemiol Infect 2012; 140(8):1372-5.
61. Chua K, Laurent F, Coombs G, Grayson ML, Howden BP. Antimicrobial resistance: Not community-associated methicillin-resistant Staphylococcus aureus (CA-MRSA)! A clinician’s guide to community MRSA - its evolving antimicrobial resistance and implications for therapy. Clin Infect Dis 2011; 52(1):99-114.
62. Moran GJ, Krishnadasan A, Gorwitz RJ, Fosheim GE, McDougal LK, Carey RB, et al. Methicillin-resistant S. aureus infections among patients in the emergency department. N Engl J Med 2006; 355(7):666-74.
63. Rebollo-Pérez J, Ordoñez-Tapia C, Herazo-Herazo C, Reyes-Ramos N. Nasal carriage of Panton Valentine leukocidin-positive methicillin-resistant Staphylococcus aureus in healthy preschool children. Rev Salud Pública 2011; 13(5):824-32.
