Tamizaje virtual de compuestos inhibidores de la SAP-2 de Candida albicans
Juan Rebollo, Ph.D (C)1*, Niradiz Reyes, Ph.D2*, Paola Suárez, MSc3*
*1 Doctorando, Grupo de genética y biología molecular. Sección de Microbiología, Facultad de Medicina, Universidad de Cartagena. Jeanrebollo@gmail.com
2* Docente, Grupo de genética y biología molecular. Sección de Microbiología, Facultad de Medicina, Universidad de Cartagena. nreyesr@unicartagena.edu.co
3* Docente, Grupo de Micología. Sección de Microbiología, Facultad de Medicina, Universidad de Cartagena. psuareza@unicartagena.edu.co
Archivos de Medicina (Manizales), Volumen 15 N° 2, Julio-Diciembre 2015, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Rebollo J.; Reyes N.; Suárez P.
Recibido para publicación: 25-02-2015 - Versión corregida: 10-08-2015 - Aprobado para publicación: 10-11-2015
Resumen
Objetivo: el incremento de la resistencia a antifúngicos en Candida spp. una levadura de carácter oportunista asociada a múltiples infecciones superficiales y sistémicas, plantea la necesidad de buscar diferentes estrategias para hallar nuevas opciones terapéuticas más selectivas y específicas. Una alternativa es el tamizaje basado en el acoplamiento virtual. En el presente trabajo, se analizaron 13418 compuestos con estructuras similares a compuestos reconocidos como inhibidores de la proteína SAP-2, seleccionada como diana antifúngica para el análisis virtual. Materiales y métodos: el estudio se realizó utilizando el programa SYBYL 8, al tiempo que se evaluó la afinidad de estas estructuras con los sitios activos de la enzima seleccionada mediante el programa FlexX integrado en SYBYL 8 y se realizó un consenso comparando los resultados con el programa Autodock Vina. Resultados: los resultados obtenidos mostraron una mayor afinidad por móleculas con estructura similar a los antirretrovirales, inhibidores de proteasas; amprenavir, saquinavir e indinavir. Conclusiones: los resultados obtenidos sugieren que estos lnhibidores de proteasas pueden ser propuestos como modelos para la búsqueda de nuevos antifúngicos que sean más selectivos contra Candida spp.
Palabras clave: candida albicans, inhibidores de proteasas, indinavir.
Rebollo J, Reyes N, Suárez P. Tamizaje Virtual de Compuestos inhibidores de la SAP-2 de Candida albicans. Arch Med (Manizales) 2015; 15(2):260-5.
Virtual screening of inhibitory compounds SEP-2 Candida albicans
Summary
Objetive: reports of Antifungal resistance to Candida spp. are increasing nowadays. Candida spp. is an opportunistic yeast associated to many different mucocutaneous and systemic diseases. Because of this problematic is necessary to search others new selective and specific compounds against this fungi. Virtual docking is a good alternative to study new molecules. Materials and Methods: here we analyse 13418 compounds similar to recognized inhibitors of SAP-2, the enzyme selected as antifungal target. SYBYL 8 was the program used to do the docking virtual besides Autodock Vina to finally select the compounds with best scores. Results: similar compounds to protease inhibitors, amprenavir, indinavir, ritonavir shows best scores in virtual docking. Conclusion: the results suggest that similar compounds to protease inhibitors, amprenavir, indinavir and ritonavir could be proposed as model to research new molecules with antifungal activity against Candida spp.
Keywords: candida albicans, antifiungal, protease inhibitors, indinavir.
Introducción
Las infecciones por Candida spp. no sólo son prevalentes sino que también causan una considerable mortalidad y morbilidad1. Candida albicans y especies no albicans son reconocidas como agentes importantes en infecciones adquiridas en hospitales a nivel mundial, ocupando el cuarto y quinto lugar como la causa más común de septicemia después de Staphylococcus coagulasa-negativo, Staphylococcus aureus y Enterococcus sp. y Pseudomonas aeruginosa2. En Colombia Zuluaga et al reportan el análisis de un total de 337 aislamientos en los que 43,6% correspondían a C. albicans, 23,4% a C. tropicalis, 13,9% a C. parapsilosis, 9,5% a C. glabrata, de los cuáles un 9,8% fueron resistentes a fluconazol y un 3,6% resistentes a voriconazol3. Estas especies muestran una resistencia creciente a los antifúngicos comúnmente utilizados en terapéutica, entre los que se destaca el fluconazol como uno de los fármacos de primera línea para el tratamiento de las candidosis sumado al hecho de que los aislamientos de Candida spp. resistentes a fluconazol son menos susceptibles a itraconazol, ravuconazol, posaconazol y voriconazol 4,5. Del mismo modo, se ha reportado resistencia frente a caspofungina, otro antifúngico de la clase de las equinocandinas, las cuáles actúan a nivel de la síntesis de β- glucano, el cual se reserva especialmente para el tratamiento de infecciones sistémicas 5-7.
Ante esta creciente resistencia a antifúngicos, el Tamizaje Virtual Basado en el Acoplamiento Molecular Computacional es un método que plantea la posibilidad de hallar moléculas dirigidas específicamente contra dianas previamente seleccionadas del microorganismo en estudio de manera que sean específicas y selectivas8. Las proteinasas están involucradas con el dimorfismo, adhesión, cavitación, cambios fenotípicos, formación de biopelículas, invasión y daño al tejido, entre otros componentes; lo que muestra la complejidad del papel de estas enzimas en el proceso patogénico inducido por Candida spp. 9-11. El objetivo del estudio que se reporta en el presente artículo es realizar el análisis de moléculas provenientes de bases de datos mediante acoplamiento con la enzima blanco seleccionada, correspondiente a SAP-2 (Aspartil Proteinasa Secretada-2), a través del acoplamiento computacional de ligando y receptor computacionales.
Materiales y métodos
Se seleccionaron un total de 13418 compuestos obtenidos de la Base de Datos PubChem (https://pubchem.ncbi.nlm.nih.gov/) con estructuras similares a compuestos reconocidos como inhibidores de la enzima blanco. La proteína SAP-2, depositada por Abad-Zapatero y Muchmore12, fue descargada de la Base de Datos de Proteínas (http://www.rcsb.org/pdb/home/home.do) con una resolución de 2.5 Å. La preparación del Surflex Protomol se realizó mediante la remoción de los sulfatos y el agua, la adición de todos los hidrógenos de la proteína y se tomó como base el ligando A70 para la selección del sitio activo. La estructura tridimensional de cada ligando se obtuvo de la base de datos de Pubchem que se encuentra en línea. En este enfoque se realizó la búsqueda de compuestos similares al ligando A70 y Pepstatina A 8,13, que son reconocidos inhibidores de SAP-2 al igual que compuestos similares a inhibidores de proteasas de VIH que han mostrado resultados positivos frente a esta enzima en ensayos in vitro 14,15. Los ligandos se prepararon minimizándolos mediante el minimizador de energía de Sybyl utilizando el campo de fuerza tripos y cargas de Gasteiger-Hückel. El número máximo de interacciones se ajustó a 100 y la minimización se terminó por el método de Powel, cuando se alcanzó el gradiente de energía 0,05 Kcal /mol- Å. Las estructuras de las moléculas se compararon entre sí, mediante análisis con el programa SYBYL 8, al tiempo que se evaluó la afinidad de estas estructuras con los sitios activos de la enzima seleccionada mediante el programa FlexX integrado en SYBYL 8 y se realizó un consenso comparando los resultados con el programa Autodock Vina16, con el fin de seleccionar los compuestos con mayor afinidad por la proteína blanco en ambos análisis para su postulación como posibles candidatos. Los cálculos de acoplamiento de los ligandos en la proteína SAP-2 con el programa AutoDock Vina fueron definidos mediante la creación de un cubo en el centro geométrico del ligando A70 presente en la estructura tridimensional seleccionada (Código PDB: 1ZAP), las dimensiones del cubo fueron 12x16x16 Å (x,y,z). Las coordenadas x, y, z para el centro del cubo fueron 13.047, 26.228 y 0.894 respectivamente. Para cada ligando se escogió la pose con el mayor valor absoluto de afinidad (Kcal/mol).
Resultados
Se evaluaron un total de 13418 compuestos obtenidos de la librería PubChem con estructuras similares a A70 (1407), Pepstatin A (7280), Amprenavir (589), Indinavir (1519), Ritonavir (1623) y Saquinavir (1000). De acuerdo al consenso los compuestos con mejores resultados corresponden a los señalados en la tabla 1.
De estos compuestos el que tiene mayor afinidad por la proteína es el compuesto 18939759 que se encontraba en el grupo del Indinavir. En la figura 1 se muestra los sitios de interacción del ligando con la proteína correspondientes a los residuos; Asn 301, Asp 86, Thr 222, Thr 221 (con dos interacciones), Tir 225 y Asn 131. En la figura 2, se muestran los sitios de interacción para el ligando clásico de la SAP-2, A70 que corresponden a los residuos Asn 301, Thr 221, Asp 218 y Asp 86, lo que muestra un menor número de interacciones al compararlo con el compuesto 18939759 que mostró una mayor afinidad por la enzima. También se realizaron otros análisis utilizando compuestos quinoidales y AINES, los cuáles mostraron scores muy bajos o negativos. Sin embargo en el análisis realizado para algunas estatinas, de acuerdo al valor obtenido en los scores, podría sugerir una posible interacción de algunas de estas moléculas con la candidopepsina-2.
Tabla 1. Compuestos similares a A70, Amprenavir, Indinavir y Saquinavir.
|
Inhibidor Base |
CID |
Nombre IUPAC |
Kcal/mol (A.V) |
|
A70 |
18393039 |
N-[(2S,3R)-4-[(3S,4aS)-3-[(2-methylpropan-2-yl)oxycarbamoyl]- |
-8.8
|
|
18393040 |
[(2S,3R)-4-[(3S,4aS)-3-[(2-methylpropan-2-yl)oxycarbamoyl]- |
-8.9 |
|
|
Amprenavir |
3008202 |
[(2S,3R,3aS,7aR)-2-methyl-3,3a,4,5,6,7a-hexahydro-2H- |
-8.9 |
|
Indinavir |
18939759 |
pyridin-3-ylmethylN-[1-[[4-hydroxy-1,6-diphenyl-5- |
-9.3 |
|
Saquinavir |
18648267 |
(2S)-N-[(2R)-2-hydroxy-4-phenyl-1-[[(2S)-pyrrolidine- |
-8.7 |
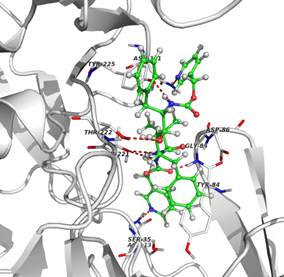
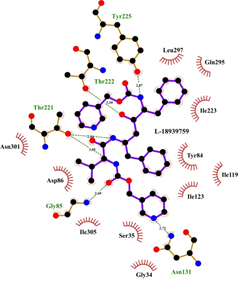
Figura 1. Complejo SAP-2 – Ligando 18939759, mostrando los sitios de interacción para la mejor pose. Vista tridimensional (Izquierda) y bidimensional (Derecha). Gráficos generados mediante Pymol (The PyMOL Molecular Graphics System, Version 1.7.4 Schrödinger, LLC - open-source), y Ligplot (Wallace A C, Laskowski R A, Thornton J M (1996). LIGPLOT: a program to generate schematic diagrams of protein-ligand interactions. Protein Eng., 8, 127-134.
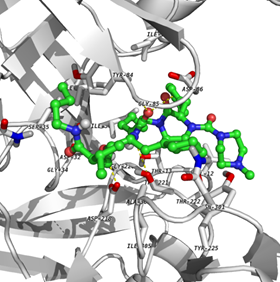
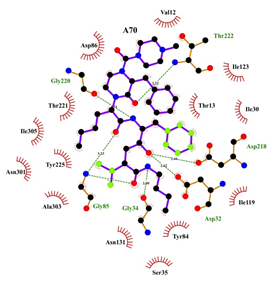
Figura 2. Complejo SAP-2 – A70, mostrando los sitios de interacción para la mejor pose. Vista tridimensional (Izquierda) y bidimensional (Derecha). Gráficos generados mediante Pymol (The PyMOL Molecular Graphics System, Version 1.7.4 Schrödinger, LLC - open-source), y Ligplot (Wallace A C, Laskowski R A, Thornton J M (1996). LIGPLOT: a program to generate schematic diagrams of protein-ligand interactions. Protein Eng., 8, 127-134.
Discusión
La búsqueda de nuevos antifúngicos más selectivos y con menos efectos adversos es un desafío constante. En estudios previos realizados in vitro con el ligando A70 y la Pepstatina A se muestran como potentes inhibidores de la SAP-2 pero no son viables desde el punto de vista farmacocinético como antifúngicos17. Los resultados del docking muestran que la búsqueda de nuevos ligandos puede orientarse hacia estructuras similares a estos compuestos. En el caso de los antirretrovirales In vitro se ha mostrado que el amprenavir es un potente inhibidor de la proteína blanco reduciendo la actividad proteolítica de C. albicans en un 92% 14, mientras que otros como ritonavir, saquinavir e indinavir inhibirían la actividad enzimática en un 45% a 65% pero dadas las características farmacológicas y su relativa toxicidad aún no se considera el uso los mismos como antifúngicos15. La mayor afinidad mostrada por los compuestos similares a amprenavir, saquinavir e indinavir sugieren que estos lnhibidores de proteasas pueden ser utilizados para la búsqueda de inhibidores de la SAP-2 que sean más selectivos.
La búsqueda de nuevos antifúngicos más selectivos y con menos efectos adversos es un desafío constante, por el incremento de las infecciones fúngicas en pacientes con algún grado de inmunosupresión o enfermedad de base. El uso de herramientas virtuales puede contribuir al diseño de nuevos fármacos, al tiempo que se plantean nuevas dianas antifúngicas. Los resultados del presente docking virtual revelan, compuestos similares a inhibidores de proteasas antirretrovirales, con una mayor afinidad por la SAP-2, por ello estos resultados podrían conducirnos a nuevos fármacos con actividad antifúngica, que sean más específicos y por tanto menos tóxicos, pero al mismo tiempo se corrobora que la aspartil proteasa (SAP 2) si puede ser un blanco para el diseño de nuevos fármacos particularmente por las diferentes funciones en que están implicada esta enzima.
Conflictos de interés: Los autores declaran no tener ningún conflicto de interés en relación al tema tratado en el presente artículo.
Fuentes de financiación: Los autores expresan sus agradecimientos a la Universidad de Cartagena por la financiación del presente trabajo, mediante resolución 4791 del 10 de diciembre de 2010.
Literatura citada
1. Klepser ME. Candida resistance and its clinical relevance. Pharmacotherapy 2006; 26:68S-75S.
2. Eloy O, Blanc V, Pina P, Gaudart A, Bressolle ML, Plainvert C, et al. Epidemiology of candidemia: results of a one month French hospitals-based surveillance study in 2004. Pathol Biol (Paris) 2006; 54:523-30.
3. Zuluaga RA, Agudelo RC, De Bedout C, Hurtado PH, Arango AM, Restrepo MA, et al. Sensibilidad a fluconazol y voriconazol de especies de Candida aisladas de pacientes provenientes de unidades de cuidados intensivos en Medellin, Colombia (2001–2007). Rev Iberoam Micol 2010; 27(3):125-9
4. Rodriguez AZ, Gomez CB, Restrepo CA, Parra HH, Arteaga MA, Moreno AR, et al. Susceptibility to fluconazole and voriconazole of Candida species isolated from intensive care units patients in Medellin, Colombia (2001-2007). Rev Iberoam Micol 2011; 27(3):125-9
5. Pfaller MA, Moet GJ, Messer SA, Jones RN, Castanheira M. Geographic variations in species distribution and echinocandin and azole antifungal resistance rates among Candida bloodstream infection isolates: report from the SENTRY Antimicrobial Surveillance Program (2008 to 2009). J Clin Microbiol 2011; 49(1):396-9.
6. Pfaller MA, Castanheira M, Messer SA, Moet GJ, Jones RN. Variation in Candida spp. distribution and antifungal resistance rates among bloodstream infection isolates by patient age: report from the SENTRY Antimicrobial Surveillance Program (2008-2009). Diagn Microbiol Infect Dis 2010; 68(3):278-83.
7. Seneviratne CJ, Wong SS, Yuen KY, Meurman JH, Parnanen P, Vaara M, et al. Antifungal susceptibility and virulence attributes of bloodstream isolates of Candida from Hong Kong and Finland. Mycopathologia 2011; 172(5):389-95.
8. Pranav Kumar SK, Kulkarni VM. Insights into the selective inhibition of Candida albicans secreted aspartyl protease: a docking analysis study. Bioorg Med Chem 2002; 10(4):1153-70.
9. Gauwerky KC, Borelli C, Korting HC. Targeting virulence: a new paradigm for antifungals. Drug Discov Today 2009; 14(3-4):214-22.
10. Hube B, Naglik J. Candida albicans proteinases: resolving the mystery of a gene family. Microbiology 2001; 147(8):1997-2005.
11. Pichova I, Pavlickova L, Dostal J, Dolejsi E, Hruskova-Heidingsfeldova O, Weber J, et al. Secreted aspartic proteases of Candida albicans, Candida tropicalis, Candida parapsilosis and Candida lusitaniae. Inhibition with peptidomimetic inhibitors. Eur J Biochem 2001; 268(9):2669-77.
12. Abad-Zapatero C, Goldman R, Muchmore SW, Hutchins C, Stewart K, Navaza J. Structure of a secreted aspartic protease from C. albicans complexed with a potent inhibitor: implications for the design of antifungal agents. Protein Sci 1996; 5(4):640-52.
13. Trabocchi A, Mannino C, Machetti F, De Bernardis F, Arancia S, Cauda R. Identification of inhibitors of drug-resistant Candida albicans strains from a library of bicyclic peptidomimetic compounds. J Med Chem 2010; 53(6):2502-9.
14. Braga-Silva LA, et al. Multiple effects of amprenavir against Candida albicans. FEMS Yeast Res 2009; 10(2):221-4.
15. Dos Santos A. HIV aspartyl protease inhibitors as promising compounds against Candida albicans. World J Biol Chem 2010; 1(2):21-30.
16. Trott O, Olson AJ. AutoDock Vina: improving the speed and accuracy of docking with a new scoring function, efficient optimization, and multithreading. J Comput Chem 31(2):455-61.
17. Cadicamo CD, Mortier J, Wolber G, Hell M, Heinrich IE, Michel D et al. Design, synthesis, inhibition studies, and molecular modeling of pepstatin analogues addressing different secreted aspartic proteinases of Candida albicans. Biochem Pharmacol 2012; 85(7):881-7.
![]()