Daniel Andrés Nieva-Posso1, María del Pilar Crespo-Ortiz2
Recibido para publicación: 21-12-2024. Versión corregida: 16-05-2025. Aprobado para publicación: 03-09-2025.
Modelo de citación:
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en ges- tantes: aspectos relevantes y revisión narrativa de la literatura. Arch Med (Manizales). 2025;25(2). https://doi.org/10.30554/archmed.25.2.5305.2025
Introducción: El Streptococcus agalactiae o Streptococcus del grupo B es un pa- tógeno relevante en la salud maternofetal y mundialmente es uno de los agentes etiológicos de sepsis neonatal temprana de alta letalidad y sepsis neonatal tardía causante de secuelas neurológicas permanentes y discapacidad infantil. La coloni- zación materna es la principal fuente de transmisión de la sepsis temprana, la cual puede prevenirse mediante la profilaxis materna intraparto. El tamizaje prenatal mediante cultivo vaginorectal constituye la principal herramienta para la detección de las gestantes colonizadas y en riesgo. Objetivo: Esta revisión pretende brindar información actualizada sobre la carga de la infección por Streptococcus agalactiae y sus efectos en gestantes y neonatos, enfocándose en el proceso óptimo de detección e identificación de la bacteria, así como las alternativas de diagnóstico molecular. Lo anterior con el fin de mejorar el limitado control de la infección debido a la falta de comprensión de estos aspectos. Metodología: Para la revisión del tema se realizó una búsqueda de la literatura en 4 bases de datos, incluyendo estudios de la última década (hasta 2023). Se seleccionaron 82 artículos que cumplieron con los criterios para la revisión narrativa, la cual se realizó en concordancia con la guía SANRA. Resultados: Se describen aspectos microbiológicos, epidemiológicos y, particular- mente, se discuten las limitaciones del cultivo vaginorectal prenatal y los retos para
![]()
Bacteriólogo y laboratorista clínico. Grupo de Investigación UROGIV. Escuela de Medicina. Facultad de Salud. Universidad del Valle. Cali, Colombia. ORCID: https://orcid.org/0000-0003-1193-0732.
CvlaC: https://scienti.minciencias.gov.co/cvlac/visualizador/generarCurriculoCv.do?cod_rh=0001771333. Correo: daniel.nieva@correounivalle.edu.co.
Bacterióloga y laboratorista clínica, MSc, PhD, docente. Grupo de Investigación en Microbiología y Enfermedades Infecciosas. Departamento de Microbiología. Facultad de Salud. Universidad del Valle. Cali, Colombia.
ORCID: https://orcid.org/0000-0003-2160-5167.
CvLaC: https://scienti.minciencias.gov.co/cvlac/visualizador/generarCurriculoCv.do?cod_rh=0000156949. Correo: maria.crespo.ortiz@correounivalle.edu.co. Autor para la correspondencia.
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
la detección e identificación de la bacteria, considerando la utilización de pruebas moleculares de punta. Conclusiones: El rendimiento del cultivo o estándar de oro es variable, lo cual disminuye su sensibilidad y poder diagnóstico. En esta revisión se hace evidente la alta sensibilidad y especificidad de las pruebas moleculares, lo que hace imperativo incluir estas pruebas complementarias en la detección antenatal de la bacteria, permitiendo la aplicación efectiva de la terapia intraparto y la prevención de la infección neonatal.
Palabras clave: Streptococcus agalactiae; técnicas de diagnóstico molecular; sepsis neonatal; mortalidad perinatal; infecciones estreptocócicas.
Introduction: Streptococcus agalactiae or Group B Streptococcus is a relevant pathogen in perinatal health and is a leading cause of early onset infections with high lethality and late onset infections causing long term neurological sequels and substantial disabilities. Maternal colonization is the main risk factor for the early onset disease which can be prevented using intrapartum prophylaxis. The culture-based prenatal screening is the main diagnosis tool for detection of colonized pregnant women at risk. Aim: This review provides an update on the Streptococcus agalactiae disease and its effects focusing on recommendations to improve bacterial detection and identification with particular emphasis on the cutting-edge molecular diagnostic tools. This also aims to improve the limited infection control measures because of the poor understanding of these aspects. Methodology: To identify relevant lite- rature, a search on four databases was performed spanning studies over the last decade (up to 2023). Eighty-two papers were selected for this narrative review in accordance to SANRA guidelines. Results: Relevant aspects of the microbiology and epidemiology are discussed and particularly the limitations of the culture-based prenatal screening and the challenges associated with bacterial detection and iden- tification using novel molecular tests. Conclusions: Prenatal screening based on vaginal-rectal culture has limitations and variability resulting in low sensitivity and poor outcomes. Molecular diagnosis has shown higher sensitivity and specificity over the culture and should be included in the routine testing to improve detection of maternal colonization allowing the effective intrapartum prophylaxis and prevention of neonatal infections.
Keywords: Streptococcus agalactiae; molecular diagnostic techniques; neonatal sepsis; perinatal mortality; streptococcal infections.
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Introdução: Streptococcus agalactiae ou Streptococcus do grupo B é um patógeno relevante na saúde materno-fetal, pois mundialmente é um dos agentes etiológicos da sepse neonatal precoce de alta letalidade e da sepse neonatal tardia que causa sequelas e incapacidades neurológicas permanentes. A colonização materna é a prin- cipal fonte de transmissão da sepse precoce, que pode ser prevenida pela profilaxia intraparto. A triagem pré-natal por meio da cultura vagino-retal é a principal ferramenta para detecção de gestantes de risco. Objetivos: Esta revisão visa fornecer informações atualizadas sobre a infecção por Streptococcus agalactiae e seus efeitos, com foco no processo ideal de detecção e identificação da bactéria, bem como alternativas de diagnóstico molecular. O acima exposto com o objetivo de melhorar o limitado controle de infecção devido à falta de compreensão desses aspectos. Metodologia: Para re- visar o tema, foi realizada uma pesquisa bibliográfica em 4 bases de dados incluindo estudos da última década (até 2023). Foram selecionados 82 artigos que atenderam aos critérios da revisão narrativa, de acordo com a diretriz SANRA. Resultados: São descritos aspectos microbiológicos e epidemiológicos e, particularmente, são discu- tidas as limitações da cultura vagino-retal pré-natal e os desafios para a detecção e identificação da bactéria considerando o uso de testes moleculares de última geração. Conclusões: O desempenho da cultura ou padrão ouro é variável, o que diminui sua sensibilidade e poder diagnóstico. Nesta revisão fica evidente a alta sensibilidade e especificidade dos testes moleculares, o que torna imperativa a inclusão destes testes complementares na detecção pré-natal da bactéria, permitindo a aplicação eficaz da terapia intraparto e prevenção de infecções neonatais.
Palavras-chave: Streptococcus agalactiae; técnicas de diagnóstico molecular; sepse; neonatal; mortalidade perinatal; infecções estreptocócicas
temprana (0 - 6 días) de alta letalidad y sepsis neonatal tardía (>7 días – 89 días) o muy tardía
El Streptococcus agalactiae, o Streptococ- (> 3 meses) con secuelas permanentes en el cus del grupo B (SGB), es un colonizante individuo, tales como retraso mental, cognitivo habitual del tracto gastrointestinal y tracto ge- y motor, además de alteraciones respiratorias nitourinario, particularmente en mujeres ges- y complicaciones auditivas y visuales [2]. Las tantes [1]. Sin embargo, en ciertas condiciones madres colonizadas transmiten la infección causa infecciones invasivas en recién nacidos, al neonato y se estima que a nivel mundial inmunosuprimidos y mayores de 60 años [1]. alrededor del 20 % de las gestantes están Desde hace varias décadas, el SGB es uno colonizadas y 40 al 70 % transmitirán la bac- de los principales agentes etiológicos de sep- teria al recién nacido [2]. Aproximadamente el ticemia, meningitis y neumonía en neonatos, 1 al 2 % de los neonatos colonizados pueden en quienes puede causar sepsis neonatal desarrollar infección invasiva [3], no obstante,
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
la frecuencia puede variar dependiendo de la región geográfica y la etnia, como es el caso de África donde las prevalencias son más altas [4]. La mortalidad por sepsis temprana oscila entre el 5 % al 27 % dependiendo del grado de desarrollo de la región [5], con un riesgo de infección y muerte al menos tres veces mayor en los prematuros [3].
A partir de 1990, la implementación de la profilaxis antibiótica intraparto (PAI) en las ges- tantes colonizadas o consideradas en riesgo, redujo significativamente la sepsis neonatal temprana de 1.8 x 1000 nacidos vivos (1990) a 0.23 x 1000 nacidos vivos (2015), por lo que la detección de gestantes colonizadas ha sido una estrategia utilizada para disminuir el riesgo de infección y muerte neonatal [6]. El tamizaje para detectar el SGB se hace mediante el cul- tivo de hisopado vaginorectal en la gestante con el fin de predecir la colonización intraparto y administrar la PAI dentro de las 4 horas del comienzo del trabajo de parto y durante el mismo [6]. Dado que la presencia y densidad de la colonización es variable en las mujeres, el Colegio Americano de Ginecólogos y Obs- tetras ha establecido que el tamizaje debe realizarse entre las 36 0/7 a 37 6/7 semanas de gestación [6], lo anterior buscando predecir mejor la colonización en el momento del parto. Esta medida ha reducido la morbimortalidad asociada a la infección por SGB en países de alto ingreso, pero ha tenido poco impacto en países de ingreso medio y bajo [7] y solo se encuentra protocolizada en 65 de 90 países con datos reportados [8]. Para el año 2021, la Organización Mundial de la Salud (OMS) estimó que se presentaron alrededor de 409.000 casos de infección por SGB en mujeres gestantes y recién nacidos, ocurriendo la mayoría de los casos en países de medio y bajo ingreso [9]. A pesar de la utilidad del tamizaje por cultivo, existe entre un 6 % al 15 % de gestantes que no son detectadas anteparto y que son positivas intraparto [10,11]. Otra limitación del tamizaje es que solo es útil en el control de la infección neonatal temprana porque no modifica la in-
cidencia de la infección neonatal tardía, los mortinatos o el parto pretérmino. El uso de la PAI aumenta la exposición de la bacteria a los antibióticos generando resistencia a eritromici- na y clindamicina [12].
En América Latina, son pocos los países que recomiendan por protocolo el tamizaje para de- tección del SGB. En Uruguay, Bolivia, Paraguay y Nicaragua, se ha aumentado la cobertura de tamizaje sobre todo en zonas rurales, llegando a ser cercana al 50 %, pero en el resto de los países es hasta del 15 % [13]. En Colombia, el tamizaje de rutina se protocolizó desde el año 2013 [14] con una adherencia del 68 % según un estudio realizado en Bogotá [15].
A pesar de que el cultivo sigue siendo un re- ferente para detectar la colonización materna, la sensibilidad de la prueba varía, puesto que diversos factores pueden alterar su eficacia, entre ellos: el uso o no de caldos de enrique- cimiento, el medio de cultivo seleccionado y la cantidad de colonias viables en la muestra. Se calcula que la sensibilidad del cultivo es del 54 % al 90 % [16] y el tiempo de espera para la obtención de resultados puede ser de 18 a 72 horas incluyendo el tiempo para la identificación y prueba de susceptibilidad del microorganismo [17]. En países de medio y bajo ingreso el porcentaje de recuperación del SGB en las muestras de hisopados va- ginorectales es muy bajo, lo que plantea la necesidad de revisar los protocolos de rutina y, adicionalmente, incorporar técnicas de diag- nóstico más sensibles [13]. Aún en países de alto ingreso la información sobre el manejo y toma de muestras no es consistente y se ha encontrado que hasta un 85 % de los labo- ratorios en los Estados Unidos no suministra información al respecto y que hasta el 34 % lo hace de forma incorrecta. No obstante, en la actualidad se dispone de pruebas moleculares basadas en la detección de bajas concentra- ciones de ADN de la bacteria, las cuales son sensibles, específicas y ofrecen resultados en menor tiempo. La reacción en cadena de
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
la polimerasa en tiempo real (qPCR) múlti- ple tiene una sensibilidad del 62 % - 100 %, comparada con el cultivo y ofrece resultados en menos de 2 horas [17], mientras que otras pruebas comerciales de qPCR reportan una sensibilidad de al menos 95 % [18]. También se dispone de sistemas de identificación como la desorción/ionización láser asistida por ma- triz (MALDI-TOF) que permite discriminar los subtipos capsulares con una sensibilidad del 99 % [19]. Estudios recientes han revelado una carga mayor de la enfermedad comparada con estimados previos, lo que ha generado una alerta de la OMS para optimizar el control de la infección mediante el mejoramiento del cui- dado materno y neonatal. La implementación de una vacuna en las gestantes es la estra- tegia más costo-efectiva para salvar muchas vidas y mejorar la salud materno-infantil, sin embargo, ésta aún se encuentra en desarrollo, por lo que la alternativa actual es optimizar la detección de las colonizaciones y el enfoque de la profilaxis y/o terapias adecuadas. En países en desarrollo, la brecha en cuanto al conocimiento de la epidemiologia, diagnóstico, manejo y efectos de la infección por SGB es muy amplia y la utilización rutinaria de pruebas moleculares y la vigilancia epidemiológica son ausentes. En concordancia con lo anterior, esta revisión narrativa tiene como objetivo sintetizar información reciente sobre la epide- miologia y microbiología del SGB enfocándose en la detección óptima de la bacteria mediante pruebas sensibles, con el fin de mejorar el li- mitado control de la infección debido a la falta de comprensión de estos aspectos.
La revisión de literatura se preparó utili- zando como guía la escala SANRA [20]. La búsqueda se realizó en cuatro bases de datos bibliográficas: PubMed, Scielo, ScienceDirect y Google Scholar utilizando los siguientes descriptores: “Streptococcus agalactiae/Group B Streptococcus” and “NAATs (Nucleic Acid Amplification Techniques)”, “pregnant woman
screening”, “diagnosis/detection”, “prevalen- ce”. Se incluyeron artículos en inglés, español y portugués de los últimos 10 años (hasta el año 2023), con particular énfasis en artícu- los originales, revisiones sistemáticas con o sin metaanálisis y estudios enfocados en el diagnóstico en muestras clínicas humanas. La búsqueda generó un total de 350 artículos basados en el título y resumen. Ambos autores examinaron los artículos y, después de elimi- nar los duplicados y/o aquellos con un foco diagnóstico muy similar, se seleccionaron 82 artículos que cumplieron con los criterios. Los artículos se categorizaron considerando los aspectos relevantes en revisión: epidemiolo- gia, espectro de la infección, microbiología y diagnóstico. A continuación, se describen los hallazgos de la revisión.
La colonización por SGB en gestantes varía de acuerdo con factores ambientales como la región y etnia o factores intrínsecos como la edad, nivel hormonal, balance inmune, además de su densidad y persistencia [21]. Un estudio realizado durante 5 años y en el que participaron 6.641.960 mujeres gestantes incluyendo 25.6 % de población migrante, encontró que la colonización por SGB fue del
5.19 %, la cual fue variable y dependiente de la región de origen así: Europa occidental
2.2 %, América del Norte 2.1 %, Australia 3.7%, España 4.6 %, Latinoamérica 4.5 -
7.7 %, Europa del Este 5.3 %, Asia 6.7 %, Oriente Medio 7.9 %, India 17.2 %, África del Norte 17.8 % y África Subsahariana 22.7 %. La frecuencia alta de colonización por SGB se asoció con un bajo producto interno bruto per cápita y altas temperaturas en el lugar de origen de las gestantes [21]. En una revisión más reciente se describe el panorama a nivel global de la colonización e infección por SGB y sus principales efectos [2]. (Tabla 1).
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Tabla 1. Distribución mundial de la colonización e infección por SGB y sus efectos.
Regiones | Colonización materna (millones de gestantes) (%) | Infección neonatal temprana (# casos) | Infección neonatal tardía (# casos) | Neuro secuelas (# casos) | % de pretérmino asociado con SGB | Mortinatos | Muertes por infección |
Mundial a | 19.7 (14.1) | 231.800 | 162.200 | 37.100 | 3.5 | 46.200 | 91.900 |
África Sub sahariana | 6.1 (16.1) | 90.800 | 78.100 | 15.000 | 4 | 20.300 | 50.600 |
Asia Central /Sur | 4.4 (11.5) | 47.300 | 23.600 | 6.600 | 2.6 | 14.700 | 16.700 |
Este y sureste de Asia | 3.1 (10.4) | 45.700 | 22.600 | 6.900 | 2.7 | 4.600 | 9.700 |
Europa y Norte América | 2.3 (19.7) | 4.300 | 2.500 | 400 | 5.1 | 700 | 400 |
Norte África/ Oeste Asia | 1.9 (19.7) | 29.000 | 20.800 | 4.900 | 4.8 | 2300 | 9.600 |
Latino América y el Caribe | 1.5 (15.1) | 12.800 | 8.400 | 2.100 | 3.9 | 1.800 | 3.600 |
Oceanía | 0.12 (18.6) | 700 | 400 | 100 | 4.7 | 100 | 300 |
a Los datos corresponden a la mediana. Fuente: adaptada y modificada a partir de Gonçalves et al. [2].
En países latinoamericanos las frecuencias de colonización son muy variables: Brasil
28.2 % [7], Uruguay 19.3 % [13], Argentina
9.1 % [22], México 1.47 % [23] y Nicaragua
0.14 % [24]. En la última década, en Colombia, varios estudios a nivel regional han observa- do frecuencias de colonización materna que oscilan entre 17 y 52 % [25,29] con alta varia- bilidad dependiendo de la población, el tiempo del tamizaje (tamizaje rutinario o en gestante pretérmino), el área geográfica, el nivel de atención y los métodos de detección (cultivo o prueba molecular) así: Santa Marta 52 % [29], Cartagena 37.6 % [27], Bucaramanga 20.7 %
[28] y Medellín 17.6 % - 36 % [25,26].
La PAI solo permite el control de la sepsis temprana, pero no tiene efecto en la epide- miologia de la enfermedad tardía por SGB, por lo que la prevención de todas las infecciones solo sería posible mediante la generación de anticuerpos protectores con la implementación de la vacuna. Otra desventaja de la PAI es que puede promover la aparición de resistencia antibiótica e inducir cambios en el microbioma intestinal, aumentando el riesgo de alergias, asma y obesidad en madres e infantes [30]. Como estrategia para disminuir estos efectos,
la OMS ha planteado el desarrollo de la vacuna como una prioridad, así como su integración en los esquemas de vacunación, con los siguientes supuestos: al menos una vacuna aprobada para el 2026 y al menos 10 países con la vacuna implementada para 2030 [9].
Aunque las manifestaciones más severas de la infección se han observado en los neo- natos y gestantes, existen otras poblaciones en riesgo, como los mayores de 60 años y los pacientes inmunosuprimidos [1]. En mujeres embarazadas la infección en la placenta desen- cadena una respuesta inflamatoria, que puede causar corioamnionitis (13 %) [31], retraso en el crecimiento intrauterino (17 %), parálisis cerebral a nivel fetal (4 %) [32], endometritis posparto (9 %) [33], sepsis materna, abortos espontáneos y muerte fetal (10 %) [34]. En los mayores de 60 años, la bacteria causa celulitis, abscesos, infecciones plantares o úlceras de decúbito y manifestaciones sistémicas como bacteriemias y septicemias [1]. En adultos la manifestación clínica más común es la bacterie- mia en un 18 % de los casos, seguido de artritis, celulitis, meningitis, osteomielitis y endocarditis;
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
principalmente en pacientes con condiciones de base, tales como diabetes, alcoholismo y enfermedad renal crónica [35,36]. En pacientes inmunosuprimidos, la bacteriemia es la mayor causa de morbimortalidad. También se han re- portado casos de endocarditis, infecciones en piel y tejidos blandos e invasiones al sistema nervioso central en porcentajes menores del 2 % [35]. En Colombia se ha reportado una inci- dencia de 0.75 x 1000 en adultos inmunosupri- midos, principalmente afectados con bacterie- mias e infecciones de piel y tejidos blandos [36].
El SGB es un coco grampositivo beta he- molítico que tiene el antígeno polisacárido es- pecífico de la pared celular del grupo B según la clasificación de Lancefield [37]. La bacteria tiene 10 serotipos capsulares diferentes (Ia, Ib, II a IX), los cuales pueden ser identificados mediante ensayos moleculares o pruebas de aglutinación en látex [37]. Se ha demostrado que los anticuerpos contra la cápsula confie- ren protección contra la enfermedad, por lo que la tipificación capsular del SGB genera información importante para conocer el efecto de la implementación de la vacuna, la cual se encuentra en fases avanzadas de desarrollo [38]. La distribución de los diferentes serotipos en todo el mundo y por regiones geográficas se presenta en la Tabla 2 [39].
Aunque no se ha establecido una asocia- ción determinante entre los serotipos y el tipo de infección o sensibilidad antibiótica, algunos se encuentran más frecuentemente como colonizantes (V) o causando infeccio- nes invasivas (Ia, II, III). Los tipos Ia, II, III y V son los más prevalentes en América, Europa y África, mientras que en Asia se reportan, además, el VI, VII y VIII. El tipo capsular IV se ha encontrado en incremento y se considera emergente.
El estudio molecular de la estructura pobla- cional de la bacteria utilizando tipificación mul- tilocus de secuencias (MLST) y secuenciación genómica, ha identificado diversos linajes o subtipos (ST) y particularmente el linaje ST17, denominado el clon o tipo hipervirulento, se ha asociado con la sepsis neonatal tardía y meningitis, causando secuelas severas en el infante [39].
El clon hipervirulento (ST17) se ha reportado a nivel mundial y se asocia con el tipo capsular III cuya prevalencia oscila entre el 11 al 25 % [40]. El ST17 posee una adhesina específica (HvgA) que le confiere la capacidad de cruzar la barrera hematoencefálica y también otros fac- tores de virulencia como una proteína mutada rica en serina (Srr2), el aparato de secreción SecA2/Y2 y una variante de la proteína Rib (de la familia alpha-like) [41] que le confieren potencial patogénico diferencial.
Tabla 2. Prevalencia mundial de los tipos capsulares del SGB.
Regiones | Ia/Ib (%) | II (%) | III (%) | IV (%) | V (%) | Tipos capsulares VI al X y otros (%) |
Mundial | 32 | 11 | 2 | 1 | 18 | 2 |
Suramérica | 50 | 13 | 16 | 0 | 10 | 1 |
Norte América | 34 | 15 | 22 | 2 | 26 | 0 |
Centroamérica | 70 | 20 | 10 | 0 | 0 | 0 |
Áfricaa | 25- 39 | 6-24 | 16-36 | 0-2 | 11-40 | 0 |
Asiaa | 18-25 | 7-14 | 12-29 | 0-4 | 16-20 | 3-20 |
Europaa | 27-30 | 11-14 | 28-34 | 3-4 | 8-17 | 0-2 |
Australia y Nueva Zelanda | 48 | 7 | 35 | 1 | 16 | 2 |
a Rangos de las regiones del continente. Fuente: Tabla adaptada y modificada a partir de Russell et al. [39].
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
La muestra recomendada para el tamizaje prenatal es un hisopado vaginorectal tomado entre las 36 0/7 y 37 6/7 semanas de gestación, considerando que el valor predictivo positivo del cultivo es mayor cuando se toma en el intervalo de las 5 semanas antes del parto [6]. Esta re- ciente modificación en las recomendaciones del Colegio Americano de Ginecoobstetricia [6] se realizó para mejorar la predicción de la coloni- zación intraparto, dado que solo 60 % de las co- lonizaciones anteparto persisten en el momento del parto [42] y que más de la mitad (53 % - > 60
%) de los neonatos con sepsis temprana nacen de madres con tamizaje negativo [43]. Para la toma de la muestra se debe usar un hisopo de punta aguda (flocado) que permite una mayor recuperación de la bacteria y el cual debe in-
troducirse cerca al introito y luego en el esfínter anal [6]. Los hisopos se deben transportar en medio Amies o Eswab, dentro de las 24 horas a la toma de la muestra, de otra forma deben ser refrigerados a 4 °C hasta su procesamiento, se ha observado que la viabilidad de la bacteria se conserva por 2 días a 20 - 25 °C o hasta 4 días entre 2 - 8 °C [44]. Los hisopos deben ser incubados 18 - 24 horas en un medio de enriquecimiento selectivo (pre-enriquecimiento) o caldo Todd Hewitt (TH) suplementado con gentamicina (8 µg/mL) o colistina (10 µg/mL) y ácido nalidíxico (15 µg/mL) (denominados caldos Trans-Vag o Lim, respectivamente) antes de hacer la inoculación en agar sangre de cordero (AS) o medios cromogénicos para SGB [6]. Colonias blancas grisáceas con beta hemólisis y catalasa negativas en el AS deben ser identificadas de acuerdo con los sistemas disponibles en el laboratorio (Figura 1).
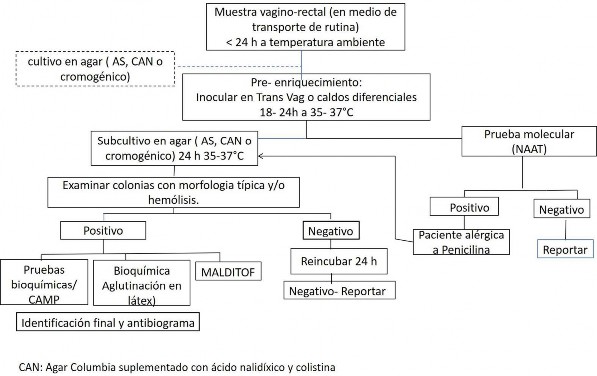
Figura 1. Detección e identificación de aislados de SGB en el laboratorio. La línea punteada indica que se sugiere un cultivo directo, si las colonias son compatibles se debe proceder a la identificación y antibiograma (pacientes alérgicas o infecciones invasivas). Un panel de pruebas bioquímicas debe acompañar a la prueba de CAMP o la aglutinación en látex. Fuente: adaptada y modificada a partir de Filkins et al. [6].
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
El enriquecimiento se recomienda dado que aumenta hasta dos veces la posibilidad de recuperar la bacteria, no realizarlo puede generar hasta un 50 % de falsos negativos, una reducción en el tiempo del enriquecimien- to también afecta la detección de la bacteria [42,45]. Con el fin de optimizar la detección se sugiere también realizar un cultivo directo de la muestra en caso de que haya proliferación de la microbiota durante el enriquecimiento, dado que se ha observado inhibición del SGB por so- brecrecimiento de Enterococcus (Figura 1) [6].
El cultivo tiene varias limitaciones, una de ellas es que se fundamenta en la detección de colonias con beta hemólisis y/o prueba de CAMP positiva (factor Christie, Atkins, and Munch-Peterson presente), no obstante 5 % de las cepas de SGB no son beta hemolíticas y pueden producir enfermedad invasiva [6,46]. Además, el cultivo requiere 24 horas adiciona- les al enriquecimiento y al menos otras 24 horas para realizar la identificación y susceptibilidad del microorganismo.
Las técnicas de amplificación de ácidos nucleicos (NAATs, por sus siglas en inglés) tienen una sensibilidad variable dependiendo de la prueba, pero usualmente es > 96 % com- parada con el cultivo (54 - 90 %) y los tiempos de reporte son más cortos. Sin embargo, también requiere el enriquecimiento selectivo
[47] y, en algunos casos, aún es necesario el cultivo para determinar la susceptibilidad de la bacteria a clindamicina y eritromicina debido a que, en gestantes alérgicas a la penicilina, la clindamicina es una opción recomendada para la profilaxis.
A pesar de la guía estándar para la toma, procesamiento e identificación del SGB, existe una pobre adherencia a estas medidas inclu- so en países de alto ingreso, lo que afecta su diagnóstico [48]. La detección de la bacteria es la base para implementar la PAI, detener la transmisión, evitar las terapias no indicadas y prevenir el desarrollo de la resistencia. La mayoría de los neonatos infectados vienen de
madres con tamizaje negativo para SGB, lo que sugiere una proporción significativa de falsos negativos por cultivo y/o la colonización mater- na posterior al tiempo de tamizaje y presente en el momento del parto [49]. En gestantes con parto prematuro o sin tamizaje previo, la rea- lización de una NAAT rápida ha representado muchos beneficios y, de hecho, se utiliza en países de alto ingreso, no obstante, aún no se recomienda como prueba de tamizaje dentro de los protocolos debido a que su valor predictivo negativo es bajo [6].
Dadas las limitaciones del cultivo (estándar de oro), la investigación se centra en el diseño y utilización de nuevos métodos diagnósticos y de tipificación. De los artículos selecciona- dos en la revisión, se encontraron 44 sobre el diagnóstico: 2 de revisión y 42 enfocados en técnicas diagnósticas independientes al cultivo: 34 (80 %) sobre NAATs, incluyendo 24 sobre aplicaciones de la reacción en cadena de la polimerasa (PCR) convencional y qPCR, uno en PCR digital, 7 en amplificación isotérmica me- diada por bucle (LAMP) y 2 sobre amplificación mediada por recombinasa y polimerasa (RPA). De los 8 artículos restantes, uno se enfocó en la detección por CRISPR Cas, 2 en secuenciación para tipificación capsular, 4 en identificación por perfil de proteínas (MALDI-TOF) y uno en biosensores. (Tabla 3).
El PCR ha sido la técnica molecular más empleada como alternativa al cultivo, los ge- nes blanco utilizados codifican por proteínas conservadas del SGB, tales como el gen cfb (factor CAMP), atr (proteína transportadora de la glutamina), sip (proteína inmunogénica de superficie), sodA (superóxido dismutasa), scpB (C5a peptidasa) o ARNr 16S, siendo los blancos más comunes el gen cfb, el atr y el ARNr 16S. El gen cfb codifica por la hemolisi- na encontrada en la mayoría de los aislados [37], exceptuando los aislados CAMP nega-
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
tivos que presentan deleciones de este gen gen [47]. El gen sip que codifica por la proteína generando resultados falsos negativos [50] inmunogénica de superficie es altamente con- y disminuyendo la efectividad de este blanco servado, esta proteína se encuentra expuesta para la detección de la bacteria. El gen atr ha en la superficie de todos los serotipos del SGB. sido reportado como el de mayor rendimiento Escobar et al. validaron un qPCR cuyo blanco por algunos autores [47,51] los cuales sugie- fue el gen sip con un límite de detección entre ren que, cuando se utilice como blanco de 2 a 5 fg/µL de ADN y correlación del 100 % amplificación el gen cfb, se debe incluir otro con el cultivo [52].
Tabla 3. Pruebas moleculares para la detección e identificación del SGB.
Estudio | Muestra utilizada (n) | Prueba molecular | Gen blanco | Sensibilidad (%) | Especificidad (%) |
Couturier BA, et al. 2014 [45] | Hisopados vagino- rectales (314) | BD Max GBS/ Illumigene GBS/ BD GeneOhm StrepB | cfb | 100 98,5 100 | 98 100 98,4 |
Mashouf RY, et al. 2014 [53] | Hisopados vaginales (203) | PCR convencional | ARNr 16S | 88,2 VPPa :35,7 LD: 100 UFC/mL | 87,4 VPNb: 99 |
Ferreira MB, et al. 2018 [54] | Hisopados vagino- rectales (130) | PCR convencional qPCR | atr cfb | 100 100 LDc 10 copias/µL | 85,6 73,6 |
Otaguiri ES, et al. 2018 [55] | Hisopados vagino- rectales (102) | qPCR múltiple | cfb ermBd, ermA, mefA/Be | 91,7 | 95,5 |
Hernández DR, et al. 2018 [16] | Hisopados vagino- rectales (726) | Aries GBS qPCR | cfb | 96,1 | 91,4 |
Shin JH, Pride D. 2019 [18] | Hisopados vagino- rectales (500) | qPCR: Hologic Panther Fusion/ Luminex Aries GBS/ Cepheid Xpert GBS LB | cfb /sip cfb cfb | 95,9 95,9 95,9 | 99,4 98,3 96,3 |
Vieira LL, et al. 2019 [56] | Hisopados vagino- rectales (270) | qPCR Xpert GBS | cfb cfb | - 62 53 | - 76 93 ref. qPCR |
Zietek M, et al. 2020 [57] | Hisopados vagino- rectales (106) | Xpert GBS (intraparto) | cfb | 81,8 | 86,9 |
Zeng YF, et al. 2020 [58] | Banco de cepas | ddPCR | cpsEf | NRg LD: 5pg/µL | NR |
Han MY, et al. 2021 [59] | Revisión 13 estudios | Xpert GBS (directo) Xpert GBS LB | cfb | 91 96 | 93 94 |
Bogiel T, et al. 2021 [60] | Hisopados vagino-rectales (250) | PCR convencional PCR convencional BDMax | cfb ARNr 16S cfb | NR NR 96,4 | NR NR 96,9 ref. Consenso |
Bogiel T, et al 2022 [61] | Hisopados vagino-rectales (250) | qPCR | cfb | 100 VPP 60,3 | 87,1 VPN 100 |
Peris MP, et al. 2022 [62] | Hisopados vagino rectales (413) | Viasure Streptococcus B qPCR | cfb | 97 | 100 |
Daniels J, et al. 2022 [63] | Hisopados vagino- rectales (722) | GeneXpert Dx IV GBS | cfb | 86 | 89 |
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Estudio | Muestra utilizada (n) | Prueba molecular | Gen blanco | Sensibilidad (%) | Especificidad (%) |
Thwe PM, et al. 2022 [50] | Hisopados vagino-rectales (621) | Xpert GBS LB XC | GTFPh/ LysRi | 99,1 VPP 71,6 VPP 95,9 LD 40-682 UFC/mL | 91,8 VPN 99,8 ref. consenso VPN 99,8 |
Chen XJ, et al. 2023 [64] | Vagino-rectales (164) | BD MAX | cfb | 100 88,4 VPP | 96 VPN 100 |
Koliwer-Brandl H, et al. 2023 [65] | hisopado vaginal (260) | Xpert GBS (directo) Genome ERA (directo) | cfb | 71,4 98,6 | 88,1 99,1 |
Sroka-Oleksiak A, et al. 2023 [47] | Hisopados vaginales y rectales (124) | PCR convencional qPCR | ARNr 16S atr cfb | (vag/rec) NR 100/100 100/90,9 | (vag/rec) NR 96,9/99 96,9/99 |
McKenna JP, et al. 2017 [66] | Hisopados vaginales (157) | LAMP (directo) | sip | 95,4 VPP100 LD: 14 copias | 100 ref. qPCR VPN 98,3 |
Guo XG, et al. 2019 [67] | Banco de cepas | Real-LAMP | fbsB j | 96,7 LD: 300 pg/µL | 91,7 |
Pu W, et al 2019 [68] | Hisopado vaginal (180) | LAMP | pcsBk | NR LD: 1pg | NR |
Xu X, et al. 2022 [69] | Hisopados vaginales (103) | LAMP vs LAMP-microfluidic chip | glkl | 100% concordancia en positivos | 92% concordancia en negativos |
Van Der Linden M, et al. 2022 [70] | Banco de cepas (104) | LAMP (HiberGene GBS test) | sip | 100 | NR |
Sung JH, et al. 2022 [71] | Hisopados vagino-rectales (527) | LAMP | sip | 87 100 | 81,2 100 ref. qPCR BDMax |
Lemaire D, et. al. 2023 [72] | Hisopado Vaginal (354) | LAMP (HiberGene) | sip | 87, 7 VPP 89,6 | 98 VPN 97,6 |
Chen J, et al. 2018 [73] | Banco de cepas (100) | RPA propidium monoazida | sip | 100% concordancia de positivos LD: 6000 copias | NR |
Hu S, et al. 2019 [74] | Hisopados Vaginales (130) | RPA | cfb | 100 100 | 99 100 ref. qPCR |
Yu D, et al. 2023 [75] | Hisopados cervicales o vaginales (179) | RPA-CRISPR – GBS (directo) | cfb | 96,6 | 100 ref. cultivo+ MALDI-TOF |
To KN, et al. 2019 [76] | Banco de cepas (947) | MALDI-TOF | N/A | 97 | 100 |
Tanno D, et al. 2022 [77] | Hisopados vagino-rectales (178) | MALDI-TOF (análisis de picos) | N/A | 100 | 88 |
Notas: aVPP: valor predictivo positivo, bVPN: valor predictivo negativo, cLD: límite de detección, dermA, ermB: genes codificadores de metilasa A y B, emefA/B: gen codificante por bomba de flujo activo fcpsE: gen E implicado en la expression de la cápsula, gNR: no reportado, hGTFP: regulador de la familia de proteinas glicosil transferasa. iLysR: región del regulador transcripcional del activador de la biosíntesis de lisina, jfbsB: gen de la proteina de union al fibrinógeno; lglk: gen de la glucoquinasa, kpcsB gen de la hidrolasa hipotética del peptidoglican; N/A no aplica, proteínas de la subunidad 28 ribosomal. La sensibilidad y especificidad de los métodos fue en su mayoría calculada con el cultivo como referencia excepto cuando se indica explícitamente otra referencia.
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Recientemente se ha diseñado un qPCR cuyo blanco incluye dos regiones cromoso- males del SGB, una región que codifica por una proteína glicosil-transferasa (GTFP) y una región del regulador transcripcional LysR, el propósito de esta técnica es subsanar las limitaciones de la PCR cuyo blanco es solo el gen cfb [50].
La mayoría de los estudios encontrados compararon el PCR convencional y el qPCR con el cultivo y las pruebas fenotípicas. La sensibilidad del PCR se ha observado hasta en un 100 % con un 87.1 % de especificidad, estos valores varían de acuerdo con el tipo de prueba [6], como se observa en la Tabla 3. En general, el PCR presenta mayor sensibilidad y especificidad que el cultivo, y el formato en tiempo real ha demostrado ser más rápido, sen- sible y con un límite de detección > 40 UFC/mL en comparación con el PCR convencional [54].
Las pruebas moleculares generan resulta- dos en menor tiempo, pueden automatizarse y procesar simultáneamente múltiples muestras [45], por lo que algunos autores sugieren que sea el nuevo estándar de oro [18,50,54]. Sin embargo, para realizar el PCR también es ne- cesario incluir el enriquecimiento en caldo TH suplementado, con el fin de aumentar su sensi- bilidad entre un 33 – 63 % para los cebadores atr y entre 44.4 – 54.5 % para los cebadores cfb [47].
El PCR se ha acoplado a plataformas au- tomatizadas de extracción, amplificación y detección del ADN en tiempo real, tales como el BD Max (Beckton Dickinson), Cepheid Smart GBS, Xpert GBS, Xpert GBS LB, Xpert GBS LB XC, Xpert Xpress (Cepheid), Illuminege system (Meridian Bioscience), Aries GBS (Luminex), IDI-Strep B (Infecto Diagnostics), AMPLIVUE GBS (QUIDEL) y GenePOC GBS LB, las cuales detectan el gen cfb (Tabla 3). Un ejemplo es el BDMax GBS que amplifica el gen cfb con sensi- bilidad de 200 UFC/mL y que en 2 horas puede procesar hasta 24 muestras simultáneamente [60]. Algunas pruebas comerciales pueden
realizarse directamente en las muestras como prueba rápida directa (sin enriquecimiento) y a pesar de que generan falsos negativos, su rendimiento es equivalente al del cultivo [42]. A pesar de su utilidad potencial, las pruebas di- rectas intraparto aún no se recomiendan como reemplazo del tamizaje anteparto debido a que no hay suficiente información que respalde su uso de rutina. Estudios previos no aleatorios no encontraron un beneficio estadísticamente significante cuando comparan las pruebas rápidas intraparto y el cultivo, no obstante, se necesitan estudios aleatorios para evaluar este aspecto [63]. A pesar de su sensibilidad variable, las pruebas comerciales directas son consideradas de utilidad en un tamizaje rápido [6,56]. Actualmente, el mejoramiento de las plataformas para pruebas rápidas intraparto es uno de los objetivos de desarrollo en cuanto a la detección de la bacteria en gestantes [78]. Las pruebas rápidas entre sí tienen efectividad simi- lar, aunque algunas ofrecen mayor flexibilidad y formatos simples que no requieren personal entrenado. Un ejemplo es el GenomERa que se ha descrito como un sistema muy simple y que puede ser aplicado fácilmente en el punto de atención [65,79].
Los métodos de extracción de ADN también pueden impactar la sensibilidad y especificidad del PCR; Schörner et al. [80] observaron que la extracción utilizando guanidina 5M tenía una sensibilidad y especificidad de 100 y 86.5 %, respectivamente, mientras que la utilización de un estuche comercial tuvo una sensibilidad y especificidad del 50 y 95 %. Lo anterior sugie- re que el rendimiento del PCR incluso puede optimizarse a nivel de la extracción. Recien- temente se ha desarrollado un PCR digital de tercera generación que puede detectar hasta 5 pg/µL de ADN, este método ultrasensible permite la cuantificación de ADN, pero todavía no está disponible comercialmente [58]. El PCR digital diluye y divide la mezcla de reacción y la distribuye en microgotas, las cuales son amplificadas en reacciones independientes, el rendimiento es parecido al del qPCR y se
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
ha utilizado en la cuantificación de patógenos. Otras versiones del PCR permiten la diferen- ciación de los tipos capsulares del SGB, lo cual es importante para la vigilancia epidemiológica, evaluación de vacunas y la identificación de los tipos más virulentos en neonatos, tales como los tipos Ia, Ib y III [81,82].
Aunque el qPCR es muy sensible y genera resultados en pocas horas, aún requiere de equipo especializado, preparación de la mues- tra y personal entrenado, haciéndolo menos versátil para ser una prueba rápida o de punto de atención del paciente. Una alternativa es el LAMP, otra NAAT ampliamente utilizada para diagnóstico con formatos simples y cualitativos de alta sensibilidad y especificidad [66]. Esta técnica puede ser manual, semiautomatizada o automatizada y se ha aplicado en la detección del SGB utilizando genes blanco diferentes al cfb, particularmente el sip, con una sensibili- dad del 87 % comparada con el cultivo, y del 100 % comparada con el PCR [70,71] y con una especificidad entre el 81 – 100 % [66,71]. Se han reportado pruebas LAMP con límites de detección de 1 pg de ADN [68] y procesamiento entre 45 - 80 minutos [67].
Otra NAAT isotérmica utilizada es la RPA, la cual es altamente sensible y selectiva, requiere de una preparación mínima de la muestra y amplifica de 1 a 10 copias de ADN en menos de 20 minutos. Básicamente, los cebadores se combinan con una recombinasa que identifica la región blanco para que luego una proteína de unión al ADN monocatenario permita que se integre una polimerasa que amplifica el frag- mento. Para la detección de genes cfb y sip se ha reportado una concordancia del 100 % con el PCR y el cultivo [74] con límite de detección de 6.000 copias y procesamiento de 4 h 20 minutos, también se han descrito pruebas RPA para discriminar bacterias viables [73].
La mayor limitación de las NAATs para la detección del SGB es que se requiere una prueba adicional para determinar la sensibilidad a clindamicina y eritromicina. Otaguiri et al. de-
sarrollaron un qPCR múltiple para detectar los genes ermA, ermB que codifican por metilasas ribosomales y mefA/B codificante de las bom- bas de flujo, los cuales confieren resistencia a macrólidos y lincosamidas [55]. Sin embargo, el PCR múltiple solo está estandarizado para ser realizado a partir de las colonias del SGB debido a que otras bacterias pueden tener los mismos genes de resistencia, generando así falsos positivos si se hace directamente de la muestra.
Técnicas novedosas diferentes a las NAATs también han sido descritas, como por ejemplo, el CRISPR-GBS utilizada por Yu et al. para la detección del gen cfb con una sensibilidad y especificidad > 96 % y un tiempo de proce- samiento de 35 minutos sin enriquecimiento [75]. Otro ejemplo es el análisis de perfiles protéicos diferenciales (subunidad 28s del RNA ribosomal) mediante el MALDI-TOF que identifica la bacteria con una sensibilidad del 100 % y especificidad del 88 % (en referen- cia con el cultivo) detectándola directamente del medio de enriquecimiento sin subcultivo [77]. El MALDI-TOF se ha descrito como una técnica rápida, simple y de fácil adaptación al diagnóstico microbiológico [76]. Este método se ha utilizado para discriminación de tipos capsulares, linajes y del clon hipervirulento en aislados de diferentes fuentes [19].
Recientemente, Alsheim et al. utilizaron un sistema basado en un sensor que incluye una vesícula de fosfolípidos y ácidos grasos acopla- dos con carboxi-fluoresceina que puede ser li- sada por los factores de virulencia de la bacteria con una sensibilidad del 83.3 % y especificidad del 85.7 % y con un tiempo de proceso de 45 minutos [83], con la ventaja de que esta técnica puede detectar bacterias viables.
La detección eficaz del SGB es determinante para el enfoque del tratamiento y conductas en las gestantes colonizadas y sus neonatos. Aunque el cultivo sigue siendo el estándar de
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
oro, la detección óptima del SGB requiere la aplicación de los protocolos recomendados integrando las pruebas moleculares. Existe evidencia amplia y fundamentada del beneficio de la detección molecular sobre el cultivo. Las NAATs, en general e independiente del formato, tienen una alta sensibilidad y especificidad con tiempos reducidos de respuesta, siendo costo- efectivas. En comparación con el cultivo, el PCR en el tamizaje permite identificar un mayor número de gestantes colonizadas, las cuales deben someterse a la profilaxis intraparto para disminuir el riesgo de infección neonatal, por lo que la incorporación de estas técnicas en la de- tección rutinaria del SGB es crucial para evitar los falsos negativos. No obstante, en casos de gestantes alérgicas a la penicilina, el cultivo se requiere para evaluar la sensibilidad a clinda- micina y eritromicina a partir de las colonias. La viabilidad y densidad de colonización también son importantes para determinar la posibilidad de transmisión; la integración de estos aspectos en las pruebas moleculares es una necesidad que aún está en proceso.
Existen desafíos importantes en cuanto a la detección del SGB a nivel mundial y particu- larmente en países de bajo y mediano ingre- so, como el nuestro, entre ellos la adherencia a los protocolos recomendados para cultivo (preenriquecimiento) y la inclusión imperativa de las NAATs al menos en el tamizaje ante- parto, dado que en la actualidad solo se utiliza
el cultivo de rutina. Adicionalmente, debido a que no hay una correlación total entre la colonización anteparto e intraparto y de la posibilidad de no tener historia de tamizaje en gestantes con partos prematuros (< 37 semanas), se necesitan pruebas rápidas que se apliquen intraparto y permitan instaurar la terapia oportunamente. En países de alto ingreso, las pruebas de diagnóstico molecular anteparto e intraparto han sido incorporadas en la rutina, demostrando su beneficio para prevenir la infección severa y sus consecuen- cias en términos de salud y costos. Mientras la vacuna es una realidad, los retos de la detección del SGB deben afrontarse mediante el conocimiento y aplicación de las guías es- tablecidas y de pruebas predictoras efectivas de la colonización intraparto.
Declaración ética: Este trabajo no requiere aval de comité de ética.
Conflicto de intereses: Los autores del manuscrito no declaran conflicto de intereses.
Financiamiento: Ninguno.
Apoyo tecnológico: Los autores informan que no usaron Inteligencia Artificial, o tecnolo- gías similares en la elaboración o edición de este documento.
Contribución: Ambos autores contribuyeron en el diseño, análisis, redacción y revisión del manuscrito.
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Raabe VN, Shane AL. Group B Streptococcus (Streptococcus agalactiae). In: Fischetti VA, Novick RP, Ferretti JJ, Portnoy DA, Braunstein M and Rood JI, editors. Gram-Positive Pathogens 3rd ed. Washington, DC, USA: ASM Press; 2019. p. 228–238. doi: https://doi.org/10.1128/9781683670131.ch14
Gonçalves BP, Procter SR, Paul P, Chandna J, Lewin A, Seedat F, et al. Group B Streptococcus infection during pregnancy and infancy: estimates of regional and global burden. Lancet Glob Health. 2022;10(6):e807–e19.
Stephens K, Charnock-Jones DS, Smith GCS. Group B Streptococcus and the risk of perinatal morbidity and morta- lity following term labor. Am J Obstet Gynecol. 2023;228(5):S1305–12. doi: https://doi.org/10.1016/j.ajog.2022.07.051
Gizachew M, Tiruneh M, Moges F, Adefris M, Tigabu Z, Tessema B. Proportion of Streptococcus agalactiae vertical transmission and associated risk factors among Ethiopian mother-newborn dyads, Northwest Ethiopia. Sci Rep. 2020;10(1):1–8. doi: https://doi.org/10.1038/s41598-020-60447-y
Madrid L, Seale AC, Kohli-Lynch M, Edmond KM, Lawn JE, Heath PT, et al. Infant Group B Streptococcal Disease incidence and serotypes worldwide: Systematic review and meta-analyses. Clin Infect Dis. 2017;65(S2):S60-S72. doi: https://doi.org/10.1093/cid/cix656
Filkins L, Hauser J, Robinson-Dunn B, Tibbetts R, Boyanton B, Revell P. Guidelines for the Detection and identi- fication of Group B Streptococcus. Washington, DC: American Society for Microbiology. 2020.
Disponible en: https://asm.org/Guideline/Guidelines-for-the-Detection-and-Identification-of
da Rocha JZ, Feltraco J, Radin V, Gonçalves CV, da Silva PEA, von Groll A. Streptococcus agalactiae colonization and screening approach in high-risk pregnant women in southern Brazil. J Infect Dev Ctries. 2020;14(4):332–40. doi: https://doi.org/10.3855/jidc.12025
Walker KF, Plumb J, Gray J, Thornton JG, Avery AJ, Daniels JP. Should all pregnant women be offered testing for group B Streptococcus? BMJ. 2021;373:n882. doi: https://doi.org/10.1136/bmj.n882
World Health Organization. Group B Streptococcus vaccine: full value of vaccine assessment. Geneva: WHO. 2021. p. 19–32. Disponible en: https://www.who.int/publications/i/item/9789240037526
Costa SC, Machado AP, Teixeira C, Cerqueira L, Rodrigues T, Ribeiro M, et al. Group B Streptococcus rectovagi- nal colonization screening on term pregnancies: ¿culture or polymerase chain reaction? J Matern Fetal Neonatal Med. 2023;36(2). doi: https://doi.org/10.1080/14767058.2023.2262078
Picchiassi E, Coata G, Babucci G, Giardina I, Summa V, Tarquini F, et al. Intrapartum test for detection of Group B Streptococcus colonization during labor. J Matern Fetal Neonatal Med. 2018;31(24):3293–300.
Hayes K, O’Halloran F, Cotter L. A review of antibiotic resistance in Group B Streptococcus: the story so far. Crit Rev Microbiol. 2020;46(3):253–69. doi: https://doi.org/10.1080/1040841X.2020.1758626
HogenEsch E, De Mucio B, Haddad LB, Vilajeliu A, Ropero AM, Yildirim I, et al. Differences in maternal group B
Streptococcus screening rates in Latin American countries. Vaccine. 2021;39: B3–B11. doi: https://doi.org/10.1016/j.vaccine.2020.10.082
Centro Nacional de Investigación en Evidencia y Tecnología en Salud CINETS. GuíaS de Práctica Clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio. Guías de Práctica Clínica. 2013. p. 1–84. https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/INEC/IETS/G.Corta.Embarazo.y.parto.Prof.Sa- lud.2013%20(1).pdf
Ospino-Muñoz AM, Bonza-González EA, Arévalo-Mojica CD, Rubio-Romero JA. Adherence to recommendations for preventing early neonatal sepsis associated with Streptococcus agalactiae colonization in a referral center in Bogotá, Colombia. 2019. Rev Colomb Obstet Ginecol. 2022;73(3):175–83. doi: https://doi.org/10.18597/RCOG.3917
Hernandez DR, Wolk DM, Walker KL, Young S, Dunn R, Dunbar SA, et al. Multicenter diagnostic accuracy evalua- tion of the luminex aries real-time PCR assay for group B Streptococcus detection in LIM broth-enriched samples. J Clin Microbiol. 2018;56(8):1–9. doi: https://doi.org/10.1128/JCM.01768-17
Di Renzo GC, Melin P, Berardi A, Blennow M, Carbonell-Estrany X, Donzelli GP, et al. Intrapartum GBS screening and antibiotic prophylaxis: A European consensus conference. J Matern Fetal Neonatal Med. 2015; 28(7):766–82. doi: https://doi.org/10.3109/14767058.2014.934804
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Shin JH, Pride DT. Comparison of three nucleic acid amplification tests and culture for detection of group B Strep- tococcus from enrichment broth. J Clin Microbiol. 2019;57(6):1–9. doi: https://doi.org/10.1128/JCM.01958-18
Rothen J, Sapugahawatte DN, Li C, Lo N, Vogel G, Foucault F, et al. A simple, rapid typing method for Strepto- coccus agalactiae based on ribosomal subunit proteins by MALDI-TOF MS. Sci Rep. 2020;10(1):1–8.
Baethge C, Goldbeck-Wood S, Mertens S. SANRA una escala para la evaluación de la calidad de los artículos de revisión narrativa. [SANRA—a scale for the quality assessment of narrative review articles]. Res Integr Peer Rev. 2019;4:2–8. doi: https://doi.org/10.1186/s41073-019-0064-8
Sahuquillo-Arce JM, Hernández-Cabezas A, Castaño-Aroca MJ, Chouman-Arcas R, Díaz-Aguirre E, Acosta-Boga B, et al. Streptococcus agalactiae in childbearing age immigrant women in Comunitat Valenciana (Spain). Sci Rep. 2020;10(1):1–8. doi: https://doi.org/10.1038/s41598-020-66811-2
Bobadilla FJ, Novosak MG, Cortese IJ, Delgado OD, Laczeski ME. Prevalence, serotypes and virulence genes of Streptococcus agalactiae isolated from pregnant women with 35–37 weeks of gestation. BMC Infect Dis. 2021;21(1):1–11. doi: https://doi.org/10.1186/s12879-020-05603-5
Palacios-Saucedo GC, Rivera-Morales LG, Vázquez-Guillén JM, Caballero-Trejo A, Mellado-García MC, Flores- Flores AS, et al. Genomic analysis of virulence factors and antimicrobial resistance of group B Streptococcus isolated from pregnant women in northeastern Mexico. PLoS One. 2022;17(3):e02642273.
Vielot NA, Toval-Ruíz CE, Weber RP, Becker-Dreps S, Alemán Rivera T de J. Rectovaginal group B Streptococ- cus colonization among pregnant women in Nicaragua: a systematic review and meta-analysis. J Matern Fetal Neonatal Med. 2021;34(15):2418–26. doi: https://doi.org/10.1080/14767058.2019.1667324
Ceballos CA, Loaiza N, Romero J, Ospina M, Vásquez EM. Caracterización de las gestantes tamizadas para Streptococcus agalactiae y su relación con sepsis neonatal temprana, en la Clínica del Prado de Medellín (Co- lombia), año 2010. Infectio. 2014;18(2):66–71. doi: https://doi.org/10.1016/j.infect.2013.12.002
Duque CM, Sánchez DM, Gómez B, Carmona JA, Cifuentes D, Gaviria AM, et al. Evaluación de una técnica de PCR en tiempo real para determinar colonización por Streptococcus agalactiae en mujeres gestantes de Medellín que consultan en Dinamica IPS. Infectio. 2018;22(1):26–9.
Disponible en: http://www.scielo.org.co/pdf/inf/v22n1/0123-9392-inf-22-01-00026.pdf
Amaya-Pino JP, Bello-Trujillo A, Mendivil-Ciodaro C, Correa-Jiménez Ó, Reyes-Ramos N. Prevalencia de colo- nización vaginal y rectal por Streptococcus agalactiae en gestantes con trabajo de parto pretérmino en Clínica Maternidad Rafael Calvo entre agosto 2011 y enero 2012. Red Colombiana de Información Científica. 2013. Disponible en: https://redcol.minciencias.gov.co/Record/UCART2_5f2dc6ae97caf51113fd32a6a950b296
Campo CH, Martínez MF, Otero JC, Rincón G. Prevalencia de colonización vaginorrectal por Streptococcus aga- lactiae y su perfil de sensibilidad en mujeres embarazadas atendidas en un hospital de tercer nivel. Biomedica. 2019;39(4):689–98. doi: https://doi.org/10.7705/biomedica.4514
Pertuz Meza YB, González Ruiz GE. Efficacy of a molecular test in the diagnosis of Streptococcus agalactiae in pregnant patients from the city of Santa Marta (Colombia). Salud Uninorte. 2021;36(2):425–35. Disponible en: http://www.scielo.org.co/scielo.php?script=sci_abstract&pid=S0120-55522020000200425&lng=en
Vornhagen J, Adams Waldorf KM, Rajagopal L. Perinatal group b streptococcal infections: virulence factors, immu- nity, and prevention strategies. Trends Microbiol. 2017;25(11):919–31. doi: https://doi.org/10.1016/j.tim.2017.05.013
Lu J, Moore RE, Spicer SK, Doster RS, Guevara MA, Francis JD, et al. Streptococcus agalactiae npx is required for survival in human placental macrophages and full virulence in a model of ascending vaginal infection during pregnancy. mBio. 2022;13(6):e02870-22. doi: https://doi.org/10.1128/mbio.02870-22
Allard MJ, Brochu ME, Bergeron JD, Segura M, Sébire G. Causal role of group B Streptococcus-induced acute chorioamnionitis in intrauterine growth retardation and cerebral palsy-like impairments. J Dev Orig Health Dis. 2019;10(5):595–602. doi: https://doi.org/10.1017/S2040174418001083
Armas Fernández A, Toraño Peraza G, Medina Hernández D, Orcasitas Alegría AM, Fragoso Simón R. Rectum/vagi- nal colonization by Streptococcus agalactiae in Cuban pregnant women. Rev Cubana Med Trop. 2018;70(3):27–37. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0375-07602014000300009&lng=es
Monari F, Gabrielli L, Gargano G, Annessi E, Ferrari F, Rivasi F, et al. Fetal bacterial infections in antepartum stillbirth: A case series. Early Hum Dev. 2013;89(12):1049–54. doi: https://doi.org/10.1016/j.earlhumdev.2013.08.010
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Vasikasin V, Changpradub D. Clinical manifestations and prognostic factors for Streptococcus agalactiae bacte- remia among nonpregnant adults in Thailand. J Infect Chemother. 2021;27(7):967–71.
Crespo-Ortiz MP, Castañeda-Ramírez CR, Recalde-Bolaños M, Vélez-Londoño JD. Emerging trends in invasive and noninvasive isolates of Streptococcus agalactiae in a Latin American hospital: A 17-year study. BMC Infect Dis. 2014:428. doi: https:/doi.org/10.1186/1471-2334-14-428
Rosa-Fraile M, Spellerberg B. Reliable detection of Group B Streptococcus in the clinical laboratory. J Clin Micro- biol. 2017;55(9):2590–8. doi: https://doi.org/10.1128/JCM.00582-17
Sobral Pena JM, Lannes-Costa PS, Nagao PE. Vaccines for Streptococcus agalactiae: current status and future perspectives. Front Immunol. 2024;15:1430901. doi: https://doi.org/10.3389/fimmu.2024.1430901
Russell NJ, Seale AC, O’Driscoll M, O’Sullivan C, Bianchi-Jassir F, Gonzalez-Guarin J, et al. Maternal colonization with Group B Streptococcus and serotype distribution worldwide: Systematic review and meta-analyses. Clin Infect Dis. 2017;65(Suppl 2):S100–11. doi: https://doi.org/10.1093/cid/cix658
Seale AC, Bianchi-Jassir F, Kohli-Lynch M, Tann CJ, Hall J, et al. Estimates of the burden of Group B Streptococcal disease worldwide for pregnant women, stillbirths, and children. Clin Infect Dis. 2017;65(Suppl 2): S200–19.
Almeida A, Rosinski-Chupin I, Plainvert C. Douarre PM, Borrego MJ, Poyart C, et al. Parallel evolution of Group B
Streptococcus hypervirulent clonal complex 17 unveils new pathoadaptive mutations. mSystems. 2017;2(5):e00074-
Plainvert C, El Alaoui F, Tazi A, Joubrel C, Anselem O, Ballon M, et al. Intrapartum group B Streptococcus scree- ning in the labor ward by Xpert® GBS real-time PCR. Eur J Clin Microbiol Infect Dis. 2018;37(2):265–70.
Stoll BJ, Puopolo KM, Hansen NI, Sánchez PJ, Bell EF, Carlo WA, et al. Early-Onset neonatal sepsis 2015 to 2017, the rise of Escherichia coli, and the need for novel prevention strategies. JAMA Pediatr. 2020;174(7).
Jiang Y, Zhou J, Li Z, Sun L. To evaluate impact on detection rate of Streptococcus agalactiae in the third trimester of pregnancy. Research Square. 2023;1–11. doi: https://doi.org/10.21203/rs.3.rs-2627065/v1
Couturier BA, Weight T, Elmer H, Schlaberg R. Antepartum screening for group B Streptococcus by three FDA- cleared molecular tests and effect of shortened enrichment culture on molecular detection rates. J Clin Microbiol. 2014;52(9):3429–32. doi: https://doi.org/10.1128/JCM.01081-14
Gendrin C, Vornhagen J, Armistead B, Singh P, Whidbey C, Merillat S, et al. A nonhemolytic Group B Streptococ- cus strain exhibits hypervirulence. J. Infect. Dis. 2018;217(6):983–7. doi: https://doi.org/10.1093/infdis/jix646
Sroka-Oleksiak A, Pabian W, Sobońska J, Drożdż K, Bogiel T, Brzychczy-Włoch M. Do NAAT-Based methods increase the diagnostic sensitivity of Streptococcus agalactiae carriage detection in pregnant women? Diagnostics. 2023;13(5). doi: https://doi.org/10.3390/diagnostics13050863
Zhu Y, Lin XZ. Updates in prevention policies of early-onset group B streptococcal infection in newborns. Pediatr Neonatol. 2021;62(5):465–75. doi: https://doi.org/10.1016/j.pedneo.2021.05.007
Mirsky R, Carpenter DM Postlethwaite, DA, Regenstein AC. Preventing early-onset group B streptococcal sepsis: is there a role for rescreening near term? J Matern Fetal Neonatal Med. 2020;33(22):3791–97.
Thwe PM, Faron ML, Pride DT, Cruz A, Gerstbrein D, Nahmod KA, et al. Multicenter evaluation of the Cepheid Xpert GBS LB XC Test. J Clin Microbiol. 2022;60(12):7–12. doi: https://doi.org/10.1128/jcm.01356-22
Mousavi SM, Hosseini SM, Mashouf RY, Arabestani MR. Identification of group B Streptococci using 16S rRNA, cfb, scpB, and atr genes in pregnant women by PCR. Acta Med Iran. 2016;54(12):765–70.
Escobar DF, Diaz-Dinamarca DA, Hernández CF, Soto DA, Manzo RA, Alarcón PI, et al. Development and analyti- cal validation of real-time PCR for the detection of Streptococcus agalactiae in pregnant women. BMC Pregnancy Childbirth. 2020;20(1):1–10. doi: https://doi.org/10.1186/s12884-020-03038-z
Mashouf RY, Mousavi SM, Rabiee S, Alikhani MY, Arabestani MR. Direct identification of Streptococcus agalactiae in vaginal colonization in pregnant women using polymerase chain reaction. J Compr Ped. 2014;5(4):e23339. doi: https://doi.org/10.17795/compreped-23339
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
Ferreira MB, de-Paris F, Paiva RM, de Souza Nunes L. Assessment of conventional PCR and real-time PCR compared to the gold standard method for screening Streptococcus agalactiae in pregnant women. Braz J Infect Dis. 2018;22(6):449–54. doi: https://doi.org/10.1016/j.bjid.2018.09.005
Saori Otaguiri E, Beletto Morguette AE, Tadachi Morey A, Reis Tavares E, Kerbauy G, de Almeida Torres RSL, et al. Development of a melting-curve based multiplex real-time PCR assay for simultaneous detection of Strep- tococcus agalactiae and genes encoding resistance to macrolides and lincosamides. BMC Pregnancy Childbirth. 2018;18(1):126. doi: https://doi.org/10.1186/s12884-018-1774-5
Vieira LL, Perez AV, Machado MM, Kayser ML, Vettori D V, Alegretti AP, et al. Group B Streptococcus detection in pregnant women: Comparison of qPCR assay, culture, and the Xpert GBS rapid test. BMC Pregnancy Childbirth. 2019;19(1)532. doi: https://doi.org/10.1186/s12884-019-2681-0
Zietek M, Jaroszewicz-Trzaska J, Szczuko M, Mantiuk R, Celewicz Z. Intrapartum PCR assay is a fast and effi- cient screening method for group b Streptococcus detection in pregnancy. Ginekol Pol. 2020;91(9):549–53. PMID: 33030736
Zeng YF, Chen CM, Li XY, Chen JJ, Wang YG, Ouyang S, et al. Development of a droplet digital PCR method for detection of Streptococcus agalactiae. BMC Microbiol. 2020;20:179.
Han MY, Xie C, Huang QQ, Wu QH, Deng QY, Xie TA, et al. Evaluation of Xpert GBS assay and Xpert GBS LB assay for detection of Streptococcus agalactiae. Ann Clin Microbiol Antimicrob. 2021;20(1):1–11.
Bogiel T, Depka D, Zalas-Więcek P, Rzepka M, Kruszyńska E, Gospodarek-Komkowska E. Application of the ap- propriate molecular biology-based method significantly increases the sensitivity of group B Streptococcus detection results. J Hosp Infect. 2021;112:21–6. doi: https://doi.org/10.1016/j.jhin.2021.03.008
Bogiel T, Ziółkowski S, Domian A, Dobrzyńska Z. An application of real-time PCR and CDC protocol may signifi- cantly reduce the incidence of Streptococcus agalactiae infections among neonates. Pathogens. 2022;11(9). doi: https://doi.org/10.3390/pathogens11091064
Peris MP, Martín-Saco G, Alonso-Ezcurra H, Escolar-Miñana C, Rezusta A, Acero R, et al. Retrospective study for the clinical evaluation of a real-time PCR assay with lyophilized and ready-to-use reagents for Streptococcus agalactiae detection in prenatal screening specimens. Diagnostics. 2022;12(9).
Daniels J, Dixon EF, Gill A, Bishop J, D’Amico M, Ahmed K, et al. A rapid intrapartum test for group B Strepto- coccus to reduce antibiotic usage in mothers with risk factors: the GBS2 cluster RCT. Health Technol Assess. 2022;26(12):1-82. doi: https://doi.org/10.3310/BICF1187
Chen XJ, Wan TW, Chao QT, Teng LJ, Lee T fen, Huang YT, et al. Applicability of an in-house extraction protocol in a Bruker Biotyper matrix-assisted laser desorption/ionization time-of-flight mass spectrometry system for the identification of Streptococcus agalactiae from broth-enriched vaginal/rectal swab specimens. J Microbiol Immunol Infect. 2023;56(4):815–21. doi: https://doi.org/10.1016/j.jmii.2023.05.003
Koliwer-Brandl H, Nil A, Birri J, Sachs M, Zimmermann R, Zbinden R, et al. Evaluation of two rapid com- mercial assays for detection of Streptococcus agalactiae from vaginal samples. Acta Obstet Gynecol Scand. 2023;102(4):450–6. doi: https://doi.org/10.1111/aogs.14519
McKenna JP, Cox C, Fairley DJ, Burke R, Shields MD, Watt A, et al. Loop-mediated isothermal amplification assay for rapid detection of Streptococcus agalactiae (group B Streptococcus) in vaginal swabs - a proof of concept study. J Med Microbiol. 2017;66(3):294–300. doi: https://doi.org/10.1099/jmm.0.000437
Guo XG, Zhuang YR, Wen JZ, Xie TA, Liu YL, Zhu GD, et al. Evaluation of the real-time fluorescence loop- mediated isothermal amplification assay for the detection of Streptococcus agalactiae. Biosci Rep. 2019;39. doi: https://doi.org/ 10.1042/BSR20190383
Pu W, Wang Y, Yang N, Guo G, Li H, Li Q, et al. Investigation of Streptococcus agalactiae using pcsB-based LAMP in milk, tilapia and vaginal swabs in Haikou, China. J Appl Microbiol. 2020;128(3):784–93.
Xu X, Jia Y, Li R, Wen Y, Liang Y, Lao G, et al. Rapid and simultaneous detection of multiple pathogens in the lower reproductive tract during pregnancy based on loop-mediated isothermal amplification-microfluidic chip. BMC Microbiol. 2022;22(1):1–16. doi: https://doi.org/10.1186/s12866-022-02657-0
Nieva-Posso D.A., Crespo-Ortiz M.P. Detección e identificación de Streptococcus agalactiae en gestantes: aspectos relevantes y revisión narrativa de la literatura.
Arch Med (Manizales). 2025;25(2)
van der Linden M, Jaschek M, Junker J, Levina N, Weidenhaupt B. Evaluation of the ‘HG Group B Streptococ- cus’ loop-mediated isothermal amplification assay for accurate identification of Streptococcus agalactiae. J Med Microbiol. 2022;71(12):1–4. doi: https://doi.org/10.1099/jmm.0.001609
Sung JH, Cha HH, Lee NY, Lee WK, Choi Y, Han HS, et al. Diagnostic accuracy of loop-mediated isothermal amplification assay for Group B Streptococcus detection in recto-vaginal swab: Comparison with polymerase chain reaction test and conventional culture. Diagnostics. 2022;12(7). doi: https://doi.org/10.3390/diagnostics12071569
Lemaire C, Cheminet M, Duployez C, Artus M, Ballaa Y, Devos L, et al. A LAMP-based assay for the molecular detection of group B Streptococcus. Eur J Clin Microbiol Infect Dis. 2023;42(10):1245–50.
Chen J, Wang Y, Liu X, Chen G, Chen X, Chen J, et al. Development of propidium monoazide–recombinase polymerase amplification (PMA-RPA) assay for rapid detection of Streptococcus pyogenes and Streptococcus agalactiae. Mol Cell Probes. 2018;41:32–8. doi: https://doi.org/10.1016/j.mcp.2018.08.007
Hu S, Zhong H, Huang W, Zhan W, Yang X, Tang B, et al. Rapid and visual detection of Group B Streptococ- cus using recombinase polymerase amplification combined with lateral flow strips. Diagn Microbiol Infect Dis. 2019;93(1):9–13. doi: https://doi.org/10.1016/j.diagmicrobio.2018.07.011
Yu D, Liang B, Xu H, Chen L, Ye Z, Wu Z, et al. CRISPR/Cas12a-based assay for the rapid and high-sensitivity detection of Streptococcus agalactiae colonization in pregnant women with premature rupture of membrane. Ann Clin Microbiol Antimicrob. 2023;22(1):1–11. doi: https://doi.org/10.1186/s12941-023-00558-2
To KN, Cornwell E, Daniel R, Goonesekera S, Jauneikaite E, Chalker V, et al. Evaluation of matrix-assisted laser desorption ionisation time-of-flight mass spectrometry (MALDI-TOF MS) for the Identification of Group B Strepto- coccus. BMC Res Notes. 2019;12:85. doi: https://doi.org/10.1186/s13104-019-4119-1
Tanno D, Saito K, Ohashi K, Toyokawa M, Yamadera Y, Shimura H. Matrix-assisted laser desorption ionization – Time-of-flight mass spectrometry with Time-of-Flight peak analysis for rapid and accurate detection of Group B Streptococcus in pregnant women. Microbiol Spectr. 2022;10(3):e0173221.
Emonet S, Schrenzel J, Martinez De Tejada B. Molecular-based screening for perinatal group B streptococcal infection: Implications for prevention and therapy. Mol Diagn Ther. 2013;17(6):355–61.
Andreasen T, Møller JK, Khalil MR. Comparison of BD MAX GBS and GenomEra GBS assays for rapid intrapartum PCR detection of vaginal carriage of group B streptococci. PLoS One. 2019;14(4):1–10.
Schörner MA, May Feuershuette OH, Scheffer MC, Senna SG, Bazzo ML, Maurici R. Detection of Group B Streptococcus agalactiae from anorectal and vaginal screening tests. Clin Microbial, 2014;3(5):169. Disponible en: https://www.researchgate.net/publication/270565089_Detection_of_Group_B_Streptococcus_agalactiae_from_Ano- rectal_and_Vaginal_Screening_Tests
Breeding KM, Ragipani B, Lee Kud, Malik M, Randis TM, Ratner AJ. Real-time PCR-based serotyping of Strep- tococcus agalactiae. Sci Rep. 2016;6:38523. doi: https://doi.org/10.1038/srep38523
Furfaro LL, Chang BJ, Payne MS. Perinatal Streptococcus agalactiae epidemiology and surveillance targets. Clin Microbiol Rev. 2018;31(4):e00049-18. doi: https://doi.org/10.1128/CMR.00049-18
Alsheim E, Thet NT, Laabei M, Jenkins ATA. Development and early testing of a simple, low cost, fast sensor for maternal and neonatal group B Streptococcus. Biosens Bioelectron. 2024;247:115923. doi: https://doi.org/10.1016/j. bios.2023.115923
![]()