Desarrollo y validación de un método analítico para la determinación de Ciprofloxacina en suero por Cromatografía Liquida de Alta Precisión con detección ultravioleta
Ana Falquez Manotas*, Esp, Ger. Sal., Luz Sarmiento Rubiano**, PhD.
* Bacterióloga - Especialista en Gerencia en salud. Coordinadora laboratorio clínico Fundación Hospital Universitario Metropolitano de Barranquilla. afalquezm@yahoo.com
** Bacterióloga PhD. Laboratorio de Cromatografía Universidad Metropolitana de Barranquilla. Lusarru@hotmail.com.
Recibido para publicación: 19-07-2013 - Versión corregida: 11-09-2013 - Aprobado para publicación: 14-11-2013
Referencia Vancouver:
Falquez-Manotas A, Sarmiento-Rubiano L. Desarrollo y validación de un método analítico para la determinación de Ciprofloxacina en suero por Cromatografía Liquida de Alta Precisión con detección ultravioleta. Arch Med (Manizales) 2013; 13(2):119-26.
Referencia Redalyc:
Ana Falquez Manotas, Luz Sarmiento Rubiano. Archivos de Medicina (Manizales). Volumen 13 N° 2. Julio-Dciembre 2013. ISSN versión impresa 1657-320X. ISSN versión en línea 2339-3874. Universidad de Manizales. Manizales
(Colombia).
Resumen
Objetivo: Desarrollar un método rápido y sencillo para la determinación de Ciprofloxacina en muestras de suero para ser utilizado en estudios farmacocinéticos. La Ciprofloxacina es un antibiótico que pertenece al grupo de las fluoroquinolonas, comúnmente usado en Colombia con un amplio espectro antibacterial. Diferentes métodos utilizando Cromatografía Liquida de Alta precisión (HPLC) han sido reportados para el análisis de Ciprofloxacina en fluidos biológicos. Materiales y métodos: Se empleó el método Cromatografía Liquida de Alta Precisión (HPLC) con detección ultravioleta a 280 nm, fase móvil isocrática, Dexametasona como estándar interno y un rango de cuantificación de 0,1 a 10 μg/ml. Resultados: Los tiempos de retención fueron 4,93 min y 15,71 minutos para Ciprofloxacina y Dexametasona respectivamente, la precisión y exactitud fueron superiores al 95% y el tiempo total de elución fué de 20 minutos por muestra. Conclusiones: Se desarrolló y validó un método analítico para la determinación de Ciprofloxacina en suero, lo suficientemente sensible, exacto, y reproductible para ser usado en estudios farmacocinéticos. Palabras clave. Cromatografía, farmacocinética, profilaxis antibiótica, suero.
Palabras clave: Cromatografía, farmacocinética, Profilaxis Antibiótica, suero.
Development and validation of an analytical method for the determination of ciprofloxacin in serum by High-Performance Liquid Chromatography with ultraviolet detectionphy with ultraviolet detection
Summary
Objective: To develop a rapid and simple method for Ciprofloxacin determination in samples of whey to be used in pharmacokinetic studies. Ciprofloxacin is an antibiotic that belongs to the group of the fluoroquinolone, commonly used in Colombia with an extensive antibacterial spectrum. Several High-Performance Liquid Chromatography (HPLC) methods have been reported for the analysis of ciprofloxacin in biological fluids. Materials and methods: the method used was High-Performance Liquid Chromatography (HPLC) with ultraviolet detection to 280 nm, mobile phase isocratic, Dexamethasone as internal standard and a range of quantification from 0,1 to 10 μg/ ml. Results: The times of retention were 4,93 min and 15,71 min for Ciprofloxacin and Dexamethasone respectively, precision and accuracy were More than 95 % and a and elution time per sample was 20 minutes. Conclusions: Was developed and validated a sensitive and accurate analytical methods for Ciprofloxacin determination in serum, It is the sufficiently reproducible to be used in pharmacokinetic studies.
Key words. Chromatography, pharmacokinetic, antibiotic prophylaxis, serum.
Introducción
La ciprofloxacina es una quinolona con actividad bactericida, que se caracteriza por la presencia de fluor en la posición 6 y piperacina en la posición 7 de la molécula (1). Su principal actividad terapéutica al igual que las demás quinolonas, es la inactivación de la DNA girasa (topoisomerasa II), enzima que cataliza la conversión del ADN súper enrollado positivamente en DNA con vueltas súper helicoidales negativas, deteniendo así la replicación celular en procariotas (2), la diferencia estructural de las enzimas involucradas en la síntesis de DNA entre procariotas y eucariotas hace que las quinolonas sean incapaces de alterar o inhibir la replicación de los genes en eucariotas, lo que limita la actividad del fármaco a algunos microorganismos. Estudios in vivo han demostrado que la Ciprofloxacina no tiene actividad genotóxica o carcinogénica y es considerado un fármaco de uso seguro en humanos y otras especies (3), aunque algunos autores consideran que la ciprofloxacina cuando está en altas concentraciones en la orina puede afectar la actividad topoisomerasa II en las células epiteliales vesicales, por lo que podría ser utilizada como terapia anti cáncer en estos tejidos (4). Gracias a su amplio espectro bactericida y su importante capacidad de penetración en diferentes tejidos, la Ciprofloxacina es utilizada en diversos procesos infecciosos causados principalmente por bacterias Gram negativas. Actualmente y debido a la creciente resistencia a los antibióticos de muchos microorganismos Gram negativos la Ciprofloxacina está siendo utilizada en terapias combinadas con otros antibióticos (5).
Diversos métodos han sido reportados para el análisis de Ciprofloxacina en variados fluidos biológicos, como la espectrofotometría posterior a la derivación con iones de cobre basada en la capacidad de las quinolonas para unirse a estos elementos (6), immunoensayo tipo ELISA (7) o la quimioluminiscencia (8) entre otros, sin embargo es la Cromatografía Liquida de Alta Precisión HPLC el método analítico más utilizado, con importantes variaciones en los protocolos de extracción y los sistemas de detección, incluidos fluorescencia (9,10) HPLC unido a espectrometría de masas (11), o ultravioleta (12,13). En este estudio hemos desarrollado un método rápido y sencillo para la determinación de Ciprofloxacina en muestras de suero con detección ultravioleta a 280 nm, fase móvil isocrática y Dexametasona como estándar interno para ser utilizado en estudios farmacocinéticos.
Materiales y métodos
Se desarrolló y valido un método analítico para la determinación de Ciprofloxacina en suero mediante la técnica HPLC con detección ultravioleta, utilizando suero de 10 voluntarios sanos en edades comprendidas entre 20 y 45 años de ambos sexos, quienes manifestaron no estar tomando ningún medicamento. Estos sueros fueron analizados con el método desarrollado pre y posteriormente a la adición de cantidades exactas de Ciprofloxacina. Las variables analizadas respecto al medicamento fueron: Especificidad, capacidad de recuperación, exactitud, linealidad, precisión y estabilidad.
Sistema cromatográfico: Se utilizó el equipo de HPLC LaChrom Elite dotado de: Bomba L2130, Inyector L2200, Detector UV L2400, Columna Hypersil GOLD C8 250 x 4,6 y 5 µ. con una fase móvil isocrática que consiste en Acido fosfórico H3PO4 0,25 M (16,85 ml/L de Acido fosfórico 85% d= 1,71 g/ml grado analítico de Merck en H2O grado HPLC de Honey Well) modificado con acetonitrilo grado HPLC de J.T. Baker en una proporción 75:25 v/v. a un flujo constante de 0,7 ml por minuto, el tiempo total de elusión por muestra fué de 20 minutos a temperatura ambiente
Reactivos y soluciones de trabajo: Se preparó una solución inicial con 118,42 mg de Ciprofloxacina clorhidrato estándar secundario de un laboratorio farmacéutico comercial, lote FPCPF100711 con humedad 6,54%, disueltos en un volumen final de 10 ml de Metanol grado HPLC y H2O en una proporción 1:10 v/v, para obtener una solución de concentración 10 mg/ml de Ciprofloxacina, a partir de esta solución se obtuvo un Stock de concentración 1mg/ml en igual diluyente, ambas soluciones se almacenaron a 4ºC por un periodo no mayor a 8 días. Como estándar interno se utilizo una solución de 1mg/ml de Dexametasona en H2O a partir de Dexametasona en la presentación comercial de 4mg/ml laboratorios Pharmayect, esta solución se almaceno en iguales condiciones.
Preparación de las muestras y curvas de calibración: A 10 voluntarios sanos quienes manifestaron no estar tomando ningún medicamento y previa firma del consentimiento informado, se tomo una muestra de sangre (tres tubos sin anticoagulante), las muestras fueron centrifugadas a 2600 g durante 10 minutos y 6 ml de suero fueron extraídos y almacenados inmediatamente a -20°C. Cada muestra de suero fué procesada como se describe a continuación y se analizó mediante HPLC para verificar la ausencia de picos de interferencia que afectaran las determinaciones de interés, finalmente se realizó un pool de sueros que fué almacenado a -20ºC hasta su uso.
Las muestras fueron procesadas de acuerdo al siguiente protocolo: en un tubo eppendorf de 1,5 ml se colocaron 0,2 ml de suero, 20 µl de Dexametasona de 1 mg/ml como estándar interno y 300 µl de acetonitrilo grado HPLC, se mezclo en vortex por 5 minutos y se centrifugo a 14000 g durante 10 minutos, 150 µl del sobrenadante fueron colocados en un vial para HPLC dotado con inserto de 200 µl y 30 µl fueron inyectados en el HPLC. La curva de calibración se realizó haciendo sueros control a partir del pool de sueros adicionando concentraciones de Ciprofloxacina en un rango entre 0,1 a 10 µg ml-1 (0.1, 0.5, 1.0, 4.0, 6.0 y 10 µg ml-1) a partir de la solución stock de 1mg/ml de Ciprofloxacina. Igualmente sueros control con concentraciones de Ciprofloxacina de 10, 4 y 0,1 µg ml-1 fueron preparados para determinar los parámetros necesarios para la validación del método analítico de acuerdo a los parámetros establecidos por la Oficina de las Naciones Unidas para tal fin 13,14 así:
Especificidad: Fué determinada analizando sueros provenientes de los voluntarios sanos para verificar la ausencia en el cromatograma de picos interferentes con el analito de interés, posteriormente estos sueros fueron adicionados con Ciprofloxacina a concentraciones de 0,1 y 10 µg/ml y Dexametasona 20 µl por muestra y nuevamente analizados. Se verifico que no existieran interferencias cruzadas entre la Ciprofloxacina y la Dexametasona.
Capacidad de recuperación: Soluciones de Ciprofloxacina de 0,1 y 10 µg/ml y sueros de donantes sanos con las mismas concentraciones procesados como muestra, fueron analizados por triplicado. La eficiencia de la extracción se calculó comparando las áreas obtenidas en los picos de los cromatogramas para la ciprofloxacina, cuando fueron analizadas muestras posteriormente al proceso de extracción y soluciones de Ciprofloxacina con igual concentración del analito.
Linealidad del sistema: Sueros de donantes sanos adicionados de Ciprofloxacina en concentración final de 0.1, 0.5, 1, 4, 6 y 10 µg/ml fueron analizadas por triplicado y realizada una curva de calibración.
Precisión y exactitud: Sueros con concentraciones de Ciprofloxacina de 0.1, 4 y 10 µg/ml fueron analizadas por triplicado y durante dos días diferentes para evaluar la repetitividad y reproducibilidad del sistema. Respecto al estándar interno, Dexametasona del cual fueron colocados 20 µl en cada muestra a una concentración de 1 mg/ml, se determinó el coeficiente de variación de los valores del área obtenida en todas muestras analizadas.
Estabilidad de los analitos: Se evaluó por triplicado en soluciones de Ciprofloxacina y en sueros control a concentraciones de 1, 4 y 10 µg/ml analizados antes y después de ser sometidos a periodos de congelación a -20ºC, descongeladas y evaluadas a las 24 y 72 horas de permanecer a temperatura ambiente en el automuestreador.
Análisis estadísticos: Para cada una de las variables a analizar se calculó a partir de los valores obtenidos en las mediciones, el promedio, la desviación estándar, coeficiente de variación y porcentaje de error.
Resultados
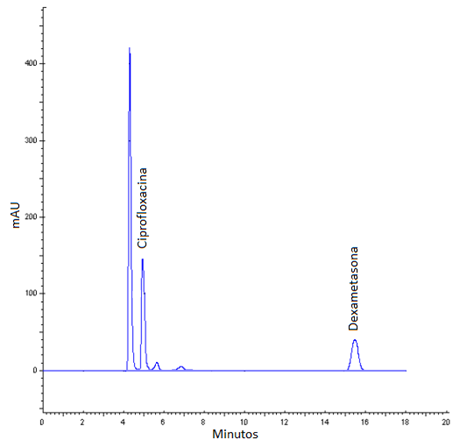
La especificidad es la capacidad del método para diferenciar el analito en presencia de otros componentes de la muestra, en los cromatogramas obtenidos con muestras adicionadas con los analitos de interés se observó la aparición de dos picos a 4,93 min y 15,71 min correspondientes a Ciprofloxacina y Dexametasona respectivamente (Figura 1). Estos picos estaban ausentes cuando muestras de sueros solos fueron analizadas.

Figura 1. Cromatograma de Ciprofloxacina 4,93 minutos (10 µg/ml) y Dexametasona 15,71minutos, se observa además un pico a 4,32 min correspondiente a la muestra de suero.
Respecto a la linealidad, los resultados del modelo lineal indican la correlación existente entre la concentración y la medida del área de los picos obtenidas en muestras de suero con los analitos, en la curva de calibración (figura 2), se obtuvo un R2 estadístico de 0,999 y en ningún caso el coeficiente de variación fué superior a 1% lo cual indica que hay muy poca dispersión entre las mediciones de una misma concentración (tabla 1).
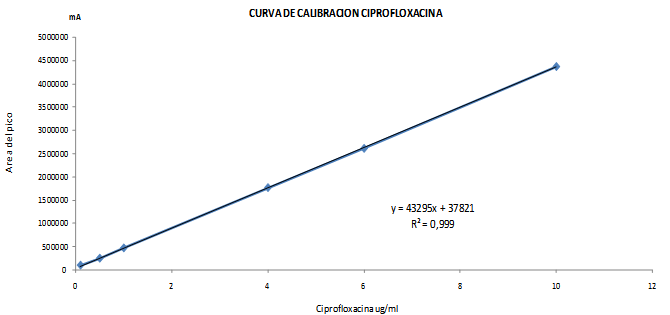
Figura 2. Curva de calibración de Ciprofloxacina con un rango de cuantificación entre 0,1 y 10 µg/ml
Tabla 1. Resultados del estudio de linealidad de los valores obtenidos de Ciprofloxacina en un rango entre 0,1 y 10 µg/ml.
|
|
|
|
|
Ciprofloxacina µg/ml |
Área del |
Promedio |
Desviación estándar |
Coeficiente variación % |
10 |
4423598 |
4379800 |
||
4371040 |
40141,530 |
0,91652 |
||
4344762 |
||||
6 |
2638745 |
2615208 |
|
|
2607362 |
20757,570 |
0,79373 |
||
2599517 |
||||
4 |
1780503 |
1769884 |
|
|
1764574 |
9196,587 |
0,51962 |
||
1764574 |
||||
1 |
473144 |
468924 |
|
|
467517 |
3721,969 |
0,79373 |
||
466110 |
||||
0,5 |
249340 |
247116 |
|
|
246128 |
2012,643 |
0,81445 |
||
245633 |
||||
0,1 |
98424 |
97740 |
|
|
97447 |
594,529 |
0,60828 |
||
97349 |
|
|
||
|
La eficiencia de la extracción se calculó mediante la comparación de las áreas obtenidas en los cromatogramas de las muestras extraídas y las soluciones no extraídas, observándose que a una concentración de Ciprofloxacina de 10 µg/ml la recuperación es de 98,6% y a la concentración de 0,1 µg/ml es de 99,8%, el coeficiente de variación de las replicas en cada caso es inferior a 0,1% (tabla 2), demostrándose una adecuada capacidad de recuperación del analito durante el procesamiento de las muestras.
Tabla 2. Capacidad de recuperación de Ciprofloxacina en el proceso de extracción del suero.
|
|
|
|
|
|
Ciprofloxacina µg/ml |
Área del pico de Ciprofloxacina en solución |
Área del pico de Ciprofloxacina en suero |
% recuperación |
Promedio |
Coeficiente variación % |
10 |
4417895 |
4423598 |
100,129 |
|
|
4501236 |
4371040 |
97,108 |
98,610 |
1,532 |
|
4406753 |
4344762 |
98,593 |
|
|
|
0,1 |
98153 |
98424 |
100,276 |
|
|
98013 |
97447 |
99,422 |
99,894 |
0,434 |
|
97365 |
97349 |
99,984 |
|
|
|
La precisión de las mediciones en las concentraciones analizadas siempre tuvo un coeficiente de variación inferior a 1,5%, respecto a la exactitud el porcentaje de error de las mediciones nunca fué superior a 5% (Tabla 3). El coeficiente de variación obtenido de los valores de las áreas del estándar interno Dexametasona fué de 4,8%.
Los análisis de estabilidad muestran que la ciprofloxacina en una muestra de suero es estable a la congelación y descongelación en los periodos analizados, cuando soluciones de ciprofloxacina fueron dejadas en el automuestreador por más de 24 horas a temperatura ambiente se observó que sufren concentración de la muestra (en promedio 5%) por evaporación del diluyente, por esta razón las muestras fueron analizadas en periodos cortos de tiempo después de su preparación.
Tabla 3. Resultados de la determinación de Ciprofloxacina en diferentes días.
|
|
|
|
|
|
Ciprofloxacina µg/ml |
Día de análisis |
Área del pico |
Concentración Ciprofloxacina µg/ml |
Coeficiente de variación % |
% error |
10 |
Día 1 |
4423598 |
10,100 |
0,594 |
4,164 |
4371040 |
9,980 |
||||
4344762 |
9,920 |
||||
Día 5 |
4379867 |
10,000 |
|||
4390034 |
10,023 |
||||
4391546 |
10,027 |
||||
4 |
Día 1 |
1780503 |
4,024 |
1,164 |
3,165 |
1764574 |
3,988 |
||||
1764574 |
3,988 |
||||
Día 5 |
1780789 |
4,025 |
|||
1763480 |
3,986 |
||||
1724574 |
3,898 |
||||
0,1 |
Día 1 |
98424 |
0,101 |
1,506 |
0,120 |
97447 |
0,100 |
||||
97349 |
0,100 |
||||
Día 5 |
99445 |
0,102 |
|||
97008 |
0,099 |
||||
95075 |
0,097 |
Discusión
Diferentes metodologías han sido reportadas para la determinación de Ciprofloxacina en variados fluidos biológicos (15,16) con importantes diferencias en los métodos de detección y en los protocolos de extracción y procesamiento de las muestras. En los protocolos comúnmente utilizados se utiliza un paso inicial de precipitación de proteínas seguido de la extracción en fase orgánica del analito, evaporación y resuspensión de la muestra en la fase móvil. Khan y colaboradores por ejemplo, emplean ácido fosfórico como precipitante de proteínas y acetonitrilo en la extracción de la Ciprofloxacina (13). El acetonitrilo puede también ser utilizado en un solo paso como precipitante de proteínas y extractor del fármaco, método que ha sido implementado por Kamberi con un paso final de evaporación del solvente y resuspención de la muestra en la fase móvil (17,18). Protocolos más sencillos que utilizan un solo paso para desproteinización y extracción eliminando el proceso de evaporación han sido diseñados con el uso de ácido perclórico al 6% obteniendo buenos resultados (19). El método que reportamos en este trabajo consiste en adicionar a 200 µl de muestra 300 µl de acetonitrilo, agitar cinco minutos en vortex centrifugar diez minutos a 14000 rpm e inyectar directamente en el HPLC 30 µl. Con este método se obtiene un extracto libre de interferencias en los tiempos de retención de los analitos de interés, con una buena recuperación del fármaco, estabilidad del analito aceptable y un rango de cuantificación de 0,1 a 10 µg/ml el cual se encuentra dentro de los limites deseables para estudios farmacocinéticos, tiene además mínimos requerimientos en tiempo, reactivos y equipos. Debido a la volatilidad del acetonitrilo se debe procurar la inyección de la muestra en el HPLC al menor tiempo posible, aunque los resultados de los estudios de estabilidad muestran que después de 24 horas a temperatura ambiente la muestra debidamente tapada en su vial de inyección dentro del automuestreador, solo se ha concentrado en un 5%. La Dexametasona es un corticosteroide sintético de formula química 9-fluoro-11b, 17-dihidroxi-16a-metil 21(fosfonoxi) pregna-1,4-diene-3,20-diona y fórmula empírica es C22H28FNa2O8P con actividad antiinflamatoria e inmunosupresora (20). Respecto al uso de como estándar interno, se observó que es un fármaco lo suficientemente estable en las condiciones analíticas utilizadas y que tiene un tiempo de retención que no permite interferencias con la Ciprofloxacina, aunque podrían probarse otras sustancias con un tiempo de retención menor que permitan disminuir el tiempo total de elusión por muestra.
Los resultados de este estudio nos permiten concluir que el método analítico evaluado para la determinación de Ciprofloxacina en sangre utilizando como estándar interno Dexametasona que fué evaluado respecto a su especificidad, límite de detección, precisión, exactitud, linealidad, capacidad de recuperación, y estabilidad, cumple con los parámetros internacionales de validación de métodos cuantitativos para el análisis de fármacos y puede por lo tanto ser implementado para en estudios farmacocinéticos.
Conflictos de interés: No hay conflicto de intereses entre los que participaron en la realización del estudio.
Fuentes de Financiación: Universidad Metropolitana de Barranquilla y Laboratorio de Toxicología Vargas Melo.
Literatura Citada
![]()