 Artículo de Investigación
Artículo de Investigación Artículo de Investigación
Artículo de Investigación1 Profesor. Programa de Medicina, Facultad de Ciencias de la Salud Grupo de investigación GIMMEIN. Universidad Libre, Seccional Cali, Colombia. ORCID: 0000-0001-9996-3744. Correo e: monikchavez@gmail.com
2 Médico. Programa de Medicina. Facultad de Salud, Universidad Santiago de Cali. Cali, Colombia. ORCID: 0000-0002-7674-0035. Correo e: lisleca14@gmail.com
3 Médico. Programa de Medicina. Facultad de Salud, Universidad Santiago de Cali. Cali, Colombia. ORCID: 0000-0002-4560-6474. Correo e.: Melissa.garcia01@usc.edu.co
Archivos de Medicina (Manizales) Volumen 20 N° 1, Enero-Junio 2020, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874, Chávez Vivas M., Lectamo Caicedo L., García Puerta M.
Recibido para publicación: 07-08-2019 - Versión corregida: 11-12-2019 - Aprobado para publicación: 14-12-2019
Chávez-Vivas M, Lectamo-Caicedo L, García-Puerta M. Niveles plasmáticos de la interlucina-1 β (IL-1β) en pacientes con diagnóstico de sepsis y choque séptico en la unidad de cuidados intensivos de una clínica en la ciudad de Cali (Colombia). Arch Med (Manizales) 2020; 20(1):23-2. DOI: https://doi.org/10.30554/archmed.20.1.3442.2020
Objetivo: el objetivo del presente estudio fue evaluar los niveles plasmáticos de IL-1β como biomarcador de sepsis bacteriana en pacientes de una clínica de la ciudad de Cali. Materiales y métodos: se realizó un estudio prospectivo en 62 pacientes con sepsis y 20 adultos sanos como control, empleando la técnica de ELISA para medir los niveles plasmáticos de las citocinas. Un análisis de regresión logística se utilizó para estimar Odds Ratio (OR), expresado con su 95% intervalos de confianza (IC del 95%) para el resultado de la sepsis en relación a los niveles de IL-1β. La prueba de Chi-cuadrado y la U de Mann-Whitney se emplearon cuando correspondió, valores de p<0,05, fueron considerados significativos y se empleó el paquete estadístico SPSS. Vs 23.00. Resultados: la edad promedio de los pacientes fue de 53 años y de estancia en la UCI de 7,00 días, 59,7% de ellos eran hombres. El foco pulmonar (43,5%), la hipertensión arterial (41,9%) y bacterias Gram negativas (59,7%) fueron los más prevalentes con una mortalidad del 16,1%. Los altos niveles de IL-1β se asoció al desarrollo de choque séptico (OR=28,050; IC95%5,512-142,740;p<0,05) y con padecer insuficiencia respiratoria (OR=9,009;IC95%:0,013-0,941; p<0,05). Conclusión: este estudio evidenció niveles plasmáticos significativamente altos de la IL-1β durante las primeras 48 horas en pacientes con choque séptico. Los altos niveles de esta citosina se relacionaron con mayor riesgo de desarrollo de choque séptico.
Palabras clave: sepsis, choque séptico, interleucina-1beta, citosinas.
Objective: the objective of the present study was to evaluate plasma levels of IL-1β were evaluated as a biomarker of bacterial sepsis in patients from a clinic in the city of Cali. Materials and methods: a prospective study was conducted a prospective study in 62 patients with sepsis and 20 healthy adults as control, using the ELISA test to measure plasma levels of cytokines. The analysis of the odds ratio (OR), expressed with its 95% confidence intervals (95% CI) for the outcome of sepsis in relation to the levels of IL-1β. The Chi-square test and the Mann-Whitney U test will be applied when appropriate, the p values <0.05, and the statistical data of the SPSS statistical package. Vs 23.00. Results: the average age of the patients were 53 years and they were in the ICU of 7.00 days, 59.7% of them were men. The pulmonary focus (43.5%), arterial hypertension (41.9%) and Gram negative bacteria (59.7%) were the most prevalent with a mortality of 16.1%. The high levels of IL-1β were associated with the development of septic shock (OR = 28,050, 95% CI 5,512-142,740, p<0.05) and with respiratory failure (OR = 9,009, 95% CI: 0.013-0.941, p<0.05. Conclusion: this study evidenced significantly high levels of IL-1β during the first 48 hours in patients with septic shock. High levels of this cytokine were associated with increased risk of septic shock development.
Keywords: sepsis, septic shock, interleukin-1beta, cytokines.
La sepsis es una enfermedad que frecuentemente se reporta en las unidades de cuidados intensivo (UCI), siendo la primera causa de muertes en estas secciones hospitalarias [1-5].
La enfermedad se encuentra modulada por una serie de citocinas, receptores y moléculas efectoras que desencadenan la respuesta inflamatoria sistémica [6,7]. La severidad de la sepsis se encuentra relacionada con la forma como estas moléculas desencadenan la respuesta inflamatoria [6].
Varios estudios han asociado la función de las formas de la citocina proinflamatoria interlucina 1 (IL-1): IL-1 α, IL-1 β y el antagonista del receptor de IL-1 (IL-1Ra) como predictores del desarrollo de la sepsis [8-14].
En el caso específico de la IL-1β se ha establecido que es capaz de inducir varios de los síntomas del choque séptico y disfunción multiorgánica [10]. Algunos estudios señalan que el incremento de los niveles plasmáticos de IL-1β se relaciona directamente con el desarrollo de sepsis, falla multiorgánica y la muerte de los pacientes con sepsis [10-14].
La IL-1β juega entonces un importante papel en la evolución de las sepsis, especialmente como indicador temprano del estado inflamatorio del paciente [10,11]. Los altos niveles plasmáticos de la citocina en los pacientes que desarrollan sepsis, es considerado por algunos investigadores mal pronóstico de la enfermedad [10,11,14].
En Colombia, el estudio realizado por Mejía et al., determinaron en el gen que codifica para la caspasa-12 (csp-12) un polimorfismo (125T>C) en la población afroamericana y lo asociaron con mayor susceptibilidad a sepsis grave que las poblaciones mestizas [15]. Sin embargo, faltan más estudios que logren identificar los componentes inflamatorios que puedan ser biomarcadores de sepsis en la población colombiana. El objetivo de este estudio fue establecer el papel biomarcador de la IL-1 β en pacientes con diagnóstico de sepsis y choque séptico en la UCI de la clínica Versalles de la ciudad de Cali.
Pacientes y controles: se realizó un estudio prospectivo que incluyó a 62 pacientes con diagnóstico de sepsis bacteriana entre marzo y noviembre de 2017. El diagnóstico de sepsis se definió con al menos dos criterios considerados como fallas orgánicas: con la escala SOFA (evaluación secuencial de falla orgánica) en el momento del ingreso y diariamente durante su estancia en la UCI según los criterios actuales definidos en el tercer consenso de sepsis [16].
La disfunción de los sistemas orgánicos se definió con los siguientes criterios: disfunción renal: creatinina sérica 2,0 mg/dl o producción de orina <0.5 ml/kg por hora a pesar de la reanimación adecuada con líquidos; disfunción hepática: bilirrubina sérica> 2,0 gr/dl, o un aumento triple en las aminotransferasas séricas; coagulación intravascular diseminada (DIC): cociente normalizado internacional (INR)>1.2, dímero d elevado, plaquetas <100 000/mm3); insuficiencia respiratoria: una relación PAO2/FiO2 f200; hipotensión: presión arterial sistólica 90 mmHg o la presión arterial media 70 mmHg a pesar de la reanimación adecuada de líquidos y vasopresores; disfunción del sistema nervioso central (SNC): alteración aguda del estado mental.
El grupo de control estuvo compuesto por 20 pacientes con hemocultivos negativos, que no cumplían con los criterios de sepsis y que firmaron el consentimiento informado.
Las variables medidas en escala nominal del estudio fueron el sexo, el agente etiológico informado, el tratamiento con antibióticos, la fecha de ingreso, la fecha de alta, comorbilidades (hipertensión arterial, enfermedad pulmonar obstructiva crónica [EPOC], Diabetes Mellitus tipo 2 [DM tipo 2], cáncer, enfermedad cardiovascular, enfermedad del hígado, enfermedad neurológica y enfermedad renal crónica), los parámetros físicos (presión arterial, temperatura, frecuencia cardíaca, etc.), el recuento celular (hematocrito, recuento de leucocitos) y todos los parámetros incluidos en la escala qSOFA se analizaron con distribución de frecuencia y porcentajes.
La edad del paciente, los días de estancia hospitalaria y los niveles plasmáticos de IL-1β en el momento de la admisión y a las 48 horas en la Unidad de Cuidados Intensivos (UCI) de la clínica se analizaron como variables medidas en escala numérica.
Recolección de muestras: para determinar los niveles plasmáticos de IL-1β, se extrajo 5 ml de sangre venosa en tubos con EDTA cómo anticoagulante. Las muestras fueron centrifugadas por 15 minutos a 1000g a 28oC, para llevar a cabo el inmuno-ensayo con el sobrenadante.
Determinación de los niveles de IL-1β por ELISA: la medición de los niveles de IL-1β se realizó por medio del inmuno ensayo enzimático usando el kit-Human IL-1β (Elabscience Biotechnology Inc. USA). El rango de detección fue de 7,8 –500pg/ml, con coeficiente de variación menor al 10%. La lectura de la densidad óptica se realizó Spectramax Reader at 450 nm,
Análisis estadístico: los datos descriptivos se expresaron como porcentaje (%) o media ± la desviación estandar (DE). Se comparó la inducibilidad de IL1-β, se consideró los niveles altos y bajos del IL1- β, el tipo de sepsis y se comparó con cada variable medida en escala nominal o numérica empleando la prueba de χ2, con un nivel de significancia de 0,05 en el Pvalor. El análisis de regresión logística también se utilizó para estimar el Odds Ratio (OR), expresado con su 95% Intervalos de confianza (IC 95%) para la susceptibilidad a la enfermedad y el tipo de sepsis resultado en relación con los niveles de la citoquina polimorfismo. Un valor de Pvalor de menos de 0,05 fue considerado estadísticamente significativo, empleado el paquete estadistico SPSS Vs 23 (Chicago, Inc).
Control de sesgos: como criterios de exclusión se consideró una edad menor de 18 años, embarazo, uso terapéutico de citocinas, heparina o trombolíticos, tratamiento con antibióticos antes del ingreso, pacientes con neoplasias terminales, infectados con VIH, trasplantados o que requieren hemodiálisis y diálisis peritoneal, tratamiento de enfermedades malignas o hematológicas y paciente que no sobrevivió más de 24 horas. Todos los análisis se trabajaron con un nivel de confianza del 95% teniéndose en cuenta un nivel de significación p<0,05.
Consideraciones éticas: este estudio fue avalado por el comité científico de ética y bioética de la clínica Versalles (Acta No.2016-17-05) y realizado teniendo en cuenta las normas internacionales contempladas en la Declaración de Helsinki y las normas técnicas, científicas y éticas establecidas en el decreto 008430 de 1993 del Ministerio de Salud y Protección Social de la República de Colombia.
La edad promedio de la población objeto de estudio fue 53 años (DE+19,47). El 40,3% fueron mujeres con un promedio de índice SOFA de 89 (DE+0,945) y 7 días (DE+4,87) de estancia hospitalaria (Tabla 1).
Tabla 1. Características sociodemográficas y nivel promedio de la IL-1β determinada en los pacientes con sepsis y choque séptico hospitalizados en la UCI de la clínica Versalles
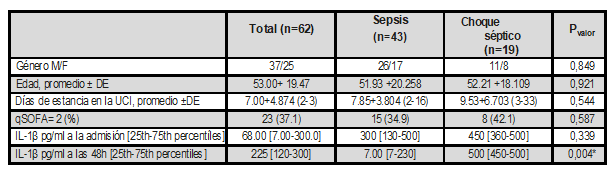
* Pvalor estadísticamente significativo ≤0,05 Fuente: autores.
La Tabla 2 resume las características clínicas de los pacientes en relación a la sobrevida. Durante las primeras 48 horas, el 69,4% de los pacientes fueron diagnosticados con sepsis y 19 pacientes (30,6%) desarrollaron choque séptico. Un total 16,1% de pacientes fallecieron, el 60% de estos pacientes tenían choque séptico (p<0,05).
Tabla 2. Características clínicas de los pacientes hospitalizados en la UCI de la clínica Versalles según la sobrevida del paciente
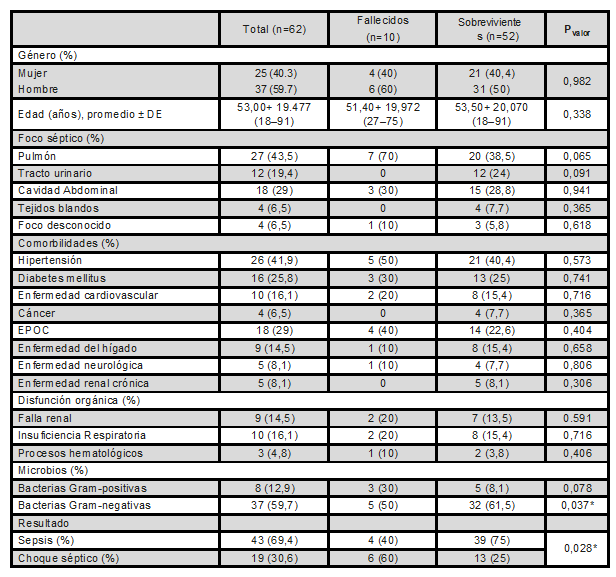
* Pvalor: estadísticamente significativo < 0,05 EPOC: Enfermedad pulmonar obstructiva crónica Fuente: autores.
El foco séptico más reportado fue el pulmón con 43,5%, seguido de cavidad abdominal con 29%.
La hipertensión arterial 41,9% y la falla respiratoria 16,1% fue la comorbilidad y la disfunción orgánica, respectivamente con mayor prevalencia entre los pacientes.
Las bacterias Gram-negativas (59,7%) como principal causante de infecciones entre los pacientes fue significativa (p<0,05).
Al momento de la admisión a la UCI, el nivel promedio de la IL-1β en los pacientes con sepsis fue de 300 pg/ml y en los pacientes que desarrollaron choque séptico de 450 pg/ml. Sin embargo, a las 48 horas, los niveles bajaron a 225 pg/ml en los pacientes con sepsis y aumentaron a 500 pg/ml en los que desarrollaron choque séptico (tabla 1).
El nivel promedio de IL-1β en los pacientes fallecidos fue de 410 pg/ml (255-500) y fue un poco más bajo en los sobrevivientes (390 pg/ml, 250-500). En los pacientes que fallecieron, el nivel de esta citocina permaneció en 410 pg/ml (218-500), mientras que en los sobrevivientes disminuyo a 300 pg/ml (120-445), aunque estas diferencias no fueron significativas (datos no mostrados).
La población control registró un valor promedio de 50,0 pg/ml de IL-1β (20,0-75,0), los valores por encima de este promedio fueron considerados altos en los pacientes con sepsis o choque séptico. Las características clínicas de los pacientes en relación a los niveles de la IL-1β se presentan en la tabla 3.
Tabla 3. Características de los pacientes hospitalizados en la UCI de la clínica Versalles con altos y bajos niveles de IL-1β
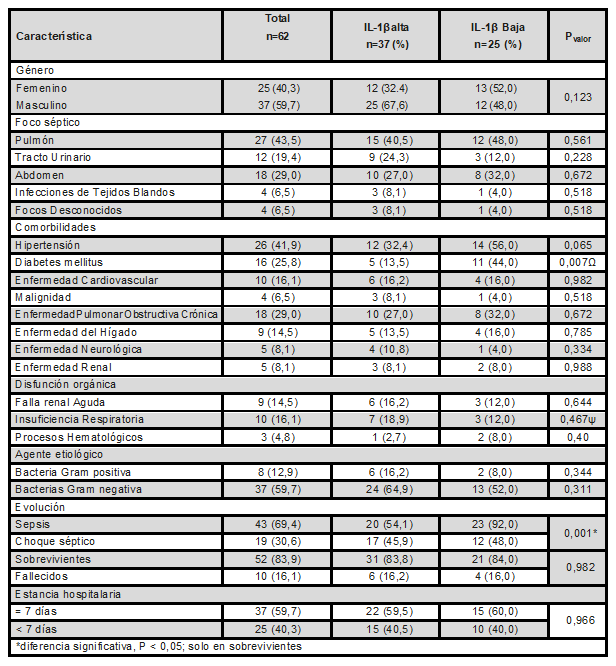
*OR=9,775: IC95%=2,002-47,598; IL1β48hrs OR=28,050;IC95%5,512-142,740;P=0,000 pacientes con choque séptico ψ IL1β48 horas OR=9,009;IC95%:1,061-76,923; P=0,019Ω OR=2,016; IC95% 0,149-1,655.Fuente: autores.
El 13,5% de los pacientes con DM tipo 2 presentaron significativamente altos niveles de IL1β (p<0,05). Según los resultados de este estudio, los pacientes con esta comorbilidad constituyen un mayor riesgo de presentar altos niveles plasmáticos de IL1β (OR=2,016; IC95% 0,149-1,655).
El 45,9% de los pacientes que presentaron niveles altos de IL-1β al momento del ingreso a la UCI, tenían un riesgo 9 veces mayor de desarrollar choque séptico (OR=9,775: IC95%=2,002-47,598; p<0,05). Cuando los niveles de la IL1β permanecieron altos durante las primeras 48 horas, el riesgo se incrementó 28 veces (OR=28,050;IC95%5,512-142,740; p<0,05) como se observa en la tabla 2, estos pacientes también tienen mayor posibilidad de sufrir una insuficiencia respiratoria (18,9%; OR=9,009;IC95%:0,013-0,941; p<0,05).
Como se indica en la Tabla 3, no se encontró relación entre los niveles plasmáticos de IL1β con el género del paciente, la sobrevida, la estancia hospitalaria en UCI, el foco séptico o el agente etiológico.
En este estudio, la edad promedio de los pacientes diagnosticados con sepsis y choque séptico fue 53 años DE+19,261, edad comparable a la reportada por Dougnac et al., en Chile [3]. Sin embargo, los reportes epidemiológicos establecen un promedio mayor a 64 años [3,4,16].
En relación al género, se determinó un ligero predominio de pacientes masculinos con sepsis y choque séptico (59,7%); estos pacientes presentaron mayores niveles plasmáticos de la IL-1β (67,6%) que las mujeres (32,4%), aunque estas diferencias no fueron significativas (p=0,123) y concuerdan con otros estudios que relacionan al hombre con mayor riesgo de desarrollar de sepsis [17-19].
Aunque no existen evidencias que relacionen al género con el desarrollo de la sepsis o la progresión de la enfermedad., algunos investigadores señalan el papel determinante de los estrógenos y andrógenos en la respuesta diferencial en el desarrollo de la sepsis [17-19].
Sin embargo, en otros estudios se ha establecido que la combinación de factores sociales, ambientales, enfermedades subclínicas y la predisposición genética a la enfermedad serían la causa principal en la respuesta inmune del paciente a la infección y probablemente contribuyan a las diferencias observadas entre géneros [10,14,15,20,21].
El pulmón fue el foco séptico más reportado (43,5%) con el mayor número de pacientes fallecidos, seguido de la cavidad abdominal (29%). El estudio realizado en México se reportó al foco abdominal como el más frecuente (47%) seguido del foco pulmonar (33 %) [4]. Estos resultados indican que las infecciones en la cavidad abdominal y el pulmón son susceptibles de complicaciones por lo que se deben prestar mayor atención.
Entre los pacientes sépticos, la hipertensión arterial fue la comorbilidad más frecuente con 41,9% seguido de la EPOC (29%) y DM tipo 2 (25,8%). La literatura señala que estas comorbilidades acentúan el estado crítico del paciente con sepsis debido a que incrementan el daño tisular y el estrés metabólico causándole más debilidad [22-24].
Los pacientes hipertensos presentaron mayor riesgo de mortalidad a causa de la sepsis o choque séptico. Este hecho se debe quizás a la pérdida en la modulación del tono vascular debido al daño endotelial que sufren los pacientes hipertensos, la cual se hace más crítica durante la sepsis, lo que explicaría el mayor riesgo de mortalidad como lo señalan algunas investigaciones [22,25,26].
Se encontró, además, que los pacientes con DM tipo 2 tienen un riesgo dos veces mayor de presentar altos niveles de IL-1β durante las primeras 48 horas de su ingreso a la UCI (OR=2,016; IC95% 0,149-1,655; p<0,05). Esta condición podría estar favorecida quizás por el metabolismo alterado de la glucosa en este grupo de pacientes, lo que contribuye al incremento de la citocina durante la fase aguda de la infección [24,25].
En cuanto a la disfunción orgánica, la más frecuente fue la insuficiencia respiratoria (16,1%), y aquellos pacientes que mantuvieron altos los niveles plasmáticos de IL-1β durante las primeras 48 horas en la UCI presentaron nueve veces más posibilidad de sufrir insuficiencia respiratoria (OR=9,009; IC95%:1,061-76,923; p<0,05).
En la sepsis grave la oxigenación tisular se encuentra disminuida acentuando el cuadro séptico y la mortalidad por insuficiencia orgánica. El fallo respiratorio agudo se debe a las lesiones en las estructuras pulmonares por la falta de oxigenación [27].
El 59,7% lo constituyó aislamientos de bacterias Gram negativas entre los pacientes sépticos. En México se encontró que el 52 % de los aislamientos eran dominados por bacterias Gram negativas, el 38% por Gram positivas y el 10% por hongos [4]. Otros reportes en Colombia, también reportan a las bacterias Gram negativas como las más aisladas [5,28,29]. En este estudio, la mayor prevalencia de bacteria Gram negativas representadas por Escherichia. coli y Klebsiella pneumoniae (22% y 16,4%, respectivamente) se determinó en las muestras clínicas de pacientes fallecidos.
Las bacterias Gram negativas presentan una endotoxina en el lipopolisacárido de la membrana celular externa de la bacteria que es liberado al torrente sanguíneo cuando hay lisis bacteriana, desencadenando la liberación de mediadores inflamatorias que ocasionan vasodilatación periférica, daño endotelial e hipoperfusión [30], llevando a cuadros más graves de sepsis y el choque séptico [31,32].
El 60% de los pacientes fallecidos desarrollaron choque séptico, siendo está condición un riesgo mayor de cuatro veces de mortalidad (OR:4,500; IC95%:1,096-18,474; p<0,05). Estos resultados son coherentes con los datos epidemiológicos que estiman una mortalidad mayor del 33% [1-3].
La mala evolución de la enfermedad resulta evidente en el comportamiento de los niveles plasmáticos de la IL-1β. Los pacientes que desarrollaron choque séptico en las primeras 24 de la admisión a la UCI presentaron los mayores niveles plasmáticos de la IL-1β con un promedio de 450 pg/ml y en las 48 horas siguientes, el promedio de esta citocina siguió aumentando hasta alcanzar 500 pg/ml, lo que evidencia la respuesta inflamatoria alterada en los pacientes con choque séptico.
La presente investigación determinó además que los pacientes que presentaron altos niveles de IL-1β al momento del ingreso a la UCI, tienen 9 veces más posibilidad de desarrollar choque séptico (OR=9,775: IC95%=2,002-47,598); si estos niveles se mantienen altos en las primeras 48 horas, el riesgo aumenta en 28 veces (OR=28,050;IC95%5,512-142,740; p<0,05).
Conclusión
El la presente investigación se encontró una relación directa entre los altos niveles plasmáticos de IL-1β y el desarrollo de choque séptico durante las primeras 48 horas del ingreso del paciente a la UCI; sin embargo, no se estableció relación con la mortalidad.
Es evidente que los pacientes con choque séptico constituyen una población significativamente más grave que el resto de los pacientes críticos. De los factores de riesgo estudiados, esta condición fue el factor de riesgo más significativo, lo cual destaca la magnitud del problema.
Una limitante del estudio lo constituyó el número reducido de pacientes con choque séptico. Se recomienda realizar más estudios, incluido un mayor número de pacientes para establecer si las concentraciones de la citocina podrían usarse como parámetros pronósticos de choque séptico en el futuro.
Conflictos de interés: los autores manifiestan no tener algún conflicto de interés.
Fuentes de financiación: este estudio recibió el apoyo financiero al centro de investigaciones de la Facultad de Ciencias de la Salud [CIFCS-No.2- Investigación con proyección social-2018].
