Ejercicio físico en pacientes con Diálisis
Iván Darío Pinzón Ríos1
Recibido para publicación: 15-05-2019 - Versión corregida: 20-06-2019 - Aprobado para publicación: 16-07-2019
Pinzón-Ríos ID. Ejercicio físico en pacientes con Diálisis. Arch Med (Manizales) 2019; 19(2):267-90. DOI: https://doi.org/10.30554/archmed.19.2.3359.2019
Resumen
Objetivo: realizar un meta-análisis sobre los efectos del ejercicio físico en la rehabilitación funcional del paciente con diálisis. La enfermedad renal crónica es una patología que puede requerir terapia de reemplazo renal (como la diálisis) para su tratamiento, que, sumada a la sintomatología, deteriora la función física de los sujetos. El ejercicio físico como modalidad de intervención del fisioterapeuta, ha mostrado ser efectivo en la mejoría de la funcionalidad y calidad de vida de estos pacientes. Conocer sus beneficios en estos pacientes, puede repercutir positivamente en la salud del paciente y costos del tratamiento a largo plazo. Materiales y Métodos: se incluyeron ensayos clínicos aleatorizados que aplicaron protocolos de ejercicio físico (flexibilidad, resistencia y fuerza) para mejorar variables físicas, fisiológicas y funcionales. Resultados: se analizaron veinte ensayos clínicos bajo los criterios de la Escala PEDro, con puntuación ≥5 calificados como de alta calidad metodológica y bajo riesgo de sesgo. También se analizaron ocho revisiones sistemáticas/meta-análisis bajo lineamientos PRISMA-equidad. Conclusiones: aplicar protocolos de ejercicio físico, tiene efectos positivos clínicamente relevantes en la función física general y calidad de vida de estos pacientes, pero aún no hay consenso respecto a su aplicación en pacientes en diálisis en el contexto colombiano.
Palabras claves: diálisis, ejercicio, terapia física.
Physical exercise in patients with Dialysis
Summary
Objective: to carry out a meta-analysis on the effects of physical exercise in the functional rehabilitation of dialysis patients. Chronic kidney disease is a pathology that may require renal replacement therapy (such as dialysis) for its treatment, which, added to the symptoms, deteriorates the physical function of the subjects. Physical exercise as an intervention modality of the physiotherapist, has been shown to be effective in improving the functionality and quality of life of patients. Knowing their benefits in these patients can have a positive impact on the patient’s health and long-term treatment costs. Materials and Methods: randomized clinical trials were included that applied protocols of physical exercise (flexibility, resistance and strength) to improve physical, physiological and functional variables. Results: twenty clinical trials were analyzed under the criteria of the PEDro Scale, with a score ≥5 rated as having high methodological quality and low risk of bias. Eight systematic reviews / meta-analyzes were analyzed under PRISMA-equity guidelines. Conclusions: to apply protocols of physical exercise, has clinically relevant positive effects on the general physical function and quality of life of these patients, but there is still no consensus regarding its application in dialysis patients in the Colombian context.
Key Words: dialysis, exercise, physical therapy specialty.
Introducción
La enfermedad renal crónica (ERC) representa un problema de salud pública y los estudios epidemiológicos muestran millones de sujetos sometidos a terapia de reemplazo renal (TRR) (cerca al 10% de la población mundial), como única opción de tratamiento [1]. Según la Organización Mundial de la Salud y la Sociedad Latinoamericana de Nefrología e Hipertensión, la ERC es una compleja interacción de procesos patológicos, que pueden desencadenar en insuficiencia renal crónica (IRC) [2]. La IRC es una nefropatía persistente mayor a tres meses con reducción progresiva e irreversible del número de nefronas capaces de realizar funciones depurativas, excretoras, reguladoras y endocrino-metabólicas; que lleva a la pérdida permanente de la tasa de filtración glomerular debida a la reducción del aclaramiento de creatinina <60 ml/min/1,73 m2 [3].
Según reporte del Sistema de Datos Renales de Estados Unidos, 350.000 personas reciben TRR de las cuales el 72% están en diálisis y 28% son sometidos a trasplante renal [4], todas íntimamente ligadas a enfermedades cardiovasculares y diabetes miellitus [5,6]. En los últimos años ha aumentado el número de nuevos casos que requieren TRR y se estima para el año 2030, los casos a nivel mundial que la requerirán, se duplicarán con respecto al año 2010, llegando a 5,5 millones de sujetos. En latinoamérica, la prevalencia de pacientes con TRR aumentó de 119 pacientes por millón de habitantes en 1991 a 660 en el año 2010 [7]. En Colombia, cerca de 21.000 pacientes están en terapia de diálisis y la prevalencia es de 510 pacientes por millón de habitantes [8]. También se reporta que el 28% de la población diabética y entre el 21-36% de la población hipertensa desarrollan ERC, sumado a esto, los pacientes con ERC estadios 1 a 4 tienen mayor prevalencia de enfermedad coronaria, falla cardíaca y factores de riesgo cardiovasculares. El porcentaje de pacientes con ERC que mueren por ECV es mayor que el de aquellos que progresan a un estadio de ERC que requiera TRR [5].
La carga de la enfermedad renal varía sustancialmente a lo largo del planeta, al igual que su detección y tratamiento. A pesar que la magnitud y el impacto de la enfermedad renal está mejor definida en los países desarrollados, evidencia reciente sugiere que los países en desarrollo tienen una carga de la enfermedad similar o incluso mayor que los primeros. En muchos escenarios, las tasas de enfermedad renal y la provisión de su cuidado están definidas por factores socioeconómicos, culturales y políticos, aún en países desarrollados. Estas disparidades existen a lo largo de todo el espectro de la enfermedad renal–desde los esfuerzos preventivos para limitar el desarrollo de la lesión renal aguda (LRA) o de la ERC [9].
En el caso colombiano, la complejidad del manejo deriva de varios factores interrelacionados: 1) su complejidad clínica y psicosocial (largos, complejos y costosos tratamientos); 2) en el sistema de salud del país (se ha manejado dentro de un modelo individual y biomédico que desestima la promoción de la salud y la prevención de la enfermedad); 3) la política incentiva la compensación económica a las EPS según la atención del alto costo, en lugar de propender por resultados en términos de salud y procesos preventivos; 4) importantes fallas para lograr el diagnóstico y la atención oportuna, aumentando el riesgo de progresión y mayor carga de enfermedad; y 5) el debilitamiento de la función rectora de la autoridad sanitaria, que permite altos costos de medicamentos e insumos [5]. Todos estos factores, pueden comprometer la calidad de vida de los pacientes con repercusiones negativas en su funcionalidad.
Por ello, es relevante conocer e intervenir los efectos derivados del tratamiento, que afectan la calidad de vida de estos pacientes. Los efectos de la TRR repercuten negativamente en la función física del sujeto, destacándose: la atrofia muscular (disminución de la síntesis y/o aumento de la degradación de la proteína muscular), pérdida de aminoácidos, inflamación crónica, inactividad física, malnutrición, baja perfusión capilar, neuropatía periférica [7], anemia y cansancio extremo; osteodistrofia renal (adelgazamiento/debilidad o malformaciones óseas); trastornos del sueño; amiloidisis asociada a la diálisis (proteínas sanguíneas que se depositan en articulaciones y tendones causando dolor, rigidez e inflamación), prurito y el “síndrome de las piernas inquietas” [10].
Dentro de las acciones que pueden mejorar estos efectos, se encuentra el ejercicio físico dirigido tanto en la sesión de diálisis como en el hogar, los cuales tienen efectos en diferentes marcadores fisiológicos como Kt/V (variable utilizada para cuantificar la adecuación del tratamiento de hemodiálisis y diálisis peritoneal. K - aclaramiento dializador de la urea, t - tiempo de diálisis, V: volumen de distribución de la urea, aproximadamente igual al agua corporal total del paciente), creatinina sérica, urea en sangre, potasio y fósforo [11]. No hay duda de los efectos benéficos del ejercicio físico en la supervivencia y la mejoría de la calidad de vida en los pacientes en la diálisis [12], sin embargo, en los programas de rehabilitación aún existen falencias acerca de su aplicación al igual que la presencia del personal idóneo (como el fisioterapeuta) para realizar su direccionamiento.
Brindar oportunidades de rehabilitación para que los pacientes se ejerciten en su centro de tratamiento tiene varias ventajas en la función física general. La condición esencial es que la unidad y el personal estén comprometidos con el tratamiento no farmacológico tipo ecléctico, donde el ejercicio físico se priorice. Por ello debe integrarse en la anamnesis rutinaria de éstos pacientes, el cuestionarlos acerca de la actividad física/ejercicio que realizan regularmente, [13]. También los programas de ejercicios que incluye una fase de entrenamiento supervisado combinado con ejercicio en el hogar, pueden ser eficaces y seguros en todas las fases de la IRC con TRR [14].
Por ende, la comprensión de los efectos de las modalidades de ejercicio físico en los pacientes con diálisis, puede brindar futuras opciones de tratamiento implementadas por los fisioterapeutas en el contexto nacional. Por tal motivo, este artículo busca revisar la evidencia científica actual de las intervenciones con ejercicio físico en el paciente dializado, sirviendo como punto de partida para la toma de decisiones en la rehabilitación renal integral.
Materiales y métodos
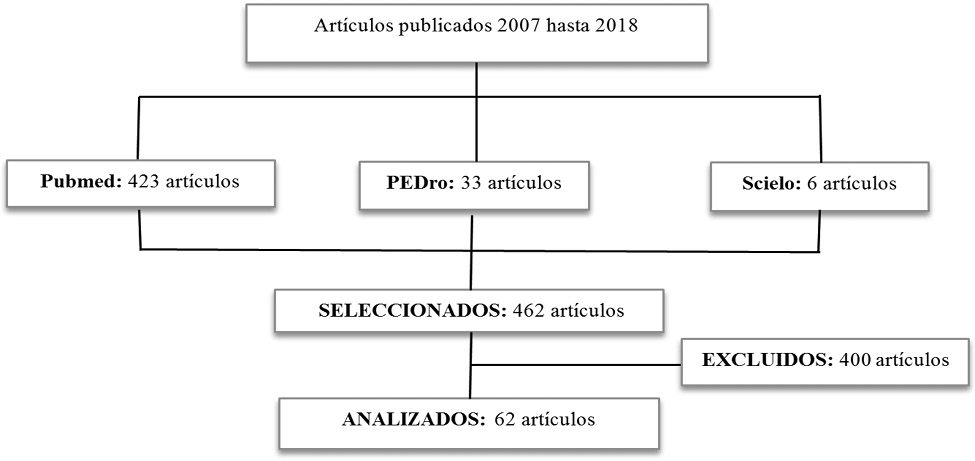
Se realizó un meta-análisis de publicaciones acerca de la efectividad del ejercicio físico en pacientes con diálisis. Se seleccionaron en las bases de datos Pubmed, PEDro y Scielo, utilizando los descriptores MeSH: dialysis, exercise y physical therapy, los cuales se combinaron con los operadores booleanos AND y OR. Como criterios de inclusión de la información se tuvo en cuenta: Ensayos Clínicos Controlados (ECC) en inglés, portugués y español desde 2007 hasta 2018, que evalúan los efectos del ejercicio físico en pacientes dializados. Se encontraron 462 publicaciones: Pubmed (423), PEDro (33) y Scielo (6) y posterior al análisis de títulos/resúmenes, se excluyeron aquellas que no cumplieron los criterios de inclusión o de los cuales no se encontró texto completo (Figura 1). La información se sistematizó en una tabla teniendo en cuenta la población, el tipo de intervención, las variables y los resultados.
La evaluación de la elegibilidad fue realizada por un revisor de manera independiente, estandarizada y no cegada. Para clasificar los ensayos clínicos se utilizó la Escala PEDro (consta de 11 ítems que evalúan la calidad metodológica de los ensayos clínicos aleatorios y controlados dando prioridad a los puntos: la validez interna y la inclusión de datos estadísticos que faciliten la interpretación de resultados) además de una revisión crítica de cada resumen y evaluación del texto completo en el caso de los trabajos cuyo resumen no fuera concluyente [15]. También se analizaron revisiones-sistemáticas/meta-análisis (RS/MA), siguiendo los lineamientos propuestos por la extensión PRISMA-equidad [16]. Finalmente se seleccionaron 20 ECC y 8 RS/MA según las especificaciones iniciales y se complementaron con información impresa o electrónica adicional, para un total de 62 referencia incluidas en este escrito.
Resultados
Se analizaron 20 ECC de acuerdo a los criterios de la Escala PEDro, los cuales se detallan en la tabla 1. Esta escala puntúa la validez externa (criterio 1), validez interna (criterios 2-9) y la suficiente información estadística para interpretar los resultados (criterios 10-11). En general, la literatura muestra buenos criterios, los estudios con puntuación ≥5 son calificados como de alta calidad metodológica y bajo riesgo de sesgo. Se obtuvo puntaciones de 7 para dos artículos, puntuación de 8 para doce artículos y puntación de 9 para seis artículos.
En la tabla 2 se relacionan las características de las intervenciones de ejercicio físico y sus principales resultados en los pacientes con diálisis. Del total de publicaciones, diecisiete dividieron en dos grupos de intervención [17-33] mientras que tres estudios dividieron los participantes en tres grupos [33-36]. Las características de las intervenciones con ejercicio físico mostraron diferentes tipos o modalidades de ejercicio físico prescrita. En trece estudios intervinieron con entrenamiento aeróbico [17-19,22-29,32], cinco aplicaron el entrenamiento de fuerza [21,22,28,32,33], cinco el entrenamiento combinado [19,24,28,29,31] mientras que los programas de flexibilidad fueron ejecutados en dos estudios [22,27]. De todos los estudios, tres entrenaron los músculos respiratorios [32-34] y diecisiete los músculos de las extremidades [17-31,35,36].
Para las variables de los estudios, dieciséis publicaciones midieron la CV como variable principal [17-19,21-28,30,31,36], once evaluaron parámetros de laboratorio (PCR, albumina, RGC) [17-19,22-34,28,30], diez consideraron la fuerza muscular (dinamometría, AST, STS-10) [17,21,22,26,28,29,31,32,34,36], diez midieron capacidad aeróbica (VO2 pico, M6M) [19,21,23,25,26,28,29,31,32,34,], cinco evaluaron nivel de actividad física [22,23,26,27,34], cuatro evaluaron depresión [19,28,30,32], tres midieron función pulmonar/PIM-PEM [32-34] y otros parámetros como personalidad [19], calidad de sueño [23], rigidez arterial [24], flexibilidad [26] y un estudio aplico entrevista y observación [33].
Discusión
La rehabilitación renal involucra el uso de todos los medios destinados a reducir el impacto de las deficiencias, limitaciones en la actividad y restricciones en la participación de los roles, propendiendo en las personas con ERC el logro de sus metas en la reintegración social. El objetivo general de la rehabilitación es permitir a las personas llevar la vida que desearían dada cualquier dificultad impuesta en su proceso de recuperación por impedimentos de una enfermedad o lesión [45]. Este meta-análisis reporta efectos positivos del ejercicio físico en la rehabilitación renal de los pacientes sometidos a diálisis, lo cual incide positivamente en su CV [17-19,21-28,30,31,36,37-44]. El ejercicio físico posee gran cantidad de beneficios para los pacientes en tratamiento dialítico, por ende, su inclusión en los programas de TRR, puede ser una forma económica de ayudar a minimizar problemas asociados en áreas fisiológica, psicológica y social del paciente [46].
En este estudio se encontraron diferentes modalidades de intervenciones con ejercicio físico donde la mayoría de las publicaciones (trece) aplicaron el entrenamiento aeróbico [17-19,22-29,32] mientras que cinco usaron el entrenamiento de fuerza [21,22,28,32,33], por su parte cinco utilizaron el entrenamiento combinado [19,24,28,29,31] y solo dos estudios aplicaron protocolos de flexibilidad [22,27]. Esto muestra la popularidad del entrenamiento aeróbico como método de entrenamiento en dichos programas, con resultados favorables en las variables fisiológicas y funcionales evaluadas. Paradójicamente a estos hallazgos, solo tres publicaciones entrenaron los músculos respiratorios [32-34] y diecisiete los músculos de las extremidades [17-31,35,36], mostrando que hay una mayor intervención de los músculos del esqueleto apendicular en comparación con la musculatura respiratoria. Datos muy semejantes se encontraron en el análisis de las RS/MA, donde los mayores efectos se evidenciaron con el entrenamiento aeróbico en comparación con las demás modalidades de intervención. Todos los estudios mostraron efectos positivos sobre la condición física general y la calidad de vida de los participantes y no reportaron efectos adversos.
Datos similares se encontraron en otras fuentes bibliográficas. Según Molsted, Bjørkman y Lundstrøm en una RS [47], reportaron que los resultados combinados para la salud física autoevaluada y la función física según el SF-36 mejoraron con el entrenamiento de fuerza en pacientes dializados (media 10.05 (2,95-17,14) p=0,006 y media 9,38 (0,79-17,97) p=0,03, respectivamente con IC 95%). Pu et al. [48], reportaron que el ejercicio intra-dialítico promovió el consumo de VO2 máx. que el cuerpo puede usar durante el esfuerzo físico (diferencia de medias (DM) 4,11; IC 95%: 2,94 a 5,27, p <0,0001), además podría reducir significativamente la presión arterial sistólica (DM −4,87; IC 95% −9,20 a –0,55; p=0,03) y la presión arterial diastólica (DM −4.11, IC 95% −6.50 a –1.72, p=0.0007). Adicionalmente Scapini et al. [49], realizaron una RS/MA encontrando que la capacidad aeróbica mejoró significativamente con el entrenamiento aeróbico (3,35 ml/kg/min, IC 95%: 1,79 a 4,91) y entrenamiento combinado (5,00 ml/kg/min, IC 95%: 3,5 a 6,50). Sólo el entrenamiento combinado redujo significativamente la presión arterial sistólica (−9 mmHg, IC 95% −13 a −4) y diastólica (−5 mmHg, 95% IC −6 a −3). Solo el entrenamiento aeróbico fue superior al control para la eficiencia de la hemodiálisis (Kt/V 0,11; IC del 95%: 0,02 a 0,20).
Contrariamente a lo reportado por Pu y Scapini, Thompson et al. [50] realizaron un RS/MA, reportando que el ejercicio no se asoció con un efecto sobre la presión arterial sistólica (DM -4,33 mmHg, IC 95%: -9,04 a 0,38). Sin embargo, la DM después de 12–16 y 24–26 semanas de ejercicio fue significativo (-4,93 mmHg, IC 95%: -8,83 a -1,03 y -10,94 mmHg, IC 95%: -15,83 a -6,05, respectivamente) pero no a las 48–52 semanas (1,07 mmHg, IC 95%: 6,62 a 8,77). En general, el ejercicio no tuvo efecto en la presión arterial ambulatoria de 24 horas (-5,40 mmHg, IC 95%: -12,67 a 1,87) o después de 48–52 semanas (-7,50 mmHg IC 95%: -20,21 a 5,21) mientras que se observó un efecto a las 24 semanas (-18,00 mmHg, IC 95%: -29,92 a -6,08), demostrando que el ejercicio no tuvo un efecto significativo en las medidas de rigidez arterial o función endotelial.
Cabe resaltar que la salud musculoesquelética de los pacientes con ERC, se ve afectada por comorbilidades pueden incluir desnutrición, osteoporosis, disminución de la masa corporal magra y sarcopenia secundaria asociada con limitaciones de movilidad y un riesgo elevado de caídas. En este sentido, los fisioterapeutas están bien posicionados entre el equipo de atención interdisciplinaria para detectar sarcopenia y proporcionar el tratamiento apropiado que pueden afectar el rendimiento funcional gracias a su razonamiento clínico sólido que le permite una mayor comprensión de la condición del paciente, desarrollar una hipótesis de diagnóstico temprano, realizar una examinación minuciosa e implementar las estrategias de intervención, así como a mitigar el riesgo de error de diagnóstico [51]. La Fisioterapia apropiada y oportuna es importante para la evaluación e intervención del riesgo de caídas para minimizar la susceptibilidad a la fractura ósea [52]. Este profesional está reconocido internacionalmente por su capacidad de prescribir y dirigir programas de ejercicio físico en diversas patologías, siguiendo procesos rigurosos de tamizaje de riesgos, evaluación y prescripción del mismo [53].
Las cualidades profesionales que posee le son útiles en los programas de rehabilitación renal, para lograr incidir positivamente en el paciente dializado. Se han reportado efectos específicos de protocolos de intervención fisioterapéutica, mostrando que la implementación de terapia física combinada con terapia respiratoria puede contribuir a la mejora de las variables como la fuerza muscular respiratoria (presión inspiratoria y espiratoria máxima), el flujo espiratorio pico máximo y la fuerza muscular periférica [54,55]. Otra de las opciones de intervención son los programas de realidad virtual, los cuales son utilizados en varias poblaciones como el ictus y parálisis cerebral; logrando mejorar la movilidad, el equilibrio o la velocidad en la marcha. Estos programas consisten en realizar ejercicio moviéndose en un entorno virtualmente reproducido y controlado, siendo buena alternativa para la rehabilitación renal [56]; aunque su principal problema puede ser el costo de los equipos, son una alternativa que ha ganado fuerza en los últimos años.
A pesar de las directrices sobre buena práctica clínica del ejercicio físico, existe un pequeño número de centros que lo aplican y en el caso colombiano, aun se subestima el total de unidades renales que cuentan con dichos profesionales. Los factores que contribuyen a los programas de ejercicios sostenibles son el compromiso profesional de un equipo multidisciplinario. El incentivo y estímulo de todo el personal de diálisis para llevar a cabo ejercicio activo, es contar con espacio físico y equipo adecuados, con individualización para cada paciente. No hay informes sobre lesiones graves como resultado de la participación en el ejercicio, lo cual indica que es hora de incluir la terapia física en el procedimiento de atención habitual de rutina en pacientes en diálisis [57].Según González-Ovando y Vega-Malagón en 2017, la fisioterapia nefrológica mostro una mejoría significativa en la fuerza y resistencia física, gracias al programa de acondicionamiento físico intra-diálisis, el cual también aumentó la capacidad funcional y mejoró el componente de la esfera física de la calidad de vida [58].
Por todo esto, los datos acerca del mejor ejercicio en diálisis aún son controversiales. Indudablemente, la elección del ejercicio físico regular para pacientes con ERC, junto con otros métodos de tratamiento podría ser la mejor forma no farmacológica, que da al paciente una oportunidad de alcanzar un óptimo funcionamiento y nivel psicosocial similar al estado pre mórbido [59]. La aplicación del ejercicio de rehabilitación debe ser segura y enfocada en las posibilidades individuales de cada paciente, y basados en las referencias anteriores, parece ser efectivo combinar el entrenamiento aeróbico y de resistencia para la mejoría del rendimiento funcional [60]. Las implicaciones para la práctica clínica, demuestran que la implementación o indicación de ejercicios aeróbicos tanto pre-dialíticos como intra-dialíticos, con una frecuencia de 2 a 3 veces por semana y una duración de 30 minutos, podría mejorar la rigidez vascular, la presión arterial, la capacidad aeróbica, el metabolismo óseo y eliminación de solutos, lo que se puede considerar como terapia complementaria en la diálisis crónica [46].
A pesar de los avances tecnológicos en el tratamiento de la ERC y del aumento de la supervivencia de estos pacientes, ninguno de los métodos existentes es curativo. Lidiar con la cronicidad de la enfermedad y con las limitaciones derivadas del tratamiento es necesario para los pacientes en TRR y proporciona importante impacto psicológico para estos individuos. El tratamiento de diálisis, en particular, causa una rutina diaria restringida que impone limitaciones al sujeto, afectando aspectos biológicos, psicológicos y sociales. Esto ocasiona una ruptura en su estilo de vida y origina la necesidad de adaptación ante esta nueva condición [61]. Pese a sus casi cuarenta años de historia y mejorías en la persistencia tanto de la técnica como de los pacientes, la diálisis afronta algunas dificultades que contribuyen a la infrautilización: la formación deficiente de especialistas, la falta de infraestructuras, la falta de información a los pacientes, la escasez de consultas de enfermedad renal crónica avanzada o baja financiación de la diálisis [62]. Es así como dichos factores, representan retos a ser superados mediante planes de mejora en el servicio y la calidad de la atención renal, donde el ejercicio puede ser una alternativa de bajo costo que influye positivamente en el estado de salud y evolución en el tratamiento de estos pacientes.
Conclusiones La TRR es un tratamiento que ha proporcionado a los pacientes con IRC, opciones de prolongar la vida mejorando diferentes marcadores fisiológicos y de laboratorio. Específicamente la diálisis es una intervención muy popular en nuestros días que ha ganado amplia aceptación en la comunidad médica. Sin embargo, los efectos subsecuentes de la misma, afectan drásticamente la independencia física funcional de estos sujetos, lo cual incide negativamente en la CV. Es así como la incorporación del ejercicio físico guiado por profesionales idóneos y capacitados como el fisioterapeuta, en los programas de rehabilitación renal, brinda nuevos horizontes en esta población que día a día crece, no sólo por la longevidad característica sino por las enfermedades crónicas concomitantes.
Según la revisión documental realizada, se puede concluir que el ejercicio físico (aeróbico, fuerza, combinado o flexibilidad) posee efectos positivos clínicamente y estadísticamente relevantes en la funcionalidad para la ejecución de las AVD y ABI, lo cual repercute positivamente en la calidad de vida relacionada con la salud de estos pacientes. Estos efectos reportados, se han dado en protocolos de intervención intra-sesión de diálisis al igual que un acompañamiento de actividad física en casa. Todos ellos guiados equipos multidisciplinarios profesionales en la rehabilitación renal a nivel mundial (en los cuales interviene el fisioterapeuta), sin embargo, a nivel nacional aún no hay reportes encontrados en esta revisión.
El ejercicio físico, ha mostrado ser efectivo en el paciente dializado, optimizando variables físicas, funcionales y psicológicas. No obstante, aún hay controversia acerca de su prescripción (existe variación en los protocolos de tratamiento en el tipo, duración, frecuencia, intensidad y progresión del ejercicio), por eso las futuras investigaciones en este campo se deben conducir a dar mayor soporte en estos elementos, así como afianzar la presencia del fisioterapeuta, como el profesional capacitado que combina en su ejercicio profesional los conocimientos en salud con la profundización en el ejercicio físico como modalidad de intervención, con miras a intervenir el movimiento corporal humano como su objeto de estudio, permitiendo una mayor visibilización del fisioterapeuta en los procesos fisioterapéuticos mediante esta modalidad de intervención, logrando mejorar el cuerpo del conocimiento de la Fisioterapia en este campo de acción emergente.
Conflictos de interés: no se declara conflicto de intereses.
Fuentes de financiación: recursos propios del autor.
Literatura citada
Lourenço BS, Nascimento MA, Siqueira VN, Draibe SA, Mello MT, Tufik S, et al. Effects of Intra-Dialysis Resistance Training in Hemodynamic Parameters, Oxidative Stress and Health-Related Quality of Life in Patients with Chronic Kidney Disease. J Clin Nephrol Ren Care 2018; 4:1-7. DOI: 10.23937/2572-3286.1510035
Otero PF, Peña J, Suárez BM, Gonzáles J, Morales LV, Marino C, et al. Situación de la enfermedad renal crónica, la hipertensión arterial y la diabetes mellitus en Colombia 2017. Bogotá D.C.: Fondo Colombiano de Enfermedades de Alto Costo - Cuenta de Alto Costo (CAC); 2018.
Gómez-Carracedo A, Arias-Muñana E, Jiménez-Rojas C. Insuficiencia Renal Crónica En: Abellán Van-Kan G, Abizanda Soler P, Alastuey Giménez C, Albó Poquí A, Alfaro Acha A, Alonso Álvarez M, et al. Tratado de Geriatría para Residentes. Madrid: Sociedad Española de Geriatría y Gerontología; 2006. p. 637-646. Capítulo 62.
Alarcón JC, Lopera JM, Montejo JD, Henao CM, Rendón G. Perfil epidemiológico de pacientes en diálisis, CTRB y RTS sucursal Medellín 2000-2004. Acta Med Colomb 2006; 31:4-12.
Lopera-Medina MM. La enfermedad renal crónica en Colombia: necesidades en salud y respuesta del Sistema General de Seguridad Social en Salud. Rev Gerenc Polít Salud 2016; 15(30):212-233. DOI: 10.11144/Javeriana.rgyps15-30.ercc
Moreno-Collazos JE, Cruz-Bermúdez HF. Ejercicio Físico y Enfermedad Renal Crónica en Hemodiálisis. Rev Nefrol Dial Traspl 2015; 35(3):212-219.
Gómez de la Torre-del Carpio A, Bocanegra-Jesús A, Guinetti-Ortiz K, Mayta-Tristán P, Valdivia-Vega R. Mortalidad precoz en pacientes con enfermedad renal crónica que inician hemodiálisis por urgencia en una población peruana: Incidencia y factores de riesgo. Nefrología 2018; 38(4):425-432. DOI: 10.1016/j.nefro.2017.11.017
Marín-Ballestas GA. Bioética: principios y recomendaciones en la aplicación de diálisis - cuidados paliativos. Rev Colomb Nefrol 2015; 2(2):137-146. DOI: 10.22265/acnef.2.2.212
Crews DC, Bello AK, Saadi G. Burden, access, and disparities in kidney disease. Rev Colomb Nefrol 2019; 6(1): 74-83.
U.S. Department of Health and Human Services - National Institute of Diabetes and Digestive and Kidney Diseases. Treatment Methods for Kidney Failure: Hemodialysis. U.S. Department of Health and Human Services; 2007.
Paluchamy T, Vaidyanathan R. Effectiveness of intradialytic exercise on dialysis adequacy, physiological parameters, biochemical markers and quality of life - A pilot study. Saudi J Kidney Dis Transpl 2018; 29(4): 902-910. DOI: 10.4103/1319-2442.239661
Faria de Moura RM, Ribeiro-Silva FC, Ribeiro GM, Aparecida de Sousa L. Efeitos do exercício físico durante a hemodiálise em individuos com insuficiência renal crônica: uma revisão. Fisioter Pesqui 2008; 15(1):86-91. DOI: 10.1590/S1809-29502008000100014
Howden EJ, Coombes JS, Strand H, Douglas B, Campbell KL, Isbel NM. Exercise Training in CKD: Efficacy, Adherence, and Safety. Am J Kidney Dis 2015; 65(4):583-591. DOI: 10.1053/j.ajkd.2014.09.017
Idier L, Untas A, Koleck M, Chauveau P, Rascle N. Assessment and effects of Therapeutic Patient Education for patients in hemodialysis: a systematic review. Int J Nurs Stud 2011; 48(12):1570-1586. DOI: 10.1016/j.ijnurstu.2011.08.006
Physiotherapy Evidence Database. [Internet] Escala PEDro-Español. Consultado (05 Enero de 2019) Recuperado de: https://www.pedro.org.au/spanish/downloads/pedro-scale/.
Welch V, Petticrew M, Tugwell P, Moher D, O’Neill J, et al. PRISMA-Equity 2012 Extension: Reporting Guidelines for Systematic Reviews with a Focus on Health Equity. PLoS Med 2012; 9(10):1-7. DOI: 10.1371/journal.pmed.1001333
Cheema B, Abas H, Smith B, O’Sullivan A, Chan M, Patwardhan A, Kelly J, et al. Progressive exercise for anabolism in kidney disease (PEAK): a randomized, controlled trial of resistance training during hemodialysis. J Am Soc Nephrol 2007; 18(5):1594-1601.
Matsumoto Y, Furuta A, Furuta S, Miyajima M, Sugino T, Nagata K, Sawada S. The impact of pre-dialytic endurance training on nutritional status and quality of life in stable hemodialysis patients (Sawada study). Ren Fail 2007; 29(5): 587-593.
Ouzouni S, Kouidi E, Sioulis A, Grekas D, Deligiannis A. Effects of intradialytic exercise training on health-related quality of life indices in haemodialysis patients. Clin Rehabil 2009; 23(1):53-63. DOI: 10.1177/0269215508096760
Peña-Amaro P, García-López J, Zagalaz-Sánchez ML, Jimeno-Ucles R, Expósito-Rodríguez A. El ejercicio físico en pacientes en insuficiencia renal crónica terminal y programa de hemodiálisis. Dial Traspl 2009; 30(4):127-132. DOI: 10.1016/S1886-2845(09)72696-7
Segura-Ortí E, Kouidi E, Lisón JF. Effect of resistance exercise during hemodialysis on physical function and quality of life: randomized controlled trial. Clin Nephrol 2009; 71(5):527-537. DOI: 10.5414/cnp71527
Chen JL, Godfrey S, Ng TT, Moorthi R, Liangos O, Ruthazer R, et al. Effect of intra-dialytic, low-intensity strength training on functional capacity in adult haemodialysis patients: a randomized pilot trial. Nephrol Dial Transplant 2010; 25(6):1936-1943. DOI: 10.1093/ndt/gfp739
Afshar R, Emany A, Saremi A, Shavandi N, Sanavi S. Effects of intradialytic aerobic training on sleep quality in hemodialysis patients. Iran J Kidney Dis 2011; 5(2):119-123.
Mustata S, Groeneveld S, Davidson W, Ford G, Kiland K, Manns B. Effects of exercise training on physical impairment, arterial stiffness and health-related quality of life in patients with chronic kidney disease: a pilot study. Int Urol Nephrol 2011; 43(4):1133-1141. DOI: 10.1007/s11255-010-9823-7
Kosmadakis GC, John SG, Clapp EL, Viana JL, Smith AC, Bishop NC, et al. Benefits of regular walking exercise in advanced pre-dialysis chronic kidney disease. Nephrol Dial Transplant 2012; 27(3): 997-1004. DOI: 10.1093/ndt/gfr364
Bohm C, Stewart K, Onyskie-Marcus J, Esliger D, Kriellaars D, Rigatto C. Effects of intradialytic cycling compared with pedometry on physical function in chronic outpatient hemodialysis: a prospective randomized trial. Nephrol Dial Transplant 2014; 29(10): 1947-1955. DOI: 10.1093/ndt/gfu248
Wu Y, He Q, Yin X, He Q, Cao S, Ying G. Effect of individualized exercise during maintenance haemodialysis on exercise capacity and health-related quality of life in patients with uraemia. J Int Med Res 2014; 42(3):718-727. DOI: 10.1177/0300060513509037
Esteve-Simo V, Junqué-Jiménez A, Moreno-Guzmán F, Carneiro-Oliveira J, Fulquet-Nicolas M, Pou-Potau M, et al. Beneficios del ejercicio físico de baja intensidad durante la sesión de hemodiálisis en el paciente anciano. Nefrología 2015; 35(4): 385-394. DOI: 10.1016/j.nefro.2015.03.006
Marchesan M, Krug RR, E Silva JRLC, Barbosa AR, Rombaldi AJ. Physical exercise modifies the functional capacity of elderly patients on hemodialysis. Fisioter mov 2016; 29(2):351-59. DOI: 10.1590/0103-5150.029.002.AO14
Martin-Alemañy G, Valdez-Ortiz R, Olvera-Soto G, Gomez-Guerrero I, Aguire-Esquivel G, Cantu-Quintanilla G, et al. The effects of resistance exercise and oral nutritional supplementation during hemodialysis on indicators of nutritional status and quality of life. Nephrol Dial Transplant 2016; 31(10):1712-1720. DOI: 10.1093/ndt/gfw297
de Lima MC, Cicotoste Cde L, Cardoso Kda S, Forgiarini LA Jr, Monteiro MB, Dias AS. Effect of exercise performed during hemodialysis: strength versus aerobic. Ren Fail 2013; 35(5):697-704. DOI: 10.3109/0886022X.2013.780977
Pellizzaro CO, Thomé FS, Veronese FV. Effect of peripheral and respiratory muscle training on the functional capacity of hemodialysis patients. Ren Fail 2013; 5(2):189-197. DOI: 10.3109/0886022X.2012.745727
Frih B, Jaafar H, Mkacher W, Ben Salah Z, Hammami M, Frih A. The Effect of Interdialytic Combined Resistance and Aerobic Exercise Training on Health Related Outcomes in Chronic Hemodialysis Patients: The Tunisian Randomized Controlled Study. Front Physiol 2017; 8:288. DOI: 10.3389/fphys.2017.00288
Manfredini F, Mallamaci F, D’Arrigo G, Baggetta R, Bolignano D, Torino C, et al. Exercise in Patients on Dialysis: A Multicenter, Randomized Clinical Trial. J Am Soc Nephrol 2017; 28(4):1259-1268. DOI: 10.1681/ASN.2016030378
Marchesan M, Krug RR, Rodrigues-Barbosa A, Rombaldi AJ. Percepção de pacientes em hemodiálise sobre os benefícios e as modificações no comportamento sedentário após a participação em um programa de exercícios físicos. Rev Bras Ciênc Esporte 2017; 39(3):314-321. DOI: 10.1016/j.rbce.2016.01.012
Bennett PN, Fraser S, Barnard R, Haines T, Ockerby C, Street M, et al. Effects of an intradialytic resistance training programme on physical function: a prospective stepped-wedge randomized controlled trial. Nephrol Dial Transplant 2016; 31(8):1302-1309. DOI: 10.1093/ndt/gfv416
Segura-Ortí E. Ejercicio en pacientes en hemodiálisis: revisión sistemática de la literatura. Nefrología 2010; 30(2): 236-246. DOI: 10.3265/Nefrologia.pre2010.Jan.10229
Smart N, Steele M. Exercise training in haemodialysis patients: A systematic review and meta-analysis. Nephrology 2011; 16(2011):626-632. DOI: 10.1111/j.1440-1797.2011.01471.x
Smart N, McFarlane J, Cornelissen V. The Effect of Exercise Therapy on Physical Function, Biochemistry and Dialysis Adequacy in Haemodialysis Patients: A Systematic Review and Meta-Analysis. Open Journal of Nephrology 2013; 3(1):25-36. DOI: 10.4236/ojneph.2013.31005
Heiwe S, Jacobson SH. Exercise training in adults with CKD: a systematic review and meta-analysis. Am J Kidney Dis 2014; 64(3): 383-393. DOI: 10.1053/j.ajkd.2014.03.020
Barcellos FC, Santos IS, Umpierre D, Bohlke M, Hallal PC. Effects of exercise in the whole spectrum of chronic kidney disease: a systematic review. Clin Kidney J 2015; 8(6):753-765. DOI: 10.1093/ckj/sfv099
de Medeiros AIC, Fuzari HKB, Rattesa C, Brandão DC, de Melo Marinho PÉ. Inspiratory muscle training improves respiratory muscle strength, functional capacity and quality of life in patients with chronic kidney disease: a systematic review. J Physiother 2017; 63(2):76-83. DOI: 10.1016/j.jphys.2017.02.016
Matsuzawa R, Hoshi K, Yoneki K, Harada M, Watanabe T, Shimoda T, et al. Exercise Training in Elderly People Undergoing Hemodialysis: A Systematic Review and Meta-analysis. Kidney Int Rep 2017; 2:1096-1110. DOI: 10.1016/j.ekir.2017.06.008
Thangarasa T, Imtiaz R, Hiremath S, Zimmerman D. Physical Activity in Patients Treated with Peritoneal Dialysis: A Systematic Review and Meta-analysis. Can J Kidney Health Dis 2018; 5:1-13. DOI: 10.1177/2054358118779821
Sokunbi G. Exercise and Rehabilitation: Needs for Kidney transplantation. J Physiother Res 2017; 1(1):1-2.
Fernández-Lara MJ, Ibarra-Cornejo JL, Aguas-Alveal EV, González-Tapia CE, Quidequeo-Reffers DG. Revisión: Beneficios del ejercicio físico en pacientes con enfermedad renal crónica en hemodiálisis. Enferm Nefrol 2018; 21 (2):167-181. DOI: 10.4321/s2254-28842018000200008
Molsted S, Bjørkman AD, Lundstrøm LH. Effects of strength training to patients undergoing dialysis: a systematic review. Dan Med J 2019; 66(1):1-9.
Pu J, Jiang Z, Wu W, Li L, Zhang L, Li Y, et al. Efficacy and safety of intradialytic exercise in haemodialysis patients: a systematic review and meta-analysis. BMJ 2019; 9(1):1-12. DOI: 10.1136/bmjopen-2017-020633
Scapini KB, Bohlke M, Moraes OA, Rodrigues CG, Inácio JFS, Sbruzzi G, et al. Combined training is the most effective training modality to improve aerobiccapacity and blood pressure control in people requiring haemodialysis forend-stage renal disease: systematic review and network meta-analysis. J Physiother 2019; 65:4-15. DOI: 10.1016/j.jphys.2018.11.008
Thompson S, Wiebe N, Padwal RS, Gyenes G, Headley SAE, Radhakrishnan J, et al. The effect of exercise on blood pressure in chronic kidney disease: A systematic review and meta-analysis of randomized controlled trials. PLoS ONE 2019; 14(2):1-18. DOI: 10.1371/journal.pone.0211032
Baker SE, Painter EE, Morgan BC, Kaus AL, Petersen EJ, Allen CS, et al. Systematic Clinical Reasoning in Physical Therapy (SCRIPT): Tool for the Purposeful Practice of Clinical Reasoning in Orthopedic Manual Physical Therapy. Phys Ther 2017; 97(1):61-70. DOI: 10.2522/ptj.20150482
Hernandez HJ, Obamwonyi G, Harris-Love MO. Physical Therapy considerations for Chronic Kidney Disease and Secondary Sarcopenia. J Funct Morphol Kinesiol 2018; 3(5):1-8.
Pinzón ID. Rol del fisioterapeuta en la prescripción del ejercicio. Arch Med (Manizales). 2014; 14(1):129-143.
Sostena-Neto JR, Magalhães-Figueiredo e Castro L, Santos de Oliveira F, Silva AM, dos Reis LM, Assunção-Quirino AP, et al. Comparison between two physiotherapy protocols for patients with chronic kidney disease on dialysis. J Phys Ther Sci 2016; 28:1644-1650. DOI: 10.1589/jpts.28.1644
Khanna S, Kaur P, Khanna SK. To Evaluate the effects of Physiotherapy (a Home Based Exercise Program) in Improving Functional Capacities and Quality of Life in Patients with Chronic Kidney Disease. IJPOT 2015; 9(3):77-81. DOI: 10.5958/0973-5674.2015.00100.8
Segura-Ortí E, Pérez-Domínguez B, Ortega-Pérez de Villar L, Meléndez-Oliva E, Martínez-Gramage J, García-Maset R, et al. Virtual reality exercise intradialysis to improve physical function: A feasibility randomized trial. Scand J Med Sci Sports 2019; 29:89-94. DOI: 10.1111/sms.13304
Stolić RV, Mihailović B, Matijašević IR, Jakšić MD. Effects of physiotherapy in patients treated with chronic hemodialysis. Biomedicinska Istraživanja 2018; 9(1):103-111. DOI: 10.7251/BII1801103S
González-Ovando IY, Vega-Malagón G. Fisioterapia Nefrológica: Mejora de la calidad de vida mediante un programa de acondicionamiento físico en pacientes con enfermedad renal crónica en una unidad de hemodiálisis en México. ESJ 2017; 13(24):405-415. DOI: 10.19044/esj.2017.v13n24p405
Mahrova A, Svoboda L, Krížová E, Prajsová J, Dragomirecká E. Quality of life of patients on peritoneal dialysis treatment – Cross sectional study in the Czech Republic. Kontakt 2016; 18:e244-e252. DOI: 10.1016/j.kontakt.2016.10.005
Mahrova A. Physical Activity is a Necessary Part of Care in Patients with Chronic Kidney Disease-Short Historical Overview. Prim Health Care 2017; 7(2):1-6. DOI: 10.4172/2167-1079.1000271
Silva SM, Braido NF, Ottaviani AC, Gesualdo GD, Zazzetta MS, Orlandi FS. Social support of adults and elderly with chronic kidney disease on dialysis. Rev Lat Am Enfermagem 2016; 24:1-7. DOI: 10.1590/1518-8345.0411.2752
Moreiras-Plaza M. De dónde venimos y adónde vamos en diálisis peritoneal: identificando barreras y estrategias de futuro. Nefrología. 2014; 34(6):756-767. DOI: 10.3265/Nefrologia.pre 2014.Sep.12603

1Archivos de Medicina (Manizales) Volumen 19 N° 2, Julio-Diciembre 2019, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874, Pinzón Ríos I.D.
M Sc Ciencias de la Actividad Física y Deporte; Especialista Pedagogía Universitaria, Fisioterapeuta. Universidad Manuela Beltrán. Bucaramanga-Colombia. ORCID: 0000-0002-5949-2930. Correo: ivandpr@hotmail.com