Función renal, niveles urinarios de cadmio y plomo en niños del municipio de Naguanagua (estado Carabobo, Venezuela), expuestos a humo de tabaco ambiental
Aura Palencia 1, Gabriela Romero 2, Angélica Figueredo 3, Omaris Barrades 4, Yoliammy Álvarez 5, Helen Acosta 6, María González 7
1. Magister Scientiarium en Toxicología Analítica. Unidad de Investigación en Toxicología Molecular. Departamento de Investigación y Desarrollo Profesional. Escuela de Bioanálisis, Facultad de Ciencias de la Salud, Universidad de Carabobo, Venezuela. Correo e.: adpalencia@uc.edu.ve. Autor para correspondencia.
2. Magister Scientiarium en Toxicología Analítica. Unidad de Investigación en Toxicología Molecular. Departamento de Ciencias Básicas. Escuela de Bioanálisis, Facultad de Ciencias de la Salud, Universidad de Carabobo, Venezuela. Correo e.: gvromero@uc.edu.ve
3. Licenciada en Bioanálisis. Maestría en Toxicología Analítica, Área de Postgrado, Facultad de Ciencias de la Salud. Universidad de Carabobo, Venezuela. Correo e.: licangeli@hotmail.com
4. Licenciada en Bioanálisis. Universidad de Carabobo, Venezuela. Correo e.: omaris_34@hotmail.com
5. Licenciada en Bioanálisis. Universidad de Carabobo, Venezuela. Correo e.: yoli_292@hotmail.com
6. Licenciada en Bioanálisis. Universidad de Carabobo, Venezuela. Correo e.: arantxa_2564@hotmail.com
7. Licenciada en Bioanálisis. Universidad de Carabobo, Venezuela. Correo e.: m_dla_57@hotmail.com
Archivos de Medicina (Manizales), Volumen 18 N° 2, Julio-Diciembre 2018, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Palencia A., Romero G., Figueredo A., Barrades O., Álvarez Y, Acosta H., González M.
Recibido para publicación: 28-09-2018 - Versión corregida: 23-10-2018 - Aprobado para publicación: 07-11-2018
Palencia A, Romero G, Figueredo A, Barrades O, Alvarez Y, Acosta H, González M. Función renal, niveles urinarios de cadmio y plomo en niños del municipio de Naguanagua (estado Carabobo, Venezuela), expuestos a humo de tabaco ambiental. Arch Med (Manizales) 2018; 18(2):255-69. DOI: https://doi.org/10.30554/archmed.18.2.2769.2018.
Resumen
Objetivo: los metales presentes en las fases gaseosa y particulada del humo del tabaco ambiental, son considerados nefrotóxicos. En esta investigación se evaluó la función renal y niveles urinarios de cadmio y plomo en niños expuestos al humo de tabaco ambiental en una comunidad del municipio Naguanagua (Carabobo, Venezuela). Materiales y métodos: la muestra estuvo conformada por 43 niños (21 expuestos y 22 no expuestos), a quienes se les determinó en orina puntual índices urinarios cadmio/creatinina, plomo/creatinina, albúmina/creatinina, calcio/creatinina, fosfatasa alcalina/creatinina y β-2-microglobulina/creatinina. Resultados: en el grupo expuesto existe una correlación positiva y significativa entre β-2-microglobulina/creatinina y albúmina/creatinina independientemente del género y la edad. Los valores absolutos de los marcadores nefrotóxicos correlacionaron positiva y significativamente con sus índices, lo que indica que es útil la corrección con creatinina, con excepción de la Fosfatasa Alcalina la cual refleja mejor su utilidad diagnóstica en valores absolutos. Plomo/creatinina, β-2-microglobulina y Calcio/creatinina mostraron diferencias estadísticamente significativas al estratificar la muestra según grupo etario. La excreción urinaria de cadmio, tanto el grupo expuesto como el control supera ciertos puntos de corte descritos en investigaciones internacionales. Conclusiones: la evaluación de la toxicidad renal debe contar con el monitoreo de varios marcadores, dado que algunos serán más sensibles a los cambios precoces debido a exposiciones crónicas.
Palabras clave: biomarcadores, metales, eliminación renal, tabaquismo pasivo.
Renal function, cadmium and lead urinary levels in children of the municipality of Naguanagua (estado Carabobo, Venezuela), exposed to environmental tobacco smoke
Summary
Objective: metals presents at the gaseous and particulate phases of environmental tobacco smoke are considered nephrotoxic. In this research, urinary levels of cadmium, lead and renal function were evaluated in children exposed to environmental tobacco smoke in a community of the Naguanagua municipality (Carabobo, Venezuela). Materials and methods: The sample consisted of 43 children (21 exposed and 22 not exposed), whom were determined urinary indices in spot urine: cadmium/creatinine, lead/creatinine, albumin/creatinine, calcium/creatinine, alkaline phosphatase/creatinine y β-2-microglobulin/creatinine. Results: in the exposed group there is a positive and significant correlation between β-2-microglobulin/creatinine and albumin/creatinine regardless gender and age. Absolute values of the nephrotoxic markers correlated positive and significantly with their indices, which indicates that correction with creatinine is useful, the exception of alkaline phosphatase, that better reflects its diagnostic utility in absolute values. lead/creatinine, β-2-microglobulin and calcium/creatinine showed statistically significant differences when stratifying the sample according to age. Urinary excretion of Cadmium, both exposed and control group exceeds certain cut points described in international researchs. Conclusions: renal toxicity evaluations should count on the monitoring of several markers, because some will be more sensitive to early changes due to chronic exposures.
Key words: biomarkers, metals, renal elimination, passive smoking.
Introducción
La exposición al humo de tabaco ambiental se origina por la inhalación involuntaria del Humo de Segunda Mano (HSM) [1], así como por la inhalación, ingestión y captación dérmica de los contaminantes residuales presentes en las fases particulada y gaseosa del tabaco conocida como al Humo de Tercera Mano (HTM) [2]. La mayoría de las patologías por exposición a este contaminante aparecen generalmente en edades avanzadas de la vida, sin embargo, se sabe que dichas enfermedades se inician sub-clínicamente en las primeras etapas de la vida por lo que se debe considerar al tabaquismo pasivo como una enfermedad pediátrica, debido a los efectos adversos que provoca en sus tres etapas (fetal, infantil y juvenil) [3-5].
El tabaco aumenta el riesgo de desarrollar enfermedad renal, induciendo cambios funcionales, alteraciones morfológicas vasculares y daño tubular renal, generalmente irreversibles [6]. En este sentido, metales pesados como cadmio (Cd) y plomo (Pb) presentes en el humo del tabaco pueden jugar un papel determinante en la génesis de patología renal [6,7]. El óxido de Cd generado durante la combustión de los cigarrillos es altamente biodisponible tanto para el fumador activo como para el pasivo [8], acumulándose en el organismo de forma gradual e incrementándose con la edad debido a su larga vida media. De esta manera el daño causado por este metal se manifiesta clínicamente por proteinuria de bajo peso molecular [9,10], aminoaciduria, bicarbonaturia, glucosuria y fosfaturia [7,11]. De igual modo, está demostrada la presencia de plomo en la fase particulada y gaseosa del humo de tabaco [12,13], lo cual representa una exposición continua a dicho metal para los fumadores pasivos, especialmente los niños. Se conoce que una exposición a plomo superior a 5 años puede inducir una atrofia tubular renal progresiva con fibrosis intersticial, que clínicamente se traduce en insuficiencia renal crónica y gota [14].
Los niveles de Cd en sangre sugieren exposición aguda, mientras que los urinarios indican exposición crónica; pero, para el caso del Pb existe gran controversia sobre cuáles son los niveles permisibles en sangre y orina, debido a que existen evidencias de que valores de Pb que antes eran considerados como no tóxicos se asocian a una mayor morbilidad de la población general [11], sin embargo, se considera elevada toda plumbemia igual o superior a 5 μg/dl [15,16].
Ahora bien, el aumento de la prevalencia de enfermedades renales crónicas y su relación con la exposición a elementos nefrotóxicos como Cd y Pb, han permitido la identificación de factores de riesgo modificables, así como la necesidad de evaluar marcadores de daño precoz, por ejemplo β-2-microglobulina urinaria (β2Mur), albuminuria, calciuria y fosfatasa alcalina urinaria (FAu) [11,17]. De allí que, la lesión renal provocada por exposición a contaminantes ambientales debe evaluarse tanto por la medición de los niveles del tóxico en sangre y orina, como por la determinación de los marcadores bioquímicos renales que proporcionan información valiosa acerca de disfunción renal subclínica en individuos con alto riesgo por su nivel de exposición [17,18], considerando las variaciones individuales en la dilución de la orina a través del ajuste por creatinina [19], lo que cobra especial importancia en el área pediátrica dada la dificultad de recoger muestras de orinas horarias simplificando la monitorización a través de índices urinarios que han demostrado su utilidad clínica [20,21].
Acerca del impacto que tiene la exposición al HSM sobre la salud, son innumerables las investigaciones publicadas y se han estudiado sus efectos en distintos grupos etarios [22-25]; siendo los estudios en niños, primordialmente orientados a evaluar los efectos de la exposición del humo del tabaco sobre el sistema respiratorio [26,27]; sin embargo son escasos los estudios sobre la función renal en niños expuestos [17] y más aún donde evalúen su asociación con la excreción urinaria de metales. Algunas investigaciones indican que los fumadores pasivos presentan mayores niveles de metales sanguíneos y urinarios que aquellos que no están expuestos a este contaminante [28-30] dichos estudios generalmente abordan población adulta [31,32], por tanto, niños y adolescentes representan una población idónea para estudiar la posible asociación entre la función renal y la exposición al HSM, ya que presentan una baja prevalencia de enfermedad renal crónica y son mucho menos propensos a ser afectados por los factores de riesgo como la diabetes y la hipertensión [33]. Considerando lo planteado, en esta investigación se evaluaron niveles urinarios de cadmio y plomo y la función renal en niños expuestos al humo de tabaco ambiental en una comunidad del municipio Naguanagua (Carabobo, Venezuela).
Materiales y métodos
Es una investigación de casos y controles, se evaluaron niños de una comunidad del Municipio Naguanagua (estado Carabobo, Venezuela), expuestos y no expuestos a humo de tabaco ambiental durante los meses de junio y julio de 2016. De esta población se seleccionó una muestra de 43 niños los cuales fueron divididos en 21 expuestos y 22 no expuestos.
Los niños “no expuestos” cumplieron con los siguientes criterios de inclusión: edad comprendida entre 1 y 12 años (ambas inclusive), no presentar patologías metabólicas, cardíacas o renales diagnosticadas, ni fiebre o síndrome viral en las 72 horas previas al muestreo, así como no presentar diagnóstico o tratamiento por intoxicación de plomo; los niños “expuestos” fueron seleccionados bajo los mismos criterios descritos para los no expuestos excepto por la exposición al humo de tabaco ambiental en el hogar (grupo expuesto), se procuró que los grupos quedaran conformados similarmente en cuanto al género y la edad. Para la selección de la muestra se aplicó una encuesta validada por juicio de expertos, para conocer las variables socio-epidemiológicas tales como: exposición al humo del tabaco ambiental, otras posibles fuentes de exposición a plomo y antecedentes clínicos.
Variables antropométricas
A los 43 niños, se les midieron las variables antropométricas de la siguiente manera: el peso y la talla (se determinaron de pie, descalzos, utilizando una balanza y un tallímetro). Se utilizó el programa WHO Anthro Plus versión 1.0.4 para calcular los valores del IMC (índice de Quetelet) y los percentiles correspondientes. Según patrones de referencia nacionales [34,35] se catalogó el estado nutricional antropométrico de la siguiente forma: obesidad IMC > p 97; sobrepeso IMC > p 90 y < p 97; normopeso IMC > p 10 y < p 90 y bajopeso IMC < p10.
Muestras
Se solicitaron dos muestras de orina puntual a cada paciente, una matutina (primera micción de la mañana) y una recolectada 2 horas después de la muestra inicial; a la primera muestra se le realizó un análisis de orina general (examen físico macroscópico, examen químico mediante las cintas de orina, proteinuria cualitativa con el reactivo de Robert y análisis del sedimento urinario), que permitió excluir muestras con bacteriuria, hematuria o proteinuria. Esta muestra se dividió en alícuotas, se conservó a 4ºC previo tratamiento con ácido nítrico (HNO3), para determinar posteriormente los niveles de Cd y Pb, otra alícuota se utilizó para determinar la excreción urinaria de albumina y creatinina. De la segunda orina se fraccionaron alícuotas, se ajustaron a pH entre 6 y 8 con NaOH 1 N y se refrigeraron a 4ºC, en esta muestra se realizaron las evaluaciones bioquímicas restantes con su respectiva corrección de creatinina. Los análisis se realizaron en la Unidad de Investigación en Toxicología Molecular (UTM), Escuela de Bioanálisis, Facultad de Ciencias de la Salud, Universidad de Carabobo.
Evaluación de los metales pesados
Todo el material de vidrio utilizado en el análisis, fue lavado con detergente, luego sumergido varios minutos en ácido nítrico (HNO3) al 50% (v/v) y posteriormente enjuagado con agua desionizada. Las muestras de orina (primera micción) se descongelaron, homogeneizaron y filtraron antes de ser analizadas. El cadmio se determinó por espectrofotometría de absorción atómica con cámara de grafito [36]. Los resultados se obtuvieron por interpolación en la curva de calibrado y se expresaron en μg de Cd/g de creatinina (μg/g). El límite de detección fue 0,03 µg/L y se asumió como punto de corte para Cd en orina puntual el valor de 1 µg/g creat descrito por dos autores [37,38], dado que no existe consenso a nivel internacional para la exposición ambiental.
El plomo se determinó por espectrofotometría de absorción atómica en llama [39], la concentración de Pb en orina de cada muestra se determinó directamente por interpolación de la lectura obtenida restando el blanco, en la curva de calibrado, se expresó en µg/dL y se ajustó determinando el índice de Pb µg/g de creatinina. Dado que no existen valores de referencia para la excreción de Pb-U en orina puntual, se asumió como elevado aquel valor que se ubicó por encima del percentil 75 calculado por grupo etario, a partir del conjunto de valores obtenidos en el grupo no expuesto.
Evaluación bioquímica de la función renal
Se determinaron niveles de β-2-Microglobulina por inmunoabsorción de ELISA, cuyos valores < 20 ug/dL fueron considerados como normales. La albuminuria (Alb) se determinó mediante técnica inmunoturbidimétrica y se tomó como punto de corte 20 mg/L [40]. Se ajustaron las concentraciones de ambas proteínas con la creatinina urinaria, obteniendo los respectivos índices urinarios. Para el índice Albúmina/creatinina (A/Cr) el punto de corte asumido fue < 30 mg/g creatinina [41], mientras que para el Índice β-2-Microglobulina/creatinina se eligió < 300 ug/g creatinina [42].
Cabe destacar que tanto el calcio como la actividad de la fosfatasa alcalina urinaria (FAu) fueron medidos inmediatamente una vez obtenidas las muestras; el calcio (Ca) y la creatinina (Cr) se determinaron mediante técnicas colorimétricas, estableciendo como punto de corte para el cociente Ca/Cr valores <0,2 en orina puntual. La actividad de FAu se midió a través de técnica colorimétrica-enzimática. Debido a la ausencia de valores referenciales para esta enzima en la matriz urinaria y que éstos, en muchos casos también dependen de la metodología empleada para su medición, se asumió como criterio que un valor elevado sería el ubicado por encima del percentil 75 calculado por grupo etario, a partir del conjunto de valores obtenidos en el grupo no expuesto. Los datos empíricos se obtuvieron a la par del muestreo para el caso del calcio y la fosfatasa, es decir, se procesaron inmediatamente, los demás parámetros se procesaron en el lapso junio – agosto 2016.
Análisis estadístico
Se utilizó el programa PAST versión 3.0 para Windows. Antes de aplicar las pruebas estadísticas todos los datos fueron probados para conocer si siguieron la distribución normal utilizando para ello la Prueba de Kolmogorov-Smirnov. Se calcularon medidas de tendencia central para las variables medidas en escala numérica, así como frecuencias absolutas para las variables medidas en escala nominal. Las diferencias entre los grupos expuesto y no expuesto fueron evaluadas con las pruebas respectivas de acuerdo al cumplimiento de los supuestos de normalidad y homogeneidad de varianza (t de Student para grupos independientes o prueba de la suma de los rangos de Wilcoxon <Wilcoxon Rank Sum Test>). Se aplicó Kruskall Wallis para diferencias entre los grupos según estado antropométrico. Se empleó tablas de contingencias y aplicación de pruebas de Ji-cuadrado para asociar las variables en cuanto a la alteración de los parámetros. Las correlaciones se realizaron con Spearman. Se consideró un nivel de significación de p ≤ 0,05.
Control de sesgos: se garantizó la confiabilidad en los resultados mediante el uso de controles de calidad y el procesamiento de las muestras codificadas, por lo que no se conocía el grupo al que pertenecía la muestra analizada.
Consideraciones éticas: se solicitó a los padres o representantes de los niños un consentimiento subrogado escrito para la participación en el estudio, siguiendo los principios éticos para las investigaciones médicas en seres humanos, establecidos en el Código de Ética para la vida del Ministerio del Poder Popular para Ciencia y Tecnología [43].
Resultados
La muestra estuvo conformada por 43 niños con edades de 1 a 12 años (ambas inclusive), de los cuales 19 fueron del género femenino y 24 del género masculino; además se clasificó según el estado antropométrico, observándose que el estado “normopeso” predominó con 62,8%, seguido por el estado “obesidad” (23,3%) y finalmente los estados “bajo peso” y “sobrepeso” presentaron la misma frecuencia (7%). La muestra también se clasificó en dos grupos según la exposición y además se hizo una discriminación según grupo etario, cabe resaltar que dicha distribución fue intencionalmente proporcional para ambos grupos. Sin embargo, se consideró relevante caracterizar la muestra según el estado nutricional antropométrico tomando en cuenta el género, el grupo etario y la exposición, como se muestra en la Tabla 1.
Tabla 1. Distribución de la muestra según género, grupo etario, estado nutricional antropométrico y exposición al humo de tabaco.
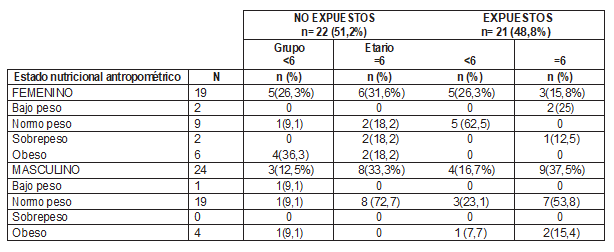
Fuente: Datos propios de la investigación.
Se evidenció que el género masculino, independientemente de la exposición y el grupo etario, presentó mejor estado nutricional antropométrico mientras que 25% de las niñas (≥ 6 años) expuestas cursaban con bajo peso y 54,5% de las niñas no expuestas presentaban obesidad. Al aplicar la prueba de Kruskall Wallis no hubo diferencias significativas para los parámetros evaluados según la exposición y el estado antropométrico (p > 0,05).
Por su parte, los valores de excreción urinaria de Pb, expresados mediante su índice (Pb/Cr), resultaron más altos en los niños expuestos de ambos grupos etarios que en los no expuestos al humo de tabaco ambiental, aunque sin diferencia significativa. El cadmio urinario, expresado a través de su índice, presentó valores superiores en el grupo etario ≥ 6 años expuesto en comparación con el grupo control pero sin diferencias estadísticas significativas (Tabla 2).
Tabla 2. Índices de Pb/Cr y Cd/Cr en los grupos estudiados
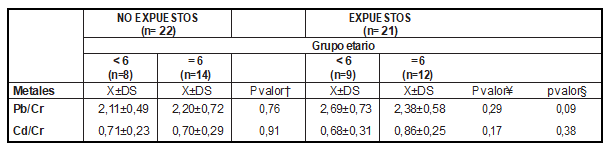
Fuente: datos propios de la investigación
Pb/Cr: índice Pb/Cr, índice Cd/Cr. Los valores se expresan como media ± Desviación estándar.
† comparación entre grupos etarios no expuestos, ¥ comparación entre grupos etarios expuestos, §según exposición
Al comparar los biomarcadores de nefrotoxicidad según la exposición y el grupo etario, se pudo observar en el grupo expuesto que las medias de los valores de β2M, índice β2M/Cr, Alb y el índice A/Cr fueron superiores en los niños ≥ 6 años, e inclusive el valor de la media para el índice β2M/Cr también es superior en los niños expuestos ≤ 6 años (Tabla 3), siendo significativa la diferencia para los grupos etarios en los niños expuestos. Así mismo, se puede evidenciar que el promedio del índice Ca/Cr en los niños ≤ 6 años también es superior en el grupo expuesto con respecto al no expuesto. Respecto a la FAu y su índice (FAu/Cr) sus medias son mayores para todos los niños que conforman el grupo expuesto, sin embargo, no existen diferencias estadísticamente significativas (p>0,05) para las variables señaladas.
Tabla 3. IMC y valores urinarios de β2M, índice β2M/Cr, Albuminuria, índice A/Cr e índice A/β2M, índice calcio/creatinina, fosfatasa alcalina, e índice fosfatasa alcalina/creatinina en los grupos estudiados
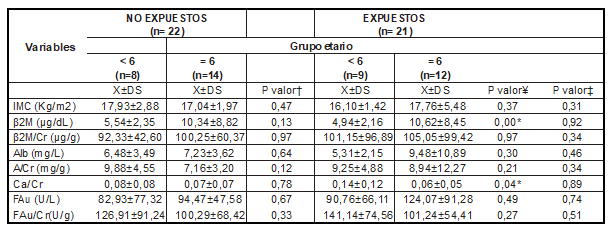
Fuente: datos propios de la investigación.
IMC: Índice de Masa Corporal, β2M: β-2-Microglobulina, Alb: Albuminuria, β2M/Cr: Índice β-2-microglobulina/Creatinina, A/Cr: Índice Albúmina/Creatinina, A/β2M: Índice Albúmina/β-2-Microglobulina, Ca/Cr: calcio/creatinina, FAu: fosfatasa alcalina urinaria, FAu/Cr: Índice fosfatasa alcalina/creatinina, Los valores se expresan como media ± Desviación estándar. Pvalor‡: Para la muestra según exposición, Pvalor†: Según grupo etario en el grupo no expuestos, Pvalor¥: según grupo etario en el grupo expuestos. ‡ según exposición.
Tabla 4. Correlación de variables (función renal, IMC) en los grupos de estudio según género y grupo etario
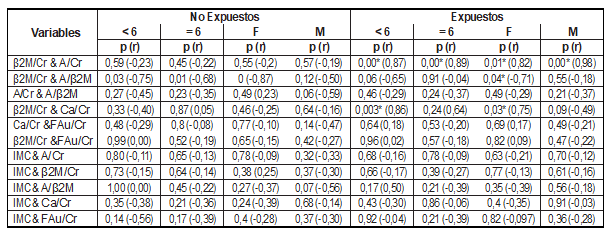
Fuente: Datos propios de la investigación
β2M: β-2-Microglobulina, A/β2M: índice Albuminuria/ β-2-Microglobulina, β2M/Cr: Índice β-2-microglobulina/Creatinina, A/Cr: Índice Albúminuria/Creatinina, Ca/Cr: calcio/creatinina, FAu: fosfatasa alcalina urinaria, FAu/Cr: Índice fosfatasa alcalina/creatinina. r (coeficiente de correlación). * P: significativa < 0,05.
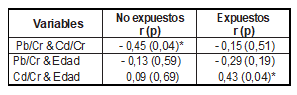
Con respecto a la excreción de los metales, se evidencia una correlación negativa y significativa entre los índices Pb/Cr y Cd/Cr en el grupo no expuesto. El índice Cd/Cr y la edad de los niños expuestos al humo de tabaco ambiental, se evidenció una correlación positiva y significativa (Tabla 5).
Tabla 5. Correlación entre metales pesados y la edad en los grupos de estudio
Fuente: datos propios de la investigación.
Pb/Cr: índice Pb/Cr, índice Cd/Cr. r (coeficiente de correlación). * La correlación es significativa en el nivel 0,05
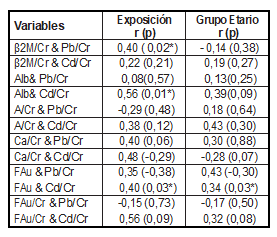
En cuanto a los marcadores de nefrotoxicidad y el índice Pb/Cr no se evidencia correlación, en el caso de la excreción de cadmio (Cd/Cr) en el grupo expuesto, la FAu y la Alb correlacionan positiva y significativamente (Tabla 6).
Tabla 6. Metales urinarios y correlación global con índices de función renal ajustados por exposición y grupo etario
Fuente: datos propios de la investigación.
β2M: β-2-Microglobulina, Alb: Albuminuria, β2M/Cr: Índice β-2-microglobulina/Creatinina, A/Cr: Índice Albúmina/Creatinina, A/β2M: Índice Albúmina/β-2-Microglobulina, Ca/Cr: calcio/creatinina, FAu: fosfatasa alcalina urinaria, FAu/Cr: Índice fosfatasa alcalina/creatinina. r (coeficiente de correlación). * La correlación es significativa en el nivel 0,05
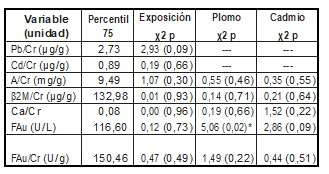
En cuanto a la alteración de los parámetros evaluados, se analizó la asociación con la exposición al humo de tabaco de acuerdo a los valores del percentil 75 del grupo no expuesto (Tabla 7), no encontrándose asociación con dicha exposición, sin embargo, cuando se analizan los marcadores nefrotóxicos con la excreción alterada de Pb/Cr, este muestra asociación significativa con FAu (p > 0,05).
Tabla 7. Asociación de la alteración de la excreción de metales con indicadores nefrotóxicos y con la exposición al humo de tabaco
Fuente: datos propios de la investigación.
β2M: β-2-Microglobulina, β2M/Cr: Índice β-2-microglobulina/Creatinina, A/Cr: Índice Albúmina/Creatinina, Ca/Cr: calcio/creatinina, FAu: fosfatasa alcalina urinaria, FAu/Cr: Índice fosfatasa alcalina/creatinina. χ2: chi cuadrado *significativo p < 0,05.
Discusión
En esta investigación se midieron indicadores de nefrotoxicidad en un grupo de niños expuestos a humo de tabaco, así como la excreción urinaria de Pb y Cd. Se procuró que el grupo no expuesto, fuese comparable en cuanto a la distribución de género y edad al grupo expuesto a fin de analizar los niveles de los diferentes índices urinarios, así como el IMC en ambos grupos, por lo que no tiene mayor relevancia disertar sobre la frecuencia del género o de la exposición en la muestra estudiada. En relación con el estado nutricional, 25% de las niñas expuestas presentaron bajo peso; aun cuando no se indagó acerca de la antigüedad de la exposición, es posible que algunos niños estén expuestos a los tóxicos del humo de tabaco desde el momento de la concepción. Al respecto existen fuertes evidencias sobre la asociación entre el tabaquismo materno durante el embarazo y la restricción del crecimiento intrauterino [44-46], sin embargo, los efectos de esta exposición sobre el crecimiento lineal postnatal no están bien definidos [47]. Se ha señalado que debido a la disminución de la vascularización de la placenta y por tanto del área de intercambio de gases y nutrientes entre la madre y el feto, se origina un retardo en el crecimiento intrauterino [48] además de malnutrición fetal, condicionando a los lactantes a IMC bajos durante su desarrollo. Adicional a esto, se ha reportado que los componentes del humo del tabaco limitan la absorción y utilización del complejo vitamínico B, disminuyen los niveles de ácido fólico, vitaminas A y C en niños, lo cual favorece el estrés oxidativo e influye en su estado nutricional [49].
Desde una perspectiva diferente, estudios recientes describen efectos obesogénicos originados por la exposición al humo del tabaco, posiblemente relacionados a la inhibición de la lipólisis, inducida por catecolaminas por los hidrocarburos aromáticos policíclicos presentes en el humo de tabaco. McConnell et al. (2015), en un estudio longitudinal llevado a cabo en niños expuestos al humo de segunda mano reportaron una mayor frecuencia de obesidad con el transcurrir de los años [22]. En el presente estudio aun cuando se observó una frecuencia de niños obesos en el grupo expuesto, no existió asociación significativa entre la exposición y el estado nutricional antropométrico, por lo que es evidente la existencia de covariables como la genética, ingesta calórica y estrato socioeconómico, que no fueron evaluadas en este estudio.
En relación a los niveles de metales urinarios, estudios previos han señalado al HSM como fuente de exposición al Pb, para niños que viven en ambientes de fumadores [28]. En esta investigación no se pudo evidenciar asociación entre la excreción urinaria de Pb y la exposición al humo de tabaco ambiental. En general la muestra presentó valores de Pb/Cr inferiores al punto de corte sugerido por Leung et al. (2013) correspondiente a 4,8 µg/g en niños chinos [50] y al reportado por Hoet et al. (2013) para adultos no expuestos ocupacionalmente en Bélgica (3 µg/g) [37]. El grupo etario < 6 años (expuesto), presenta cifras más altas que el resto de los grupos sin diferencias significativas, esto puede deberse a diferencias en la excreción del metal de acuerdo a la edad, ya que se ha descrito que niños menores de 2 años retienen 34% del Pb absorbido en comparación con los adultos (1%) y presentan mayor excreción [51].
Por otra parte, algunos autores han encontrado asociación entre la exposición a HSM y Pb sanguíneo [30,52], sin embargo, en esta investigación se empleó la orina puntual como método no invasivo de monitoreo. Existen estudios que apoyan la eficacia de la medición de Pb en orina puntual como indicador reciente de exposición [53], en este sentido, un estudio concluye que la medición urinaria puede reemplazar la medición sanguínea en la evaluación de la exposición ocupacional a este metal, mas no en el caso de la exposición ambiental en niños [51]. Los hallazgos de esta investigación no permiten realizar tal afirmación dado que se requieren estudios con diseños que puedan poner en evidencia la utilidad de la orina puntual, así como los puntos de cortes respectivos que establezcan niveles de exposición en nuestra población. Aun así la plumburia encontrada en la muestra es significativa tomando en cuenta que la OMS señala que no existen concentraciones de plomo que puedan considerarse seguras.
En cuanto al Cadmio, tanto el grupo expuesto como el control presentan una excreción urinaria superior al punto de corte (0,29 µg/g) descrito para niños chinos [50]; también superan la mediana reportada en niños japoneses (0,34 μg/g) [54] y en niños de Bélgica (0,32-0,36 µg/g) [55]. Asimismo, supera el valor medio reportado en adultos de Bizkaia (País Vasco) correspondientes a 0,54 µg/g [56]. Cabe resaltar que no existe un consenso sobre el valor referencial para la excreción de este metal en exposiciones ambientales. En el ámbito ocupacional, la OSHA (2003) ha establecido que 3 μg/g es un nivel de decisión para retirar al trabajador del área laboral y monitorear periódicamente [57].
En el presente estudio no se evidenció asociación entre la excreción urinaria de Cd (Cd/Cr) y la exposición al humo de tabaco, esto puede ser explicado debido a que la alimentación y el tabaquismo representan las principales fuentes de exposición a dicho metal a nivel no ocupacional. Se ha señalado que dichas exposiciones pueden considerarse equivalentes [58], al respecto, varios autores sugieren que la exposición dietética puede ejercer mayor influencia que otras fuentes [54-56], sin embargo, en el presente estudio no se indagó sobre la alimentación. Además, resulta importante tener en cuenta el carácter bioacumulativo del Cd en el organismo, principalmente en riñones, por lo que la correlación positiva entre la edad y Cd/Cr en el grupo expuesto en este estudio indica que se debe monitorear periódicamente este metal, así como marcadores de función renal, en esta población.
En cuanto a los marcadores de nefrotoxicidad evaluados, los grupos estudiados no sobrepasan los valores referenciales ni presentan diferencias estadísticamente significativas con respecto a la exposición. La β-2-Microglobulina presentó valores superiores en los niños ≥ 6 años y particularmente en el grupo expuesto se observan diferencias estadísticamente significativas entre los grupos etarios, lo que se contrapone con lo descrito por otros investigadores, dado que en su estudio el índice de este polipéptido fue mayor en niños del grupo etario < 7 años, sin nefropatías [59]. Cabe resaltar que la utilidad de la β-2-Microglobulina urinaria como marcador precoz de nefrotoxicidad ha sido señalada en diversas investigaciones [38, 60, 61] por tanto los resultados de este marcador en esta investigación son relevantes conociendo la capacidad de resistencia innata y adquirida del sistema nefrológico. Dado que este polipéptido es un marcador de efecto, los valores en exposiciones tempranas pueden mantenerse de forma subclínica en la etapa pediátrica para debutar con alguna alteración en la etapa adulta, de allí que sería recomendable en la evaluación pediátrica incluir este marcador como cribado, especialmente en grupos susceptibles a exposiciones ambientales, dado que los efectos pueden ser reversibles en etapas incipientes de la alteración tubular.
Por su parte, el índice Ca/Cr de la muestra no sobrepasa el punto de corte considerado normal en la literatura (0,2), sin embargo los niños del grupo expuesto < 6 años, presentan niveles superiores en comparación con el resto de los grupos etarios evaluados, siendo estadísticamente significativa la diferencia con respecto al grupo etario de contraste, este hallazgo coincide con los resultados de Hibi et al. (2015) quienes demostraron que la excreción de calcio varía con la edad siendo mayor en los niños de menor edad [59]. Además este hecho se ve reforzado por la correlación negativa y significativa del índice Ca/Cr con la edad, observada en el análisis global de la muestra ajustada por exposición. Aun cuando en este estudio no se evidenció correlación con la excreción de los metales, se evidencia correlación con β2M/Cr específicamente en el grupo expuesto, lo cual apoya la utilidad de este índice como marcador de lesión tubular.
En cuanto a la fosfatasa alcalina (FA), enzima del borde en cepillo del segmento Tubular S3 del riñón, región altamente vulnerable a la lesión tóxica algunos autores observaron una débil correlación positiva entre este marcador y la plumbemia en hombres expuestos ocupacionalmente [62,63]. En el presente estudio la excreción de FAu y Pbu se asociaron al superar el percentil 75 establecido como punto de corte, además esta enzima se correlacionó con el Cd/Cr, en el grupo expuesto, lo cual apoya su utilidad como marcador precoz de citotoxicidad. Cabe resaltar que son escasos los estudios en nuestra población sobre niveles de excreción fisiológica de enzimas urinarias especialmente en niños, lo que dificulta la interpretación de los valores obtenidos, en este sentido, Di Carlo et al. (2007) reportan un punto de corte de 8 UI/L para esta enzima en adultos sin nefropatías [64]. Este valor es superado ampliamente en la muestra de este estudio, lo cual permite sugerir que pueden existir diferencias en la excreción de FAu entre adultos y niños. Se requiere profundizar al respecto, puesto que dichos autores no encontraron relación entre el aumento de la actividad de FA sérica y la urinaria, lo cual descartaría la suposición de que al ser niños y presentar la isoenzima ósea sérica elevada, pudiera influir en la excreción de la enzima durante el crecimiento.
La excreción de albumina urinaria es reconocida como indicador de alteraciones en la función glomerular, se ha reportado asociación de la excreción urinaria de Cd con los niveles de Albuminuria, independientemente de la diuresis, la edad o el tabaquismo [55]. En este estudio se observó una correlación positiva y significativa entre la Alb y Cd/Cr en el grupo expuesto, aun cuando los niveles de Alb están dentro de rangos fisiológicos. Este hecho reviste importancia debido a que bajas concentraciones de Cd urinario pudieran estar impactando a largo plazo la función glomerular de los niños.
Un gran número de enfermedades nefrológicas son el resultado de la interacción de dos determinantes: uno interno o constitucional y otro externo o medioambiental. Cada uno de los determinantes incluye numerosos factores de riesgo [65]. En la práctica resulta difícil estimar el porcentaje de peso atribuido a factores medioambientales, de allí que recientemente, se ha planteado un enfoque denominado exposoma que apoya la evaluación de la exposición basado en la vigilancia biológica ya que las fuentes y niveles de exposición se modifican a lo largo del tiempo, pero pueden ser detectadas en sus niveles tóxicos en las muestras obtenidas durante etapas críticas de la vida [66,67].
El tamaño muestral y diseño transversal de esta investigación es una limitación, estudios longitudinales especialmente en la población infantil son necesarios para monitorear el estatus de contaminación en la población a largo plazo, así como la interacción sinérgica a múltiples metales pesados. Por otra parte, desde el punto de vista analítico, el índice de individualidad para una prueba de laboratorio se puede aumentar estratificando la población en grupos, lo que optimizaría la utilidad de la prueba. Existen además alternativas para evaluar diferencias en el monitoreo de un analito de los individuos, tal es el caso del Valor de Referencia del Cambio de un analito o xenobiótico específico, un método utilizado para interpretar una diferencia en las mediciones en un paciente, donde el resultado de la prueba actual se compara con los resultados pasados del paciente y no con un valor de referencia basado en la población [68].
Más allá de las limitaciones señaladas, los resultados de este estudio indican la importancia de considerar la edad para interpretar los valores de los marcadores tubulares así como para la excreción urinaria de los metales estimados en orinas puntuales, asimismo que los niños de esta comunidad están expuestos a metales y que es necesario identificar todas las fuentes de exposición posible a fin de disminuir el impacto a nivel renal de los mismos, mediante estrategias de control en diversos ámbitos.
A manera de conclusión, este estudio permite evidenciar entre otros aspectos, que a nivel nacional no existen investigaciones que permitan comparar los resultados acá obtenidos, de igual modo son escasos los estudios en población infantil latinoamericana, por lo tanto, no existen consensos sobre la excreción de estos metales en dicha población. Un aspecto importante a destacar es la correlación positiva y significativa de los valores absolutos de los marcadores nefrotóxicos con sus índices, lo que indica que es útil la corrección con creatinina, con excepción de la FAu la cual parece reflejar mejor su utilidad diagnóstica en valores absolutos. Es evidente que la estratificación de la muestra según grupo etario es determinante para una interpretación adecuada de la excreción urinaria de metales y marcadores nefrotóxicos. La evaluación de la toxicidad renal debe contar con el monitoreo de varios marcadores, dado que algunos serán más sensibles a los cambios precoces debido a exposiciones crónicas.
Conflictos de interés: no existen conflictos de intereses.
Fuentes de financiación: este estudio fue subvencionado por la Unidad de Toxicología Molecular de la Universidad de Carabobo.
Literatura citada
1. Hawkins S, Berkman L. Identifying infants at high- risk for second-hand smoke exposure. Child Care Health Dev 2014; 40(3):441-445. DOI: [10.1111/ cch.12058]
2. Jacob P, Benowitz NL, Destaillats H, Destaillats H, Gundel L, Hang B, et al. Thirdhand Smoke: New Evidence, Challenges, and Future Direc- tions. Chem res toxicol 2017; 30(1):270-294. DOI:
10.1021/acs.chemrestox.6b00343.
3. Ferrís J, Ortega J. López J, Berbel O, Marco A, Gar- cía J. Tabaquismo parental y cáncer pediátrico. Rev Esp Pediatr 2004; 60(3):225-236.
4. Joya X, Manzano C, Álvarez AT, Mercadal M, Torres F, Salat-Batlle J, Garcia-Algar O. Transgenerational Exposure to Environmental Tobacco Smoke. Int J Environ Res Public Health 2014, 11:7261-7274. DOI: [10.3390/ijerph110707261].
5. Aoki Y, Yee J, Mortensen M. Blood cadmium by race/hispanic origin: The role of smoking. Environ Res 2017; 155:193-198. DOI: 10.1016/j. envres.2017.02.016
6. Gutiérrez D. Enfermedad renal crónica, su re- lación con el tabaquismo. Comportamiento en pacientes con hipertensión arterial. Portales Médicos 2007; 2(6):55-58
7. Price R. Cadmium Nephropathy and Smoking. Clin Med Insights Urol 2017; 10: 1–8. DOI: https://doi.org/10.1177/1179561117726090.
8. Soisungwan S, Moore M. Adverse Health effects of chronic exposure to low-level cadmium in foodstuffs and cigarette smoke. Environ Health Perspect 2004; 112(10):1099-1103. DOI: 10.1289/ ehp.6751.
9. Buser MC, Ingber SZ, Raines N, Fowler DA, Scini- cariello F. Urinary and blood cadmium and lead and kidney function: NHANES 2007-2012. Int J Hyg Environ Health 2016; 219:261-267. DOI:
10.1016/j.ijheh.2016.01.005
10. Robles-Osorio ML, García-Solís P, Solís-Sainz JC, Montero-Perea D, Avilés-Romo I, Sabath-Silva E. Non-critical urinary cadmium excretion as a risk factor associated with tubular markers of early kidney injury in Central Mexico. Nefrología (Madr)2017; 37(5):552-554. DOI: 10.1016/j.nef- ro.2017.01.008
11. Sabath E, Robles-Osorio ML. Renal health and the environment: heavy metal nephrotoxicity. Nefrol Publ Of Soc Esp Nefrol 2012; 32(3):279-86. DOI:
10.3265/Nefrologia.pre2012.Jan.10928
12. Klepeis N, Apte M, Gundel L, Sextro R, Nazaroff W. Determining size-specific emission factors for environmental tobacco smoke particles. Aerosol Sci Technol 2003; 37(10):780-790. DOI: http: //doi. org /10.1080/02786820300914
13. Campbell RCJ, Klerx WNM, Talhout R, Stephens WE. Speciation of metals and mettaloids in tobacco and tobacco smoke: implications for health and regulations. RIVM Report 2015-0026.
14. Paraíso V, Felipe C, Martín J. Nefropatías tóxicas: concepto, clasificación, etiopatogenia y fenoti- pos clínicos. Medicine 2007; 9(81):5192-5199. DOI: https://doi.org/10.1016/S0211-3449(07)74633-7.
15. Betts KS. CDC Updates Guidelines for children’s lead exposure. Environ Health Perspect 2012;
120(7):a268. DOI:10.1289/ehp.120-a268.
16. Instituto Nacional de Seguridad e Higiene en el Trabajo. Límites de exposición para agentes químicos. Madrid: Instituto Nacional de Seguridad e Higiene en el Trabajo; 2015.
17. García E, Loeffler L, Weaver V, Fadrowski J, Navas A. Kidney function and tobacco smoke exposure in US adolescents. Pediatrics 2013; 131(5):1415-
23. DOI: 10.1542/peds.2012-3201.
18. Tagle R, González F, Acevedo M. Microalbu- minuria y excreción urinaria de albúmina en la práctica clínica. Rev méd Chile 2012;
140(6):797-805. DOI: http://dx.doi.org/10.4067/ S0034-98872012000600016..
19. Calabia ER. Medida de la función renal. Evalua- ción del cociente microalbuminuria/creatinina. Nefrología 2004; 24(suppl6):35-46.
20. García V, Muros M, León C, Duque J, Oliva C, Du- que R, et al. Estudio de la eliminación urinaria de N-acetil-glucosaminidasa y β2-microglobulina en la infancia. Trastorno de su excreción en la diabetes mellitus y en patología renal. Nefrología
1990; 10(4):393-399.
21. Salabarría J, Santana S, Liriano M. Excreción urinaria de una sustancia predicha del índice sustancia/creatinina. Rev Latinoam Patol Clin Med Lab 2015; 62(2):119-126.
22. McConnell R, Shen E, Gilliland FD, Jerrett, M, Wolch J, Chang CC, Berhane K. A Longitudinal Cohort Study of Body Mass Index and Childhood Ex- posure to Secondhand Tobacco Smoke and Air Pollution: The Southern California Children’s Health Study. Environ Health Perspect 2015;
123(4):360–366. DOI: 10.1289/ehp.1307031.
23. Diver WR, Jacobs EJ, Gapstur SM. Secondhand Smoke Exposure in Childhood and Adulthood in Relation to Adult Mortality Among Never Smok- ers. AJPM 2018; 55(3):345-352. DOI: 10.1016/j. amepre.2018.05.005.
24. Mu-Rong C, Marcus SC, Chung-Yih K, Chih-Hong P, Chiung-Wen H. Children are particularly vul- nerable to environmental tobacco smoke ex- posure: Evidence from biomarkers of tobacco- specific nitrosamines, and oxidative stress. Environ Int 2018; 120:238-245. DOI: 10.1016/j. envint.2018.08.006.
25. Zakhar J, Amrock SM, Weitzman M. Passive and Active Tobacco Exposure and Children’s Lipid Profiles. Nicotine Tob Res 2016; 18(5):982. DOI:
10.1093/ntr/ntv158
26. Ciria MA, Capote RA, Rodríguez SA, Sardiñas SY. Tabaquismo pasivo y recurrencia de crisis en niños asmáticos de edad escolar. Rev Cubana Med Gen Integr 2016; 32(2):191-201.
27. Sorroza RA, Barberan TJ, Cajas FN, Jinez H, López E, Rodríguez J. Neumonía adquirida en la comuni- dad asociada a tabaquismo pasivo en pediatría. Dom Cien 2018, 4(1):268-279.
28. Ordóñez-Iriarte JM, González-Estecha M, Guillén- Pérez J, Martínez-García MJ, Gaviña-Fernández- Montes B, Aparicio-Madre MI, Bodas-Pinedo A. Fac tores de riesgo asociados a los niveles de plomo en sangre de niños de la Comunidad de Madrid en 2010. Rev salud ambient 2013; 13(2):169-177.
29. Apostolou A, Garcia-Esquinas E, Fadrowski JJ, McLain P, Weaver V, Navas-Acien A. Secondhand Tobacco Smoke: A Source of Lead Exposure in US Children and Adolescents. Am J Pu- blic Health 2012; 102(4):714-22. DOI: 10.2105/ JPH.2011.300161
30. Protano C, Astolfi ML, Canepari S, Vittali M. Urinary levels of trace elements among primary school- aged children from Italy: The contribution of smoking habits of family members. Sci Total Environ 2016; 557–558:378–85. DOI: 10.1016/j. scitotenv.2016.03.073
31. Viroonudomphol D, Suwanton L, Pinyosirikul U, Satsue S, Harnroongroj T. Effect of Active and Passive Smoking on Heavy Metals Toxic and Antioxidant Trace Elements. J Med Biol Eng 2016;
5(1):58-62. DOI: 10.12720/jomb.5.1.58-62.
32. Jung SY, Kim S, Lee K, Kim JY, Bae WK, Lee K, Han JS, Kim S. Association between secondhand smoke exposure and blood lead and cadmium concentration in community dwelling women: the fifth Korea National Health and Nutrition Examination Survey (2010-2012). BMJ Open 2015;
5(7):e008218. DOI: 10.1136/bmjopen-2015-008218
33. García V, Rodrigo M. Pruebas de función tubular.Tubulopatías. Nefrología 2012; 7:0. DOI: 10.3265/ Nefrologia.2010.pub1.ed80.chapter2794
34. Aponte M, Rojas C, Moreno J, Piña T, Gonzalez Z, Paolini M, et al. Sobrepeso y obesidad en Vene- zuela. Prevalencia y factores condicionantes. Caracas: Gente de Maíz; 2011.
35. Mata-Meneses E, Moya-Sifontes M, Cordova M, Bauce G. Antropometría nutricional en escolares venezolanos. RAAB 2007; 9(2):29-50.
36. Castro C, Machado G, Palma D, Siqueira M, Silveira J, Alvarez E, Borbada J. Determination of cadmium in human urine by electrothermal atomic absorption spectrometry. Anal Chim A
2003; 491(2):231-237. DOI: https://doi.org/10.1016/ S0003-2670(03)00820-1
37. Hoet P, Jacquerye C, Deumer G, Lison D, Haufroid V. Reference values and upper reference limits for26 trace elements in the urine of adults living inBelgium. Clin Chem Lab Med 2013; 51(4):839-849.
38. Swaddiwudhipong W, Mahasakpan P, Jeekeeree W, Funkhiewa T, Sanjumb R, Apiwatpaiboon T, Phopueng I. Renal and blood pressure effects from environmental cadmium exposure in Thai children. Environ Res 2015; 136:82-87.
39. Instituto Nacional de Seguridad e Higiene en el Trabajo de España. Determinación de plomo en orina - Método de quelación-extracción/ Espectrofotometría de absorción atómica MTA/ MB-013/. Disponible en http://www.insht.es/Insht- Web/Contenidos/Documentacion/FichasTecnicas/ MetodosAnalisis/Ficheros/MB/MB_013_A87.pdf.
40. Inserra F, Angerosa M. Documento de Consenso: implicancia de la proteinuria en el diagnóstico y seguimiento de la enfermedad renal crónica. Acta Bioquím Clín Latinoam 2013; 47(3):0-0.
41. Alegre J, Alles A, Angerosa M, Bianchi M, Dorado E, Fayad A, et al. Implicancia de la proteinuria en el diagnóstico y seguimiento de la enfermedad renal crónica. Bioquim Patol Clín 2013; 77(2):34-45.
42. Chan PC, Kulasingamb V, Lem-Ragosniga B. Validating urinary measurement of beta-2-mi- croglobulin with a Roche reagent kit designed for serum measurements. Clin Biochem 2012;
45(16–17):1533–1535. DOI: 10.1016/j.clinbio- chem.2012.06.029
43. Ministerio del Poder Popular para Ciencia, Tecno- logía e Industrias Intermedias. Código de Bioética y Bioseguridad. Comisión de Bioética y Biose- guridad (CoBioBios). Tercera edición. Caracas, FONACIT; 2008.
44. Berlanga MR, Salazar G, García C, Hernández J. Maternal smoking effects on infant growth. Food Nutr Bull 2002; 23(3 Suppl):142-5.
45. Fenercioglu AK, Tamer I, Kratekin G, Nuhoglu A. Impaired Postnatal growth of infants prenatally exposed to cigarette smoking. Tohoku J Exp Med 2009; 218(3):221-8.
46. Baheiraei A, Shamsi A, Mohsenifar A, Kazemnejad A, Hatmi Z, Milani M, Keshavarz A. The effects of secondhand smoke exposure on infant growth: a prospective cohort study. Acta Med Iran 2015;
53(1):39-45.
47. Muraro AP, Gonçalves-Silva RM, Moreira NF, Ferrei- ra MG, Nunes-Freitas AL, Abreu-Villaça Y, Sichieri R. Effect of tobacco smoke exposure during preg- nancy and preschool age on growth from birth to adolescence: a cohort study. BMC Pediatrics
2014; 14(99). DOI: http://doi.org/10.1186/1471-2431-14-99.
48. Niu Z, Xie C, Wen X, Tian F, Ding P, He Y, et al. Pla- centa mediates the association between maternal second-hand smoke exposure during pregnancy and small for gestational age. Placenta 2015;
36(8):876-80. DOI: 10.1016
49. Wilson KM, Finkelstein JN, Blumkin AK, Best D, Klein JD. Micronutrient levels in children exposed to secondhand tobacco smoke. Nicotine Tob Res
2011; 13(9):800-8. DOI: 10.1093/ntr/ntr076
50. Leung TF, Chan I, Liu T, Lam C, WK, Wong G. Re- lationship between passive smoking exposure and urinary heavy metals and lung functions in preschool children. Pediatrics Pneumonol 2013;
48(11):1089-1097. DOI: 10.1002/ppul.22801
51. Moreira FR, Neves EB. Uso do chumbo em urina como indicador de exposição e sua relação com chumbo no sangue. Cad Saúde Púb 2008;
24(9):2151-2159.
2013; 10:E213. DOI:10.5888/pcd10.130056.
53. Gulson B, Cameron M, Smith A, Mizon K, Korsch M, Vimpani G, McMichael A, et al. Blood lead–urine lead relationships in adults and children. Envi- ron res Section A 1998; 78:152-160. DOI: 10.1006/ enrs.1997.3810
54. Ilmiawati C, Yoshida T, Itoh T, Nakagi Y, Saijo Y, Sugioka Y, Kayama F. Biomonitoring of mercury, cadmium, and lead exposure in Japanese chil- dren: a cross-sectional study. Environ Health Prev Med 2015; 20(1):18–27. DOI: 10.1007/s12199-014-
0416-4
55. Chaumont A, Voisin C, Deumer G, Haufroid V, Annesi-Maesano I, Roels H, et al. Associations of urinary cadmium with age and urinary proteins: further evidence of physiological variations unrelated to metal accumulation and toxicity. Environ Health Perspect 2013; 121:1047–1053. DOI: 10.1289/ehp.1306607.
56. Zubero MB, Aurrekoetxea JJ, Ibarluzea JM, Arenaza MJ, Basterretxea M, Rodríguez AC, et al. Metales pesados (Pb, Cd, Cr y Hg) en población general adulta próxima a una planta de tratamiento de residuos urbanos de Bizkaia. Rev Esp Salud Pública 2008; 82(5):481-492.
57. U.S. Department of Labor. Cadmium. Occupational Safety and Health Administration. OSHA 3136-08R; 2003.
58. European Food Safety Authority. Panel on Con- taminants in the Food Chain. Cadmium in food– Scientific opinion of the panel on contaminants in the Food Chain. EFSA J 2009, 2009:1–139.
59. Hibi Y, Uemura O, Nagai T, Yamakawa S, Yama- saki Y, Yamamoto M, et al. The ratios of urinary β2-microglobulin and NAG to creatinine vary with age in children. Pediatr Int 2015; 57:79–84. DOI: 10.1111/ped.12470.
2015; 39:35-41.
61. Lim H, Lim J, Choi JH, Kwon H, Ha M., Kim H, Park J. Associations of low environmental exposure to multiple metals with renal tubular impairment in korean adults. Toxicol Res 2016; 32(1):57–64.
62. Pegenaute C, Herrero S, Goncalves M, Alvarez I. Biomarcadores de nefrotoxicidad en trabajado- res expuestos a cadmio. Med Segur trab 2016; 62(244):263-281.
63. Cabrera WE, Behets G, Lamberts L, D´Haese P. Plomo y nefropatía. Biomarcadores urinarios enla detección de daño renal precoz. Rev Med Chile 2016; 144:704-709.
64. Di Carlo, MB, Gómez AG, Madalena LB, Facio ML, Pizzolato MA, Negri GA. Utilidad de la fosfatasa alcalina urinaria como marcador precoz de lesión tubular renal. Acta bioquim clín latinoam 2007; 41(3):369-377.
65. Vicente-Herrero M, Ramírez IM, Capdevila GL, Te- rradillos GM, López-González A, Aguilar JE, et al. Exposoma: un nuevo concepto en Salud Laboral y Salud Pública. Rev Asoc Esp Espec Med Trab 2016; 25(3):176-183.
66. Rappaport SM. Implications of the exposome for exposure science. J Expo Sci Environ Epidemiol 2011; 21:5-9.
67. Chung M, Kannan K, Louis G, Patel Ch. Toward capturing the exposome: Exposure biomark- er variability and coexposure patterns in the shared environment. Environ Sci Technol 2018; 52(15):8801-8810. DOI: 10.1021/acs.est.8b01467
68.Wang RY, Caldwell KL, Jones RL. Analytical con- siderations in the clinical laboratory assessment of metals. J Med Toxicol 2014; 10(2):232–239. DOI: 10.1007/s13181-014-0381-8.
![]()