Biomarcadores en la detección temprana de Cardiotoxicidad Inducida por quimioterapia; estado actual
Evert Armando Jiménez Cotes*, Wendy Sofía Meyer Martínez**, Daniel Gallego González***
Archivos de Medicina (Manizales), Volumen 15 N° 1, Enero-Junio 2015, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Jiménez Cotes E.A.; Meyer Martínez W.S.; Gallego González D.
* Estudiante de Internado, Facultad de medicina, Universidad Pontificia Bolivariana. Correo e: evertarmando.jimenez@upb.edu.co
** Estudiante de Internado, Facultad de medicina, Universidad Pontificia Bolivariana. Correo e: wendysofia.meyer@upb.edu.co
*** Estudiante de Pregrado. Facultad de medicina, Universidad Pontificia Bolivariana. Corre e: daniel.gallegogo@upb.edu.co
Recibido para publicación: 05-11-2014 - Versión corregida: 08-05-2015 - Aprobado para publicación: 11-05-2015
Resumen
Actualmente la cardiotoxicidad por quimioterapia es considerada como el “Talón de Aquiles” en el manejo de los pacientes con cáncer, debido a que afecta fuertemente la calidad de vida y supervivencia, independientemente del pronóstico oncológico. Los mecanismos moleculares por los cuales se produce la cardiotoxicicidad dependen de la selectividad de los medicamentos antineoplásicos por las quinasas, el daño celular mediado por radicales libres de oxígeno y la inducción de reacciones inmunológicas. La ecocardiografía ha sido el método diagnóstico de elección durante muchos años, sin embargo, los cambios aparecen sólo cuando se ha producido una disfunción miocárdica significativa, es por esto que los biomarcadores surgen como una novedosa estrategia de tamizaje temprano, con el propósito de modular la terapia antineoplásica de manera oportuna y evitar la progresión de la toxicidad cardiaca. El objetivo del presente artículo es realizar una revisión del estado del arte de aquellos biomarcadores de cardiotoxicidad inducida por quimioterapia reportados en la literatura, además de hacer una síntesis de los diferentes efectos cardiotóxicos, mecanismos de cardiotoxicidad y métodos que se han desarrollado para su diagnóstico.
Palabras clave: marcadores biológicos, toxicidad, quimioterapia, insuficiencia cardiaca.
Jiménez-Cotes EA, Meyer-Martínez WS, Gallego-González D. Biomarcadores en la detección temprana de Cardiotoxicidad Inducida por quimioterapia; estado actual. Arch Med (Manizales) 2015; 15(1):126-37.
Biomarkers in the early detection of chemotherapy-induced cardiotoxicity; current state
Summary
Currently cardiotoxicity induced by chemotherapy is considered as the “Achilles’ Heel” in the management of patients with cancer, because it strongly affects the quality of life and survival of patients, regardless of cancer prognosis. The molecular mechanisms of cardiotoxicity depend of the selectivity of the anticancer drugs against the kinases, the cell damage mediated by oxygen free radicals and the induction of immunological reactions. Echocardiography was the diagnostic method of choice for many years, however, the changes appear only when a significant myocardial dysfunction has occurred, which is why biological markers are emerging as a novel early screening strategy, in order to modulate antineoplastic therapy in a timely manner and prevent the progression of cardiac toxicity. The aim of this article is to review the state of the art of those biomarkers of cardiotoxicity induced by chemotherapy reported in the literature, in addition to a summary of various cardiotoxic effects, mechanisms of cardiotoxicity and diagnosis methods that have been developed.
Keywords: biological markers, toxicity, drug therapy, heart failure.
Introducción
La cardiotoxicidad por quimioterapia hace referencia a las lesiones miocárdicas relacionadas con la aplicación de terapias farmacológicas antineoplásicas1, la cual era considerada hace unas décadas como una complicación poco frecuente y de baja importancia en la práctica clínica oncológica, a pesar de ser un efecto adverso ampliamente conocido desde 1967, cuando se reportaron los primeros casos de falla cardíaca en niños con leucemia que recibían altas dosis de doxorrubicina2,3; hasta que se comprobó que los medicamentos como el imatinib, cuyos blancos moleculares eran receptores tumorales o ciertas tirosinquinasas, tenían efectos adversos directos sobre el sistema cardiovascular4,5. En los últimos años, la detección y tratamiento de las enfermedades oncológicas mediante quimioterapia ha aumentado progresivamente, al igual que sus novedosas drogas con alta agresividad anti-neoplásica6. Pero estas últimas a su vez, han aumentado la incidencia de cardiotoxicidad, la cual afecta la calidad de vida, el pronóstico y la sobrevida de los pacientes oncológicos7,8. Es por esto que hoy en día es más común la coexistencia de cáncer y enfermedades cardiovasculares en un mismo paciente9.
Diversos estudios han demostrado que ciertos anticuerpos y medicamentos antineoplásicos como las antraciclinas, el trastuzumab y el 5-fluorouracilo (5-FU), se asocian con el desarrollo de insuficiencia cardíaca hasta en un 20% de los pacientes en tratamiento quimioterapéutico10,11. Debido a lo anterior, las personas que inician quimioterapia son clasificadas dentro del estadio A de falla cardiaca, estas tienen un mayor riesgo de desarrollar disfunción ventricular12. Además, el riesgo de muerte cardiovascular es mayor que el riesgo real de recurrencia tumoral10,13.
Para dimensionar esta problemática, es importante comprender que la toxicidad cardiovascular como consecuencia de los tratamientos suministrados durante la quimioterapia comprende un amplio grupo de enfermedades cardiacas tales como miocarditis, pericarditis, enfermedades tromboembólicas, isquemia vaso espástica, alteraciones electrocardiográficas como arritmias, prolongación del intervalo QT, entre otras2,4,11, las cuales se clasifican como agudas o subagudas debido a que se manifiestan al iniciar la quimioterapia o hasta dos semanas después de finalizado el tratamiento, además de otras enfermedades crónicas como hipertensión arterial, síndrome coronario agudo y cardiomiopatías, las cuales inician hasta un año después de terminada la quimioterapia6 (Figura 1). Todos éstos son considerados efectos secundarios que tienen como punto final la disminución de la función ventricular izquierda8-10,13-15.
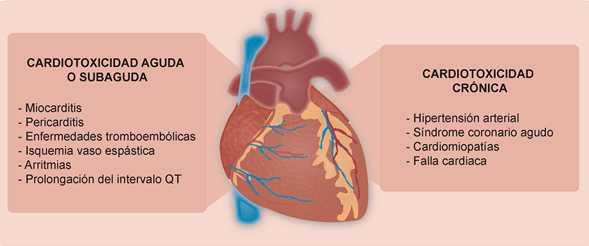
Figura 1. Manifestaciones clínicas de cardiotoxicidad inducida por antineoplásicos.
Fuente: Autores.
Adicionalmente, muchas de las vías moleculares que son utilizadas como blancos terapéuticos en oncología, con frecuencia son las mismas vías bioquímicas cardio-protectoras, lo cual hace imprescindible la búsqueda de nuevas estrategias diagnósticas así como el desarrollo de biomarcadores, que permitan una detección temprana de estos efectos adversos, para poder realizar medidas preventivas antes de la aparición de complicaciones y secuelas. El objetivo del presente texto es realizar una revisión del estado del arte de aquellos biomarcadores de cardiotoxicidad por quimioterapia reportados en la literatura, además de hacer una síntesis de los diferentes efectos cardiotóxicos, mecanismos de cardiotoxicidad y los métodos que se han desarrollado para su diagnóstico.
Efectos cardiotóxicos y mecanismos de cardiotoxicidad por quimioterapia
Dentro de todos los medicamentos antineoplásicos que se han identificado por sus efectos adversos sobre el sistema cardiovascular, las antraciclinas como la doxorrubicina, epirrubicina y la daunorrubicina, son las que tienen un mayor impacto clínico debido a sus potentes efectos cardiotóxicos, por lo que su uso terapéutico se limita frecuentemente4,6. Otros fármacos citotóxicos que han sido asociados a cardiotoxicidad son el 5-FU, busulfan, capecitabina, ciclofosfamida, cisplatino, dacarbamazina, fludarabina, mecloretamina, melfalan, mitoxantrona, mitomicina, taxoides como paclitaxel y docetaxel, además de anticuerpos monoclonales como el trastuzumab y el rituximab2,6,11 (Figura 2). Los mecanismos de inducción de cardiotoxicidad incluyen el daño celular debido a la formación de radicales libres de oxígeno, inducción de reacciones inmunogénicas por la presencia de células presentadoras de antígeno en el corazón y la influencia de los agentes citotóxicos sobre ciertos fosfolípidos, especialmente la cardiolipina, entre otros11.
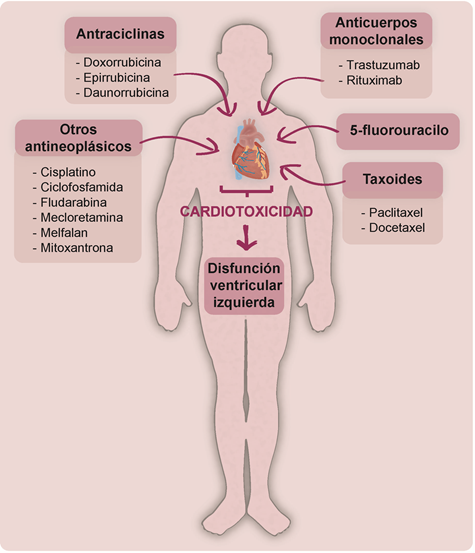
Figura 2. Medicamentos antineoplásicos con efectos cardiotóxicos.
Fuente: Autores.
Lal5 et al publicaron en el 2013 la existencia de dos tipos generales de cardiotoxicidad, dependiendo del blanco molecular sobre el cual actúan los medicamentos antineoplásicos y su selectividad. De esta forma, se habla de “toxicidad en el blanco” cuando los fármacos como el sorafenib, atacan selectivamente quinasas del cáncer que también proporcionan una función importante a nivel cardiovascular; mientras que la “toxicidad fuera del blanco”, se produce por fármacos como el sunitinib, que son poco selectivos e inhiben hasta 90 quinasas, atacando tanto al cáncer como al corazón5.
También se ha evidenciado que el riesgo de cardiotoxicidad por quimioterapia se aumenta por factores como la edad, predisposición genética, antecedente de radioterapia, administración concomitante con otros fármacos de quimioterapia, enfermedad cardiaca subyacente y dosis acumulativas del medicamento4. A continuación se describen algunos de los agentes citotóxicos más implicados, sus mecanismos de toxicidad y algunos factores de riesgo reportados en la literatura.
Antraciclinas
En pacientes tratados con antraciclinas se ha reportado cardiomiopatía, insuficiencia cardiaca congestiva y alteraciones electrocardiográficas tales como cambios inespecíficos en el segmento ST, disminución del voltaje del complejo QRS y prolongación del intervalo QT6. Estos efectos pueden ser a corto, mediano o largo plazo, dependiendo de si se manifiestan al iniciar la terapia, un año después, o incluso tras 20 años de haber completado el tratamiento4. La administración de dosis acumulativas de antraciclina es el factor de riesgo más significativo, pues a dosis mayores de 450-550mg/m2 los pacientes presentan frecuentemente insuficiencia cardiaca congestiva y cardiomiopatía11. Otros factores de riesgo identificados para estos fármacos son la tasa de dosis, posología, tratamiento concomitante con otros antineoplásicos y análogos cardiotóxicos, los cuales se pueden modificar, además de agregar un agente cardioprotector para disminuir estas complicaciones cardiovasculares6.
Las antraciclinas aumentan la concentración de radicales libres al ser metabolizados enzimáticamente, lo que conduce a la destrucción de las mitocondrias y muerte del miocito4 (Figura 3). Sin embargo, la susceptibilidad de las células cardiacas al estrés oxidativo depende de la disminución en los niveles de enzimas cardiacas antioxidantes11. Dependiendo de las dosis de doxorrubicina, las concentraciones de radicales libres inducen necrosis o activación de vías apoptóticas, a partir de las proteínas Bax, citocromo c y caspasa-34. Se ha encontrado que a concentraciones bajas del fármaco prevalecen los mecanismos de apoptosis, mientras que ha dosis altas predomina la necrosis11. Una investigación publicada en el 2013 por Herger16 et al demostró in-vitro por medio de cromatografía líquida de intercambio iónico, que la doxorrubicina induce cambios directamente sobre algunos aminoácidos del miocardio, tales como lisina, arginina, β-alanina, valina y serina, incluso a bajas concentraciones, lo que confirma la cardiotoxicidad inducida por ese fármaco16.
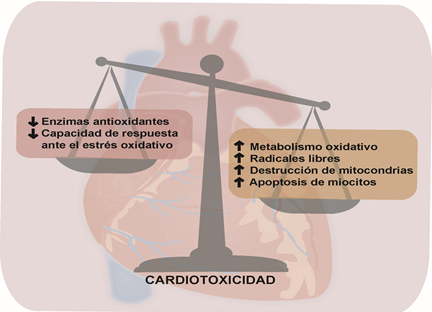
Figura 3. Mecanismo de cardiotoxicidad inducido por antineoplásicos como las antraciclinas. Fuente: Autores.
Otros mecanismos de cardiotoxicidad inducidos por antraciclinas, se basan en la disrupción de la estructura de la sarcómera miocárdica4; inhibición de la peroxidación lipídica cardiaca, que conduce al aumento de radicales libres; alteración del transporte mitocondrial del calcio, lo cual conduce a muerte celular, lesión tisular y deterioro de la contracción cardiaca; y en el incremento de la respuesta autoinmune activada a partir del daño de la membrana citoplasmática de los miocitos11.
Taxoides
Por su parte, los taxoides como el paclitaxel y el docetaxel, también producen diversos efectos cardiotóxicos tras su administración. En el caso del paclitaxel, combinado o no con cisplatino, desencadena en algunos pacientes trastornos cardíacos consistentes en bradi o taquiarritmias, bloqueos aurículoventriculares y de rama, isquemia cardiaca e hipotensión11. La formulación de paclitaxel usada clínicamente es una mezcla que contiene el adyuvante Cremofor EL, el cual también se asocia con cardiotoxicidad, nefrotoxicidad y reacciones de hipersensibilidad17. Los factores de riesgo que predisponen a toxicidad cardiaca comprenden la angina inestable, enfermedades coronarias severas, insuficiencia cardiaca congestiva y fibrilación auricular11.
Ciclofosfamida
En cuanto a la ciclofosfamida, un agente alquilante del grupo de las oxazoforinas, se ha reportado que a altas dosis produce efectos agudos tales como pericarditis, descompensación cardiaca y cardiomiopatía en tan sólo 10 días de haber iniciado su administración2. También se presenta en algunos pacientes una disminución de la función sistólica y al igual que las antraciclinas, incrementa las concentraciones intracelulares de radicales libres de oxígeno11.
Fluorouracilo
Se estima que del 1 al 18% de los pacientes tratados con 5-FU, un antimetabolito de uridina, presentan cardiotoxicidad, la cual es más frecuente cuando se administra en infusión continua2,11. Estos pacientes presentan arritmias cardiacas, isquemia miocárdica, angina, insuficiencia cardiaca congestiva y muerte súbita11, siendo la angina el síntoma más frecuente durante las primeras horas del inicio de la terapia18. Con la forma oral del 5-FU, la capecitabina, también se reporta una alta tasa de toxicidad a pesar de que el fármaco actúa selectivamente sobre el tumor19. La tasa de mortalidad del 2,2 al 13% durante el seguimiento del tratamiento con altas dosis de 5-FU, demuestra cuán peligroso pueden ser estos efectos adversos18.
Cisplatino
A su vez, se ha reportado que algunos pacientes tratados con cisplatino desarrollan infarto agudo de miocardio. En algunos estudios se ha postulado que estos efectos adversos del cisplatino se deben a daños vasculares, activación de la agregación y de la vía del ácido araquidónico plaquetaria e hipomagnesemia11.
Trastuzumab
Para la terapia del cáncer de mama se cuenta con un anticuerpo monoclonal, el trastuzumab, el cual actúa directamente contra la proteína receptora 2 del factor de crecimiento epidérmico humano (HER2). La cardiotoxicidad asociada a su administración es similar a la que se presenta en los pacientes tratados con antraciclina, la cual se manifiesta con insuficiencia cardiaca congestiva11. El riesgo a padecer serios eventos adversos cardiacos tras el tratamiento con trastuzumab es mayor en pacientes con factores de riesgo preexistentes18.
Diagnóstico y monitoreo de cardiotoxicidad
Para el monitoreo de los pacientes que se encuentran en tratamiento oncológico con quimioterapia, se deben realizar rutinariamente estudios imaginológicos del corazón para identificar la disfunción miocárdica clínica o subclínica. La evaluación periódica de la función cardiaca por medio de ecocardiografía transtorácica es el método diagnóstico no invasivo más utilizado en la práctica clínica oncológica para la medición de cardiotoxicidad en pacientes con quimioterapia, la cual se evidencia por medio de disminución de la fracción de eyección ventricular izquierda (FEVI)18. Sin embargo, el estándar de oro en el diagnóstico sigue siendo la biopsia endomiocárdica, ya que permite medir directamente la presencia y extensión de fibrosis cardiaca debido a quimioterapia20,21.
La Sociedad Europea de Oncología recomienda la medición de la FEVI al comienzo de la terapia antineoplásica en pacientes mayores de 60 años o con factores de riesgo cardiovasculares, luego de la administración de la mitad de la dosis acumulativa total de antraciclinas, antes de las siguientes dosis y a los 3, 6 y 12 meses después de finalizado el tratamiento quimioterapéutico9,22. Cuando se presenta una disminución mayor del 10% asociado a un valor absoluto de FEVI menor del 50%, se recomienda la suspensión de la terapia antineoplásica23,24, debido a que diversos estudios han demostrado que la presencia de cambios en la FEVI se asocian con insuficiencia cardiaca crónica 3 años después de finalizada la quimioterapia25.
Por otra parte, el electrocardiograma de 12 derivaciones que presenta trastornos en la repolarización, disminución del voltaje del complejo QRS (indicativo de cardiomiopatía) y prolongación del intervalo QT en aquellos pacientes con extensos tratamientos con antraciclinas, se ha postulado como un marcador temprano de disfunción ventricular izquierda26-28; sin embargo, estos métodos diagnósticos subestiman el daño cardiaco, son operador dependiente y los cambios sugestivos por cardiotoxicidad sólo aparecen cuando ya se ha producido una disfunción miocárdica significativa, lo que limita la intervención farmacológica temprana. Por lo tanto, se han propuesto otros métodos y técnicas en búsqueda de una detección precisa y oportuna de la cardiotoxicidad inducida por quimioterapia9.
Actualmente, los avances en ecocardiografía tridimensional, doppler tisular, imágenes de velocidad de deformación cardiaca y resonancia magnética cardiaca parecen ser prometedores en la detección de cambios subclínicos29-32.
Biomarcadores de cardiotoxicidad por quimioterapia
La medición de biomarcadores séricos específicos de injuria miocárdica ha sido propuesta como una estrategia atractiva, válida y novedosa en la identificación y monitoreo de cardiotoxicidad en pacientes tratados con quimioterapia, debido a su relativa facilidad de uso, capacidad de predicción, precisión y exactitud9,33,34. Los principales marcadores séricos son la Troponina, el BNP y NT-proBNP17.
La Troponina está compuesta por tres subunidades de proteínas (Troponina C, I, y T) que se encuentran a lo largo del filamento delgado del músculo estriado cardiaco, regulando el proceso de contracción miocárdica mediada por el calcio. En los últimos años, estas proteínas se han posicionado como marcadores de injuria miocárdica, por lo que son medidos comúnmente en la práctica clínica35. Recientemente se han publicado varios estudios que apoyan el uso de Troponina I (TnI) ultrasensible como biomarcardor predictivo de cardiotoxicidad para suspender la terapia con antraciclinas36, con una alta sensibilidad (82%) y especificidad (77%), y un valor predictivo positivo cercano al 84%, todo esto, en relación a la dosis acumulativa de quimioterapia, una mayor reducción de la FEVI y presencia de eventos cardiovasculares33,37-42.
Este biomarcador fue inicialmente estudiado en ratas expuestas a fármacos antineoplásicos, a través de las cuales se evidenció la relación entre la dosis acumulada de citotóxicos y la injuria cardiaca40,41,43. Otros reportes en niños con leucemia demostraron un incremento de los niveles de Troponina T (TnT) en el 30% de los pacientes en tratamiento con antraciclinas hasta por tres meses después de finalizado el tratamiento antineoplásico, asociándose con el desarrollo de disfunción ventricular a mediano plazo44. Los pacientes con TnI-positiva presentan una mayor incidencia de eventos cardiovasculares y la persistencia de niveles elevados después de un mes de terminada la quimioterapia se asocia con un mayor deterioro de la funcionalidad cardíaca y mayor incidencia de eventos adversos en comparación con aquellos pacientes que sólo muestran un aumento transitorio de este biomarcador45. Sin embargo, la gran utilidad de la Troponina para evaluar cardiotoxicidad se debe a su alto valor predictivo negativo de aproximadamente 99%, por lo tanto aquellos pacientes que no presentan niveles positivos de TnI después del tratamiento con citotóxicos, se consideran de bajo riesgo, con pronóstico favorable y con una reducción significativa de los eventos cardiovasculares durante al menos 1 año posterior al tratamiento6,33,39,46-48.
Otro de los marcadores séricos estudiados en insuficiencia cardiaca son el péptido natriurético cerebral (BNP, por sus siglas en inglés) y su precursor el NT-proBNP que aparece en etapas tempranas de disfunción diastólica, característica de la cardiomiopatía por citotóxicos. Múltiples estudios han reportado resultados variables en cuanto a la posible asociación directa con cardiotoxicidad al parecer debido a los diferentes métodos de medición de los péptidos, falsos positivos y altos costos6,49,50. Algunas investigaciones han demostrado pequeñas elevaciones en los niveles de BNP posterior al tratamiento con antraciclinas, asociándose a una mayor disfunción diastólica, mientras que otros estudios fracasaron al intentar establecer la utilidad de los péptidos como biomarcadores de cardiotoxicidad51. Los primeros estudios en pacientes con quimioterapia, tratados principalmente con antraciclinas, demostraron que la elevación persistente de BNP se relacionaba con el desarrollo de disfunción ventricular52 y a pesar de que la mayoría de los estudios publicados en los últimos años sugieren que el aumento en los niveles de BNP es predictivo para el desarrollo de insuficiencia cardíaca, la heterogeneidad de los datos hace difícil la comparación de los resultados, impidiendo sacar conclusiones definitivas o indicaciones objetivas acerca del uso rutinario de este biomarcador en la práctica clínica53.
La búsqueda de biomarcadores de disfunción endotelial parece ser una nueva alternativa en la estratificación de pacientes en riesgo de eventos vasculares, debido a su papel en los procesos inflamatorios ateroscleróticos. En el 2004 se publicó un estudio que reportó el aumento de los niveles del Factor inhibidor tipo 1 del activador del plasminógeno (PAI-1) y del activador de plasminógeno de tipo tisular (tPA) en pacientes con cáncer testicular diseminado. Posteriormente, se reportó que la bleomicina y el cisplatino inducen alteraciones en la función de las células endoteliales, con respecto a la proliferación, inflamación y fibrinólisis, debido al aumento in vitro de la apoptosis de células endoteliales micro-vasculares HMEC-1 y a una sobrerregulación de las moléculas de adhesión intercelular tipo 1 (ICAM-1)54. Sin embargo, en la actualidad no se ha demostrado una correlación objetiva con el desarrollo de eventos cardiovasculares a largo plazo, al igual que el papel predictivo de estos marcadores.
Los avances en proteómica han permitido identificar ciertas proteínas relacionadas con disfunción ventricular izquierda, tales como la proteína de unión de ácidos grasos (FABP) la cual participa en el metabolismo y transferencia intracelular de los ácidos grasos. Ésta se ha propuesto recientemente como un nuevo biomarcador de isquemia y necrosis miocárdica55-57, debido a que es liberada de las células miocárdicas al torrente sanguíneo después 2 a 4 horas de la lesión isquémica, y retorna a los valores normales en un periodo de 18 a 36 horas57. En el año 2009 se reportó que los pacientes en quimioterapia con una FEVI menor del 50% presentaban niveles más altos de FABP en comparación con aquellos sin evidencia de disfunción cardiaca58. Sin embargo estos marcadores no son muy específicos, por lo que se requieren nuevos estudios que avalen su utilidad clínica.
A su vez, el uso combinado de biomarcadores parece ser otra alternativa atractiva en la evaluación de cardiotoxicidad por quimioterapia. Recientemente se publicaron los resultados de una cohorte de 78 pacientes con cáncer de mama tratados con doxoburricina y trastuzumab en los que se evaluaron múltiples biomarcadores y su utilidad predictiva tanto individual como en combinación. El análisis combinado de TnI y mieloperoxidasa presentó una mejor utilidad conjunta en la predicción de cardiotoxicidad, con un Hazard Ratio (HR) de 1,38 y 1,34 respectivamente, lo cual ofrece una información adicional del riesgo de cardiotoxicidad59.
La farmacogenómica ha surgido como un potencial campo de estudio de biomarcadores de disfunción cardiaca inducida por quimioterapia60. Los polimorfismos en genes específicos implicados en la biotransformación de medicamentos fueron evaluados en 156 niños, encontrándose múltiples variantes genéticas en SLC28A3 y otros genes asociados a cardiotoxicidad inducida por antraciclinas, lo cual sugiere que factores clínicos de riesgo combinados con perfiles genéticos podrían utilizarse para identificar a aquellos pacientes de alto riesgo que luego pueden ser intervenidos de manera preventiva y oportuna, evitando el desarrollo futuro de cardiotoxicidad durante o después de la terapia oncológica60,61.
Conclusión
En los últimos años, los avances en el tratamiento y desarrollo de nuevos fármacos antineoplásicos han logrado aumentar la sobrevida y la remisión de algunos tipos de cáncer. Es así como las enfermedades neoplásicas han pasado de ser entidades agudas con alta morbi mortalidad, a patologías crónicas, en algunos casos tratables, que han obligado a redireccionar las estrategias preventivas de efectos adversos asociados al tratamiento. Los pacientes con cáncer constituyen un grupo especial de riesgo, no solo por las complicaciones inherentes a su patología neoplásica, las cuales predisponen al desarrollo de eventos cardiovasculares, sino también por los efectos adversos de la quimioterapia y las comorbilidades asociadas a los estilos de vida, como lo es el consumo de tabaco, alcohol, malos hábitos dietarios, obesidad, entre otros. Por lo tanto, ante una estrategia antitumoral debe igualmente considerarse una estrategia global de tamizaje y de protección cardiovascular.
El conocimiento acerca de la incidencia y el mecanismo de cardiotoxicidad de estos medicamentos es fundamental dentro de la práctica clínica, para ofrecer un manejo médico óptimo y garantizar un buen pronóstico de vida a los pacientes que reciben quimioterapia. La identificación precoz de los pacientes en estadios subclínicos y de aquellos con alto riesgo de presentar disfunción ventricular, es la estrategia que se debe adoptar para poder definir el tipo de seguimiento e intervenir oportunamente antes del desarrollo de disfunción contráctil irreversible.
El grupo de las antraciclinas presenta el mayor riesgo de cardiotoxicidad, por lo que la sospecha diagnóstica y el seguimiento debe ser más minucioso en el grupo de pacientes tratados con estos medicamentos. El uso de biomarcadores, en especial la troponina con su alto valor predictivo negativo, permite estratificar a los pacientes que no requieren de un seguimiento estricto de cardiotoxicidad, disminuyendo el uso de métodos diagnósticos innecesarios, los costos para el sistema de salud y para los pacientes. Aunque se ha enfatizado en estrategias para prevenir la cardiotoxicidad, no existe un consenso acerca de cuál es la manera más efectiva para abordar a estos pacientes. Es por esto que se requiere de nuevos estudios prospectivos que incluyan grandes cohortes de pacientes y que utilicen métodos validados y comercialmente disponibles para la tamización, con biomarcadores que permitan hacer una mejor clasificación y estratificación del riesgo de cardiotoxicidad; además de diseñar herramientas para su tratamiento oportuno.
Literatura citada
1. Khouri MG, Douglas PS, Mackey JR, Martin M, Scott JM, Scherrer-Crosbie M, et al. Cancer therapy-induced cardiac toxicity in early breast cancer: addressing the unresolved issues. Circulation 2012; 126(23):2749-63.
2. Gharib MI, Burnett AK. Chemotherapy-induced cardiotoxicity: current practice and prospects of prophylaxis. Eur J Heart Fail 2002; 4(3):235-42.
3. Navarrete S, Castellanos A, Chaparro A. Cardiotoxicidad por quimioterapia. Un enfoque práctico para el clínico. Insuf Card 2011; 6(3):131-143.
4. Raschi E, Vasina V, Ursino MG, Boriani G, Martoni A, De Ponti F. Anticancer drugs and cardiotoxicity: Insights and perspectives in the era of targeted therapy. Pharmacol Ther 2010; 125(2):196-218.
5. Lal H, Kolaja KL, Force T. Cancer genetics and the cardiotoxicity of the therapeutics. J Am Coll Cardiol 2013; 61(3):267-74.
6. Dolci A, Dominici R, Cardinale D, Sandri MT, Panteghini M. Biochemical markers for prediction of chemotherapy-induced cardiotoxicity: systematic review of the literature and recommendations for use. Am J Clin Pathol 2008; 130(5):688-95.
7. Jensen BV. Cardiotoxic consequences of anthracycline-containing therapy in patients with breast cancer. Semin Oncol 2006; 33(3 Suppl 8):S15-21.
8. Suter TM, Ewer MS. Cancer drugs and the heart: importance and management. Eur Heart J 2013; 34 (15):1102-11.
9. Todaro MC, Oreto L, Qamar R, Paterick TE, Carerj S, Khandheria BK. Cardioncology: state of the heart. Int J Cardiol 2013; 168(2):680-7.
10. Yeh ET. Cardiotoxicity induced by chemotherapy and antibody therapy. Annu Rev Med 2006; 57:485-98.
11. Schimmel KJ, Richel DJ, van den Brink RB, Guchelaar HJ. Cardiotoxicity of cytotoxic drugs. Cancer Treat Rev 2004; 30(2):181-91.
12. Bonow RO, Bennett S, Casey DE, Ganiats TG, Hlatky MA, Konstam MA, et al. ACC/AHA Clinical Performance Measures for Adults with Chronic Heart Failure: a report of the American College of Cardiology/American Heart Association Task Force on Performance Measures (Writing Committee to Develop Heart Failure Clinical Performance Measures): endorsed by the Heart Failure Society of America. Circulation 2005; 112(12):1853-87.
13. Hanrahan EO, Gonzalez-Angulo AM, Giordano SH, Rouzier R, Broglio KR, Hortobagyi GN, et al. Overall survival and cause-specific mortality of patients with stage T1a,bN0M0 breast carcinoma. J Clin Oncol 2007; 25(31):4952-60.
14. Yeh ET, Bickford CL. Cardiovascular complications of cancer therapy: incidence, pathogenesis, diagnosis, and management. J Am Coll Cardiol 2009; 53(24):2231-47.
15. Altena R, Perik PJ, van Veldhuisen DJ, de Vries EG, Gietema JA. Cardiovascular toxicity caused by cancer treatment: strategies for early detection. Lancet Oncol 2009; 10(4):391-9.
16. Herger Z, Cernei N, Kudr J, Gumulec J, Blazkova I, Zitka O. A Novel Insight into the Cardiotoxicity of Antineoplastic Drug Doxorubicin. Int J Mol Sci 2013; 14:21629-46.
17. Martins K, MessiasII A, LeiteI F, Duek E. Preparation and characterization of paclitaxel-loaded PLDLA microspheres. Mat Res 2014; 17(3):650-56.
18. Schlitt A, Jordan K, Vordemark D, Schwanborn J, Langer T, Thomssen C. Cardiotoxicity and oncological treatments. Dtsch Arztebl Int 2014; 111(10):161-8.
19. Endo A, Yoshida Y, Nakashima R, Takahashi N, Tanabe K. Capecitabine induces both cardiomyopathy and multifocal cerebral leukoencephalopathy. Int Heart J 2013; 54(6):417-20.
20. Cooper LT, Baughman KL, Feldman AM, Frustaci A, Jessup M, Kuhl U, et al. The role of endomyocardial biopsy in the management of cardiovascular disease: a scientific statement from the American Heart Association, the American College of Cardiology, and the European Society of Cardiology. Circulation 2007; 116(19):2216-33.
21. Isner J, Ferrans V, Cohen S, Witkind B, Virmani R, Gottd-iener J, et al. Clinical and morphologic cardiac findings after anthracycline chemotherapy Analysis of 64 patients studied at necropsy. Am J Cardiol 1983; 51(7):1167-74.
22. Bovelli D, Plataniotis G, Roila F. Cardiotoxicity of chemothera-peutic agents and radiotherapy-related heart disease: ESMO Clinical Practice Guidelines. Ann Oncol 2010; Suppl 5:v277-v282.
23. Schwartz RG, McKenzie WB, Alexander J. Congestive heart failure and left ventricular dysfunction complicating doxorubicin therapy: seven-year experience using serial radionuclide angiocardiography. Am J Med 1987; 82(6):1109-18.
24. Eidem BW. Identification of anthracycline cardiotoxicity: left ventricular ejection fraction is not enough. J Am Soc Echocardiogr 2008; 21:1290-2.
25. Mitani I, Jain D, Joska TM. Doxorubicin cardiotoxicity: prevention of congestive heart failure with serial cardiac function monitoring with equilibrium radionuclide angiocardiography in the current era. J Nucl Cardiol 2003; 10:132-39.
26. Horacek JM, Jakl M, Horackova J, Pudil R, Jebavy L, Maly J. Assessment of anthracycline- induced cardiotoxicity with electrocardiography. Exp Oncol 2009; 31:115-7.
27. Jannazzo A, Hoffman J, Lutz M. Monitoring of anthracycline-induced cardiotoxicity. Ann Pharmacother 2008; 42:99-104.
28. Nakamae H, Tsumura K, Akahori M. QT dispersion correlates with systolic rather than diastolic parameters in patients receiving anthracycline treatment. Intern Med 2004; 43:379-87.
29. Tassan-Mangina S, Codorean D, Metivier M. Tissue Doppler imaging and conventional echocardiography after anthracycline treatment in adults: early and late alterations of left ventricular function during a prospective study. Eur J Echocardiogr 2006; 7:141-6.
30. Jurcut R, Wildiers H, Ganame J, D’hooge J, Paridaens R, Voigt JU. Detection and monitoring of cardiotoxicity - what does modern cardiology offer? Support Care Cancer 2008; 16:437-45.
31. de Geus-Oei LF, Mavinkurve-Groothuis AM, Bellersen L, et al. Scintigraphic techniques for early detection of cancer treatment-induced cardiotoxicity. J Nucl Med 2011; 52:560-71.
32. Hundley WG, Bluemke DA, Finn JP. American College of Cardiology Foundation Task Force on Expert Consensus Documents, ACCF/ACR/AHA/ NASCI/SCMR 2010 expert consensus document on cardiovascular magnetic resonance: a report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents. J Am Coll Cardiol 2010; 55:2614-62.
33. Cardinale D, Sandri MT, Colombo A, Colombo N, Boeri M, Lamantia G, et al. Prognostic value of Troponin I in cardiac risk stratification of cancer patients undergoing high-dose chemotherapy. Circulation 2004; 109:2749-54.
34. Vasan RS. Biomarkers of cardiovascular disease: molecular basis and practical considerations. Circulation 2006; 113(19):2335-62.
35. Panteghini M. The new definition of myocardial infarction and the impact of troponin determination on clinical practice. Int J Cardiol 2006; 106:298-306.
36. Sawaya H, Sebag IA, Plana JC, Januzzi JL, Ky B, Tan TC, et al. Assessment of echocardiography and biomarkers for the extended prediction of cardiotoxicity in patients treated with anthracyclines, taxanes, and trastuzumab. Circ Cardiovasc Imaging 2012; 5(5):596-603.
37. Sandri MT, Cardinale D, Zorzino L, Passerini R, Lentati P, Martinoni A, et al. Minor increases in plasma troponin I predict decreased left ventricular ejection fraction after high-dose chemotherapy. Clin Chem 2003; 49(2):248-52.
38. JESC/ACC Committee. Myocardial infarction redefined - a consensus document of the Joint European Society of Cardiology/American College of Cardiology Committee for the redefinition of myocardial infarction. Eur Heart J 2000; 21:1502-13.
39. Cardinale D, Sandri MT. Role of biomarkers in chemotherapy-induced cardiotoxicity. Prog Cardiovasc Dis 2010; 53:121-9.
40. Mavinkurve A, Kapusta L, Nir A, Groot J. The role of biomarkers in the early detection of anthracycline-induced cardiotoxicity in children: a review of the literature. J Pediatr Hematol Oncol 2008; 25(7):655-64.
41. Pongprot Y, Sittiwangkul R, Charoenkwan P, Silvilairat S. Use of cardiac markers for monitoring of doxorubixin-induced cardiotoxicity in children with cancer. J Pediatr Hematol Oncol 2012; 34:589-95.
42. Cardinale D, Sandri MT, Martinoni A, Tricca A, Civelli M, Lamantia G, et al. Left ventricular dysfunction predicted by early troponin I release after high-dose chemotherapy. J Am Coll Cardiol 2000; 36(2):517-22.
43. Mitchell MB, Parker CG, Meng X, Brew EC, Ao L, Brown JM, et al. Protein kinase C mediates preconditioning in isolated rat heart. Circulation 1993; 88(suppl I):I-633.
44. Lipshultz SE, Rifai N, Sallan SE. Predictive value of cardiac troponin T in pediatric patients at risk for myocardial injury. Circulation 1997; 96:2641-48.
45. Auner HW, Tinchon C, Linkesch W, Tiran A, Quehenberger F, Link H, et al. Prolonged monitoring of troponin T for the detection of anthracycline cardiotoxicity in adults with hematological malignancies. Ann Hematol 2003; 82:218-22.
46. Steen H, Giannitsis E, Futterer S, et al. Cardiac troponin T at 96 hours after acute myocardial infarction correlates with infarct size and cardiac function. J Am Coll Cardiol 2006; 48:2192-94.
47. Sparano JA, Brown DL, Wolff AC. Predicting cancer therapy-induced cardiotoxicity. The role of troponins and other markers. Drug Saf 2002; 25:301-11.
48. Garrone O, Crosetto N, Lo Nigro C, Catzeddu T, Vivenza D, Monteverde M, et al. Prediction of anthracycline cardiotoxicity after chemotherapy by biomarkers kinetic analysis. Cardiovasc Toxicol 2012; 12(2):135-42.
49. Braunwald E. Biomarkers in heart failure. N Engl J Med 2008; 358:2148-59.
50. Emdin M, Clerico A, Clemenza F, et al. Recommendations for the clinical use of cardiac natriuretic peptides. Ital Heart J 2005; 6:430-46.
51. Sherief LM, Kamal AG, Khalek EA, Kamal NM, Soliman AA, Esh AM. Biomarkers and early detection of late onset anthracycline-induced cardiotoxicity in children. Hematology 2012; 17(3):151-6.
52. Suzuki T, Hayashi D, Yamazaki T, et al. Elevated B-type natriuretic peptide levels after anthracycline administration. Am Heart J 1998; 136:362-3.
53. Erkus B, Demirtas S, Yarpuzlu AA, Can M, Genc Y, Karaca L. Early prediction of anthracycline induced cardiotoxicity. Acta Paediatr 2007; 96:506-9.
54. Nuver J, De Haas EC, Van Zweeden M, Gietema JA, Meijer C. Vascular damage in testicular cancer patients: a study on endothelial activation by bleomycin and cisplatin in vitro. Oncol Rep 2010; 23:247-53.
55. de Lemos JA, O’Donoghue M. The skinny on fatty acid-binding protein. J Am Coll Cardiol 2007; 50(21):2068-70.
56. Kilcullen N, Viswanathan K, Das R, Morrell C, Farrin A, Barth JH, et al. Heart type fatty acid-binding protein predicts long-term mortality after acute coronary syndrome and identifies high-risk patients across the range of troponin values. J Am Coll Cardiol 2007; 50(21):2061-7.
57. O’Donoghue M, de Lemos JA, Morrow DA, Murphy SA, Buros JL, Cannon CP, et al. Prognostic utility of heart-type fatty acid binding protein in patients with acute coronary syndromes. Circulation 2006; 114(6):550-7.
58. ElGhandour AH, ElSorady M, Azab S, ElRahman M. Human heart-type fatty acid-binding protein as an early diagnostic marker of doxorubicin cardiac toxicity. Hematol Rev 2009; 1:e6.
59. Ky B, Putt M, Sawaya H, French B, Januzzi JL Jr, Sebag IA, et al. Early increases in multiple biomarkers predict subsequent cardiotoxicity in patients with breast cancer treated with Doxorubicin, taxanes, and trastuzumab. J Am Coll Cardiol 2014; 63(8):809-16.
60. Visscher H, Ross CJ, Rassekh SR, Barhdadi A, Dube MP, Al-Saloos H, et al. Pharmacogenomic prediction of anthracycline- induced cardiotoxicity in children. J Clin Oncol 2012; 30:1422-8.
61. Schwartz RG, Jain D, Storozynsky E. Traditional and novel methods to assess and prevent chemotherapy-related cardiac dysfunction noninvasively. J Nucl Cardiol 2013; 20(3):443-64.
![]()