Artículos de Revisión
Malaria, enfermedad tropical de múltiples métodos diagnósticos
María Alejandra Aristizábal Giraldo 1, Lina María Martínez Sánchez 2, Dayana Andrea Quintero Moreno 3, Johan Harley Muñoz Ríos 4, Laura Esperanza Valencia Asprilla 5
1.Estudiante de pregrado Medicina, Universidad Pontificia Bolivariana, Calle 78 B N 72 a 109, Medellín, Colombia. Escuela de Ciencias de la Salud, Facultad de Medicina, teléfono: +57(4) 4488388. Email: mariaa.aristizabal@upb.edu.co
2. Bacterióloga, Esp, MSc, Docente titular, Universidad Pontificia Bolivariana, Calle 78 B N 72 a 109, Medellín, Colombia. Escuela de Ciencias de la Salud, Facultad de Medicina, teléfono: +57(4) 4488388. Email: linam.martinez@upb.edu.co
3. Estudiante de pregrado Medicina, Universidad Pontificia Bolivariana, Calle 78 B N 72 a 109, Medellín, Colombia. Escuela de Ciencias de la Salud, Facultad de Medicina, teléfono: +57(4) 4488388. Autor de correspondencia Email: dayana.quinteroq@upb.edu.co
4. Estudiante de pregrado Medicina, Universidad Pontificia Bolivariana, Calle 78 B N 72 a 109, Medellín, Colombia. Escuela de Ciencias de la Salud, Facultad de Medicina, teléfono: +57(4) 4488388. Email: johan.munozr@upb.edu.co
5. Estudiante de pregrado Medicina, Universidad Pontificia Bolivariana, Calle 78 B N 72 a 109, Medellín, Colombia. Escuela de Ciencias de la Salud, Facultad de Medicina, teléfono: +57(4) 4488388. Email: laura.valenciaa@upb.edu.co
Archivos de Medicina (Manizales), Volumen 17 N° 2, Julio-Diciembre 2017, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Aristizábal Giraldo M.A.; Martínez Sánchez L.M.; Quintero Moreno D.A.; Muñoz Ríos J.H.; Valencia Asprilla L.E.
Recibido para publicación: 31-07-2017 - Versión corregida: 02-11-2017 - Aprobado para publicación: 05-11-2017
Resumen
La malaria es una enfermedad causada por el parasito de género Plasmodium, que se transmite mediante la picadura de la hembra del mosquito Anopheles. Entre los años 2000 a 2015 se han reportado 212 millones de casos a nivel mundial. En Colombia, la malaria es considerada un problema de salud pública, se estima que al menos el 70% del territorio cuenta con las condiciones ecológicas necesarias para la transmisión del parasito. Para evitar el aumento en el número de casos de malaria, se utilizan 3 pilares de prevención: evitar la exposición y realizar control del vector, quimioprofilaxis y diagnóstico oportuno. Después de este último, se debe brindar el tratamiento, cuyos objetivos son: curación clínica del paciente, curación radical de la infección y control de la transmisión. Para el diagnóstico, existen diferentes métodos, los cuales se evalúan y diferencian de acuerdo a la sensibilidad y especificidad; con base en esto, se define el Gold Standard, como prueba de referencia. En la actualidad, el Gold Standard para el diagnóstico de malaria es un método microscópico: gota gruesa. Sin embargo, existen otros métodos: extendido de sangre periférica, métodos moleculares y métodos serológicos.
Palabras clave: malaria, anopheles, diagnóstico.
Aristizábal-Giraldo MA, Martínez-Sánchez LM, Quintero-Moreno DA, Muñoz-Ríos JH, Valencia-Asprilla LE. Malaria, enfermedad tropical de múltiples métodos diagnósticos. Arch Med (Manizales) 2017; 17(2):402-14.
Malaria, tropical disease of multiple diagnostic methods
Summary
Malaria is a disease caused by the parasite of the genus Plasmodium, which is transmitted by the bite of the female Anopheles mosquito. Between 2000 and 2015, 212 million cases have been reported worldwide. In Colombia, malaria is considered a public health problem, it is estimated that at least 70% of the territory has the necessary ecological conditions for the transmission of the parasite. To avoid the increase of the number of malaria cases, three pillars of prevention are used: avoiding exposure and performing vector control, chemoprophylaxis and timely diagnosis. After this, the treatment should be provided. The objectives of the treatment are: clinical cure of the patient, radical cure of infection and control of transmission. To diagnosis, there are different methods, which are evaluated and differentiated according to sensitivity and specificity; Based on this, the Gold Standard is defined as the Benchmark test. Nowadays, the Gold Standard for the diagnosis of malaria is a microscopic method call thick gout. However, there are other methods such as: peripheral blood smear, molecular methods and serological methods.
Keywords: malaria, anopheles, diagnostic.
Definición y etiología
La malaria es una enfermedad infecciosa, que se transmite mediante la picadura de la hembra del mosquito Anopheles infectada por el parásito. Son cinco las especies del parásito del género Plasmodium que tienen la capacidad de infectar a los humanos: P. falciparum, P. vivax, P. ovale, P.malariae y P. knowlesi [1]. Este último ha sido recientemente identificado; proviene de los primates, pero tienen la capacidad de infectar humanos, como se ha reportado en las zonas de Malasia y Borneo, ubicados en el continente asiático; los afectados tienen en común el antecedente de haber permanecido en un entorno selvático [2]. La especie P. falciparum, es la principal causante de los episodios mortales por malaria; además es la especie más común en el continente africano. En contraste, P. vivax es la especie más frecuente en los demás continentes y es responsable de 80 millones de episodios anuales de la enfermedad [1].
Las formas más graves de la malaria se deben a P. falciparum, esta clase de Plasmodium tiene la capacidad de ubicarse en la microvasculatura venosa profunda y producir manifestaciones clínicas severas entre las cuales se incluyen anemia profunda, insuficiencia respiratoria, insuficiencia renal, malaria cerebral y malaria severa del embarazo [3]. P. vivax y P. ovale, pueden originar formas latentes en el hígado, llamadas hipnozoitos, los cuales son los responsables de recurrencias de la enfermedad, después de abandonar la zona endémica [2]. Por su parte, P. malariae, puede causar episodios febriles muchos años más tarde y acompañarse de síndrome nefrótico [2].
Ciclo de vida
El período de incubación del parásito, depende de la especie de Plasmodium; siendo P. malariae el de mayor duración con un período que va entre 18 y 40 días, seguido de P. falciparum con un período que oscila entre 10 y 12 días, el de P. vivax y ovale es de 14 días en promedio y por último, P. knowlesi, que es de 11 días [2].
Se han estudiado dos tipos de reproducciones, la sexual, la cual se produce en las hembras de los mosquitos del género Anopheles; y la de tipo asexual se da en el hígado y los glóbulos rojos de los seres humanos infectodos [2].
En el intestino del mosquito hembra Anopheles infectado por el parásito Plasmodium, se da la reproducción sexual; en este órgano los cigotos se convierten en esporozoitos, una forma de protozoo, que posteriormente se ubican en las glándulas salivales [4]. Cuando el mosquito infectado pica a un ser humano, los esporozoitos pasan de la glándula salival del insecto al torrente circulatorio de la persona, donde se quedan aproximadamente 1 hora. Posteriormente, el protozoo en forma de esporozoito penetra las células parenquimatosas del hígado, donde se multiplica mediante reproducción asexual y produce otra forma de protozoo denominado merozoito. Con el paso del tiempo, los hepatocitos infectados se lisan, liberando un gran número de merozoitos móviles, que pasan al torrente sanguíneo; luego invaden los eritrocitos y cada 48 a 72 horas se multiplican entre 6 y 20 veces a través de reproducción asexual, causando lisis celular y liberación de un mayor número de merozoitos infecciosos. Dicho proceso, puede repetirse muchas veces; agravando cada vez más la sintomatología de la enfermedad. Finalmente, algunos merozoitos regresan al hígado y constituyen la base para nuevos episodios de malaria; mientras que otros se convierten en gametocitos ya sean masculinos o femeninos, retornando al torrente circulatorio [4].
Por último, un mosquito hembra de tipo Anopheles, succiona la sangre de una persona infectada y los gametocitos pasan al intestino del mosquito; en dichos órganos se convierten en gametos maduros, los cuales se fusionan para la formación del cigoto, dando lugar así a la reproducción sexual [4].
Transmisión
La transmisión de la malaria se da a través de la picadura del mosquito hembra del género Anopheles, infectado con cualquiera de las especies de Plasmodium [2]. La distribución geográfica de este vector incluye la franja tropical y subtropical [1]. En Colombia se han identificado aproximadamente 47 especies, de las cuales las más representativas son Anopheles albimanus, Anopheles darlingi y Anopheles nuneztavari. Este vector se encuentra en gran variedad de nichos como excavaciones, estanques de peces, lagunas, entre otros [5].
A nivel mundial se ha identificado que la ubicación, la edad, el nivel socio económico y el número de personas que habitan por vivienda; son determinantes del riesgo para la trasmisión de esta infección [6]. En Colombia, específicamente, se consideran como factores de riesgo: la minería ilegal, la actividad piscícola, la agricultura, el conflicto armado y el desplazamiento forzado; pues favorecen la presentación rural y peri-rural de la enfermedad [7, 8].
Epidemiología
La malaria es una de las enfermedades infecciosas transmitidas por vectores que tiene mayor prevalencia a nivel mundial aunque el número de casos ha disminuido a través del tiempo debido a que se encuentra en proceso de control y erradicación, de acuerdo a la OMS la incidencia ha disminuido en un 41% entre los años 2000 a 2015 y un 21% en el período 2010 y 2015; durante el último año se presentaron a nivel mundial 212 millones de casos [9,10].
África, es el continente en el cual se registra el mayor número de casos y muertes, el cual representa el 90%; sin embargo, la cifra de personas infectadas ha descendido de 131 millones en el 2010 a 114 millones para el 2015, siendo más alta en niños entre 2 y 10 años. [9, 10]. El segundo lugar es ocupado por la región de Asia sudoriental, que representa el 7% de los casos [10]. El continente americano, por su parte, aporta una baja carga a las estadísticas, sin embargo, los países que lideran las tasas de infección en este continente son: Brasil y Colombia que aportan el 70% de los casos, con un 52% y 13% respectivamente [6,11].
En Colombia, la malaria es considerada un problema de salud pública, se estima que al menos el 70% del territorio cuenta con las condiciones ecológicas necesarias para la transmisión de la enfermedad; y son cinco regiones las que reportan el mayor índice: Costa pacífica, Orinoquia, Amazonia, Urabá y Bajo Cauca [7,11]. Durante el año 2016, según el Boletín Epidemiológico Semanal (BES) número 52 del SIVIGILA, en Colombia se presentaron 83 356 casos de malaria, cuya etiología se atribuyó el 57% a P. falciparum, 39,7% a P. vivax y 3,3 % a malaria mixta. Del total de casos reportados, 81 862 fueron malaria no complicada, el 78,1% de éstos, se concentraron en tres departamentos: Chocó, Nariño y Antioquia. Por otra parte, se reportaron 1 494 casos de malaria complicada, liderados por los departamentos de: Chocó, Antioquia y Nariño, los cuales representaron el 63,95% de los casos [12].
En lo transcurrido del año 2017, de acuerdo al BES número 41 se han presentado 43 757 casos de malaria, la etiología de la infección se atribuye en 57,7% a P. falciparum, 40,3% a P. vivax y 2% corresponden a infección mixta, los departamentos con mayor número de casos reportados, en orden decreciente son Chocó, Nariño y Antioquia. Con respecto al tipo de malaria, 42 880 casos corresponden a malaria no complicada y 877 corresponden a malaria complicada [13].
Con base en los datos publicados por la dirección de vigilancia y análisis de riesgo en salud pública del Instituto Nacional de Salud en Colombia, la población más afectada para el período 2016-2017 fueron hombres, afrocolombianos entre los 20 y 24 años [12].
Los indicadores mundiales demuestran que entre 2000 y 2015, la tasa de mortalidad por esta enfermedad disminuyó un 62% y un 29% entre 2010 y 2015 [10]. Sin embargo, el panorama cambió durante el año 2016, debido a que se intensificó significativamente la transmisión de malaria en los municipios endémicos de algunos países del continente Americano. Además del incremento de los casos por P. falciparum en algunos focos endémicos [14].
Manifestaciones clínicas
La malaria exhibe un amplio espectro de cuadros clínicos, incluyendo la infección asintomática, la infección sintomática sin complicaciones y la malaria complicada. Este espectro depende de múltiples factores tales como el huésped, los determinantes ambientales y la especie parasitaria. Un ejemplo ilustrativo de este hecho, es que las personas que han habitado en zonas altamente endémicas
desarrollan protección parcial para los síntomas severos a una edad temprana porque han estado continuamente expuestos al protozoo [15].
La presentación clínica inicial de la enfermedad es inespecífica y puede ser difícil el reconocimiento de la misma, ya que los primeros síntomas pueden resultar parecidos a los típicos del inicio de una enfermedad viral. Entre estos podemos encontrar: cefalea, sensación de malestar general, dolor abdominal, mialgias, escalofríos y picos febriles; los cuales aparecen en promedio de 10 a 15 días post picadura de un mosquito infectado [16].
Adicionalmente, puede presentarse otra brecha de síntomas como dolor torácico, dolor abdominal, artralgias, hipotensión ortostática, cefalea intensa, diarrea, náuseas, vómito y tos que pueden hacer pensar en otros diagnósticos diferenciales tales como dengue, leptospirosis, meningitis, entre otros [17].
En la malaria aguda se presentan escasas alteraciones físicas, tales como: bazo palpable, anemia, hepatomegalia e ictericia leve y fiebre; esta último, es su signo predominante en la mayoría de los casos. La cual suele ser irregular en las fases iniciales, llamada fiebre de aclimatación, se presenta debido al comienzo de la enfermedad y liberación de merozoítos que no se ha sincronizado; con valores mayores de 40 ºC y generalmente se acompañan de taquicardia [18]. Con el tiempo, la hemólisis se organiza de manera sincrónica y se presentan episodios febriles con una periodicidad característica: de un día por medio en las infecciones causadas por P. vivax, P. ovale y P. falciparum, y cada dos días cuando es causado por P. malariae [18].
Por otro lado, con un tratamiento a tiempo, la tasa de mortalidad por P. falciparum es aproximadamente 0,1% [19].
La malaria grave por P. falciparum presenta un gran número de cuadros clínicos que se muestran a continuación.
Malaria cerebral es una de las complicaciones clínicas más severas de la infección por P. falciparum, con una tasa de mortalidad cercana al 20%. La fisiopatología es la cito-adherencia al endotelio cerebral de los glóbulos rojos, plaquetas y leucocitos infectados, que conducen a la obstrucción de los microvasos y la inflamación excesiva del cerebro [20, 21]. Se puede presentar de forma súbita o gradual después de una crisis convulsiva desencadenante. Las manifestaciones son simétricas y difusas e incluyen alteración del estado de conciencia, conductas anómalas, mirada divergente, reflejo de labios fruncidos con ausencia de los demás reflejos primitivos, hipotonía o hipertonía y resistencia a la flexión de la cabeza. Es importante mencionar que aproximadamente una quinta parte de estos pacientes tienen hemorragias retinianas visibles [17]. La mortalidad aún con tratamiento, alcanza cifras del 20% en adultos y 15% en niños. De las personas sobrevivientes, 10-15% quedan con secuelas neurológicas permanentes [18]. Mientras que otras pueden ser reversibles, como el deterioro cognitivo que afecta durante varios años después del episodio y se presenta en el 14-25% de los niños [22].
Otra manifestación importante de malaria grave es la hipoglicemia que se da por el incremento del consumo de glucosa por el hospedador y el parásito, llevando a una insuficiencia hepática. Esto suele acompañarse de una acidemia metabólica grave, que es causa prevalente de muerte por esta patología [23]. Otro de los factores implicados en el proceso de la hipoglicemia, es la hiperinsulinemia, dependiente del factor de necrosis tumoral alfa (TNF-α). Este último está implicado también en la hematopoyesis, actuando como inhibidor de este proceso, lo cual contribuye a la anemia [18].
La insuficiencia renal, es otro de los signos de malaria grave por P. falciparum, que se explica por la conglomeración de eritrocitos parasitados que hacen interferencia en la circulación renal. Esta insuficiencia se expresa en forma de necrosis tubular aguda [17].
Por otro lado, la disfunción hepática es otra de las manifestaciones clínicas relevantes en la malaria grave, la cual se manifiesta habitualmente con ictericia hemolítica leve.
En estudios previos se encontró que en la región del Pacífico Colombiano la complicación más frecuente por P. falciparum fue la disfunción hepática en un 33%, seguida de la insuficiencia renal 31%, hiperparasitemia 22%, malaria cerebral 17% y anemia grave 13% [24].
Otras de las complicaciones son: edema pulmonar, síndrome de distrés respiratorio del adulto (SDRA), gastroenteritis, anemia y hemorragias [18].
El edema pulmonar se produce en respuesta al secuestro de glóbulos rojos parasitados en la microcirculación pulmonar, generando daño endotelial y favorece la extravasación de líquidos hacia el intersticio y la luz alveolar. Este proceso se potencia por la liberación de citoquinas inflamatorias, lo que puede conducir al edema pulmonar y/o SDRA. Cuando se presenta el edema pulmonar y SDRA la mortalidad es del 15%; con frecuencia se evidencia en mujeres embarazadas [18]. En comparación con la etiología de los casos de malaria que desarrollan síndrome de distrés respiratorio, se encontró que era más prevalente en los casos de P.vivax [25].
Las alteraciones hematológicas son una manifestación común de la malaria complicada y son las más frecuentes en los niños. Se puede evidenciar con un hematocrito menor del 15% o una hemoglobina menor de 5 gr/dl, en presencia de parasitemias hasta del 50%. Por su parte las alteraciones de la coagulación y la trombocitopenia, son de poca intensidad [26]. La razón fisiopatológica de estos procesos, se debe a que la presencia del plasmodio en el interior del glóbulo rojo, causa rigidez a nivel de su membrana celular, haciéndola más propensa a romperse, lo que conduce a mayor captación esplénica de glóbulos rojos parasitados y ocasiona anemia. A nivel del bazo, se presenta una mayor actividad y mayor secuestro de plaquetas, lo que explica la esplenomegalia y la trombocitopenia, respectivamente [18].
Por su parte, la malaria causad por P. knowlesi es muy frecuente la aparición de hipotensión, trastorno renal y por último trombocitopenia, la cual es constante en los hallazgos clínicos y no guarda relación con el nivel de parasitemia [18].
Métodos diagnósticos
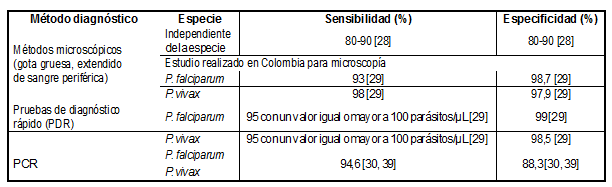
El diagnóstico de la malaria se basa en la historia clínica, los signos y síntomas. Debido a que estos últimos son inespecíficos, es necesario el uso de métodos diagnósticos. Existen diferentes pruebas entre las que se encuentran: métodos microscópicos como la gota gruesa y extendido de sangre periférica; métodos moleculares como: reacción en cadena de la polimerasa (PCR); prueba rápida de diagnóstico de malaria (PDR) y pruebas serológicas. Las diferencias son dadas por la sensibilidad y especificidad que presenta cada método diagnóstico, ver tabla 1 [27]. El gold standard es la gota gruesa, el cual permite la cuantificación y diferenciación de las especies de Plasmodium [27].
Tabla 1. Comparación de la sensibilidad y especificidad de los diferentes métodos diagnósticos de malaria.
Métodos microscópicos
Es el método tradicional y es considerado estándar de oro para el diagnóstico de malaria, el cual se confirma con la identificación de la especie de Plasmodium presente en la sangre. Para tener un resultado fiable se requiere de un personal entrenado y con amplia formación y experiencia. La sensibilidad y especificidad de esta prueba oscilan entre 80-90%, independiente de la especie de Plasmodium [28]. Un estudio realizado en Colombia indica que a través de este método de microscopía, la sensibilidad es 93% y especificidad es 98,7% para P. falciparum, mientras que para P. vivax, la sensibilidad es 98% y la especificidad es 97, 9% [29]. Dentro de las dificultades que presenta este método es que solamente detecta parasitemias mayores a 50 parásitos/μL, y no permite detectar coinfecciones; esta incapacidad de detectar infecciones con baja carga de parásitos sanguíneos, conduce al no tratamiento de los pacientes y por ende al progreso de la enfermedad [30, 31].
Dentro del análisis a través de la microscopía se encuentran incluidas dos técnicas que son: la gota gruesa y el extendido de sangre periférica, cuyos resultados a pesar de ser muy específicos, dependen de múltiples variables como la calidad en la preparación de la muestra, la habilidad a la hora de hacer la lectura y el nivel de parasitemia.
Gota gruesa
Colombia es uno de los países con mayor prevalencia de malaria en Latinoamérica, la prueba de la gota gruesa es la más solicitada en los casos de sospecha de la enfermedad, en los cuales una cuarta parte de las personas dan un resultado positivo a la prueba [32].
La técnica consiste en la realización de una punción con una lanceta estéril en el segundo o tercer dedo de la mano, previo a una limpieza con alcohol, para obtener de 3 a 4 gotas de sangre. Éstas luego de ser depositadas en un portaobjetos se extienden con movimientos rápidos en una capa gruesa y uniforme, luego se debe dejar secar y colorear con Giemsa [33]. Esta técnica permite observar mayor cantidad de sangre deshemoglobinizada y por ende mayor cantidad parásitos. Lo que se evidencia son los núcleos de los parásitos en forma de anillo o como una mancha [32].
Se debe realizar recuento de parásitos, solamente a los pacientes infectados con Plasmodium falciparum o a ciertas personas que provengan de zona endémica para este tipo de especie; existen un método para estimar la parasitemia denominado recuento real de glóbulos blancos, en el cual, se debe contar el número de parásitos y de leucocitos en campos diferentes hasta completar 200 leucocitos:
Cálculo de la parasitemia por microlitro de sangre:
|
Parásitos/μL= |
|
* En caso de no contar con el recuento de leucocitos del paciente, se puede asumir una concentración promedio de 8.000 leucocitos/mL |
Dentro de las debilidades de la gota gruesa se encuentra la dificultad para la identificación de las diferentes especies al presentarse ruptura de los eritrocitos y una sensibilidad limitada cuando el grado de parasitemia es bajo (<1000 parásitos asexuados/ microlitro) [34].
Extendido de sangre periférica
La técnica consiste en la realización de una punción con una lanceta estéril, para obtener una gota de sangre. Esta es depositada en un portaobjetos para realizar posteriormente una extensión en capa fina [33]. Este método facilita ver ciertas características morfológicas del parásito en los glóbulos rojos e identificar con mayor claridad la especie del parásito, cuando no se ha logrado con el método de gota gruesa [35].
Existen muchas tinciones que nos permiten hacer el diagnóstico de malaria, siendo importante mencionar la tradicional de Giemsa, la tinción de Field, el método de Leishman y la tinción fluorescente con naranja de acridina [33].
A la observación microscópica, tras la realización de la tinción, pueden ser identificados 3 estadios diferentes del parásito: gametocitos, trofozoitos y esquizontes, donde por lo general, el núcleo del parásito tiene una morfología redonda y es de un color rojo intenso, que se describe como rojo grosella, y el citoplasma de color azul toma diferente formas, desde una de anillo a una completamente irregular [32, 35].
Posteriormente, se hace un cálculo de la densidad parasitaria para evaluar la severidad de la infección y mantener un control del tratamiento que se le va a suministrar [2]. Los métodos más utilizados para realizar dicho proceso son: sistema de cruces (semicuantitativo) y cálculo del número de parásitos por microlitro de sangre [35].
Sistema de cruces: Cualquier número menor a 40 parásitos en 100 campos debe escribirse el número de parásitos encontrados y si hay más de 40 parásitos, entonces se reporta así:
+/2: De 40 a 60 parásitos en 100 campos
+ : Un parásito por campo en 100 campos
++: 2 a 20 parásito por campo en 100 campos
+++: 21 a 200 parásitos por campo en 100 campos
++++: Más de 200 parásitos por campo en 100 campos
Cálculo del número de parásitos por microlitro de sangre: es un método más práctico, preciso y que permite comparar. Para este cálculo se deben tener en cuenta tanto el número de parásitos como de leucocitos [35].
Las Pruebas de Diagnóstico Rápido (PDR)
Conocida también como “tira reactiva”, es un método rápido y sencillo, por el cual se detectan antígenos específicos presentes en la sangre de la persona afectada, que son producidos por el parásito. Presenta una sensibilidad similar a la gota gruesa, de un 95% con 100 parásitos/μL en el caso de P. falciparum. Un estudio realizado en Colombia, identificó que la especificidad de PDR en el diagnóstico de malaria por P. falciparum es 99% y por P. vivax es 98,5% [29].
Se trata de una prueba inmunocromatográfica de flujo lateral, que se realiza mediante una tirilla, la cual está recubierta con dos anticuerpos monoclonales: uno para la proteína rica en histidina 2 (HRP2) de la especie de P. falciparum y el otro anticuerpo es específico para la enzima deshidrogenasa láctica parasitaria (pLDH) de la especie de P. vivax. La interpretación se basa en la presencia de una o dos líneas y su relación con la línea de control [29].
Es una prueba muy recomendada para lugares de difícil acceso, donde no se cuenta con instrumentos de laboratorio para el uso de pruebas de mayor sensibilidad [36]. Las dificultades que presenta son: inestabilidad en medios húmedos, no identificación de infecciones mixtas ni grados de parasitemia por debajo de 100 parásitos/μL [37].
Se debe tener en cuenta que a pesar de su contribución significativa en el diagnóstico de malaria debido a la facilidad con la que pueden llevarse a cabo, PDR tienen varias limitaciones, tales como la falsa positividad debido a una infección previa, la reactividad cruzada con anticuerpos heterófilos y factor reumatoide [38].
Por otra parte, la diversidad genética y la supresión de la proteína rica en histidina 2 (HRP2) pueden afectar la sensibilidad, generando diagnóstico falso negativo, especialmente en los casos de Plasmodium falciparum que no presentan HRP2 y HRP3 (dichos cambios se han descrito especialmente en casos de países como Perú y Papúa Nueva Guinea).
Dentro de las pruebas de diagnóstico rápido, encontramos unas que se basan en la detección de antígenos específicos del parásito, tales como las enzimas Lactato Deshidrogenasa (pLDH) y aldolasa. Las desventajas que esto presenta son el alto costo y la escasa capacidad de diagnosticar infecciones mixtas [34].
Los métodos moleculares
Reacción en cadena de la polimerasa (PCR)
Es una técnica in vitro basada en la amplificación directa de un gen o una porción de ácido desoxirribonucleico (ADN) o indirecta de ácido ribonucleico (ARN) presente en mezclas de diversas fuentes [30].
Este método presenta una alta sensibilidad, equivalente a 94,6%; superando otras pruebas, debido a que puede detectar más de 0,002 parásitos/μL de sangre y la presencia de co-infección, es decir, más de una especie de Plasmodium; sin embargo su especificidad es del 88,3% [30, 39]. Una de las ventajas en comparación con los otros métodos diagnósticos, es que se demostró que se puede detectar la enfermedad en el estado pre-eritrocito al detectar el ADN del parásito mediante una PCR en la materia fecal de los pacientes y en sangre periférica, debido a las grandes inoculaciones del mosquito [40].
Se ha utilizado principalmente PCR anidada, que detecta la subunidad 18S del ácido ribonucleico ribosómico (ARNr) del Plasmodium, este tipo de PCR ha servido de estándar para la comparación con otros tipos de PCR como PCR en tiempo real (qpcr), puesto que este ha tenido baja eficiencia a la hora de realizar la electroforesis [39].
La reacción en cadena de la polimerasa en tiempo real (qPCR) ha tenido un aumento importante en su implementación, pues tiene alta sensibilidad y especificidad, es de fácil manejo, es la más rápida, tiene el menor riesgo de contaminación, confirma resultados ambiguos arrojados por microscopía y tiene la capacidad para identificar infecciones mixtas [28].
Sin embargo, tiene desventajas tales como el alto coso, falta de control de calidad, falta de estandarización, falsos positivos por contaminación, la interpretación clínica puede ser ardua, el requerimiento de elementos sofisticados y personas altamente entrenadas en la técnica [28].
Métodos preventivos
La malaria, es una enfermedad prevenible y tratable. Entre los años 2001 a 2013 se logró disminuir en un 47% la tasa de mortalidad por esta infección, alcanzar este objetivo se atribuye a la ampliación e implementación de estrategias para la prevención de esta enfermedad [16].
La estrategia de prevención está basada en tres pilares: evitar la exposición y realizar control del vector, quimioprofilaxis y diagnóstico oportuno. En cuanto a lo relacionado con el vector se recomienda el uso de insecticidas, vestimenta que cubra gran parte del cuerpo y mosquiteros. La quimioprofilaxis, se recomienda a viajeros que se expondrán a lugares con una alta-media carga de la infección, sin embargo, se ha encontrado que su uso puede llevar a eventos adversos entre un 35 a 42% [16, 41, 42]. El principal fármaco utilizado en la profilaxis es la Cloroquina, no obstante, si el territorio a visitar reporta resistencia a este antimalárico, se deberá recurrir a otros medicamentos como son la atovaquona/proguanil, doxiciclina y mefloquina. En la fase final del tratamiento profiláctico se utiliza Primaquina pues actúa sobre las formas hepáticas del parásito, lo que permitirá asegurar la protección a futuro [43].
Tratamiento
El tratamiento farmacológico antimalárico debe dar inicio inmediatamente se obtenga la confirmación parasitológica por examen microscópico, y tiene 3 objetivos principales: la curación clínica del paciente, la curación radical de la infección malárica y el control de la transmisión de la enfermedad [3, 44].
Los criterios básicos para definir el esquema terapéutico son: definir si la malaria es complica o no, identificación de la especie causante de la infección, evaluación de la densidad parasitaria, la edad, el estado o no de embarazo, la tolerancia del paciente al tratamiento vía oral e información sobre malaria previa y su correspondiente tratamiento [44].
El esquema de tratamiento de primera línea en Colombia, para malaria no complicada producida por P. falciparum consta de Arthemether 20 mg + Lumefantrina 120 mg vía oral. Deben darse 6 dosis distribuidas 2 veces por día, durante 3 días. Pero es de resaltar que si el caso anterior se presenta en una mujer embarazada el tratamiento varía, debido a las reacciones adversas documentadas de este esquema. Durante el primer semestre se debe dar Quinina más Clindamicina y durante el segundo semestre Arthemether con Lumefantrina [3].
Por su parte, el esquema de tratamiento de primera línea en Colombia para malaria no complicada producida por P. vivax es Cloroquina vía oral distribuida de la siguiente manera: 600 mg el primer día, 450 mg a las 24 horas y 50 mg a las 48 horas, o Primaquina vía oral 15 mg/ día durante 14 días [45].
Finalmente, si la malaria es complicada, el esquema básico Colombiano consta de Artesunato 2,4 mg/ kg intravenoso al ingreso, a las 12 y 24 horas. Luego se debe continuar con esta misma dosis 1 vez al día hasta que el paciente tolere la vía oral o hasta completar 7 días de tratamiento [4].
Perspectivas futuras
La Estrategia Técnica Mundial (GTS) contra la malaria 2016-2030, plantea como metas para el año 2030: reducción a nivel mundial de la incidencia de casos de malaria y la mortalidad asociada en al menos un 90% en comparación con los datos del 2015; eliminar la enfermedad en al menos 35 países en los que había transmisión en el 2015 y prevenir el restablecimiento de la enfermedad en todos los países que previamente se haya eliminado. Para su cumplimiento, se prioriza en tres pilares que son: garantía al acceso universal a la prevención, diagnóstico y tratamiento; acelerar los esfuerzos hacia la eliminación y logro del estado libre de malaria, transformar la vigilancia de la malaria en una intervención central. Cuenta a su vez, con un Plan de Acción e Inversión para vencer la malaria (AIM) [10, 16].
Con respecto a los Objetivos de Desarrollo Sostenible (ODS), entre sus metas se encuentra, ponerle fin a múltiples epidemias para el año 2030, entre ellas la de la malaria [10].
Para el seguimiento del progreso de estas metas, se tienen 41 indicadores para utilizar tanto a nivel mundial, nacional como subnacional [10].
Entre las estrategias de prevención se encuentra la vacunación contra malaria, sin embargo, no se han obtenido resultados contundentes con ninguna vacuna, por lo cual no hay aprobación de su uso. A pesar de esto, se continúa trabajando en la creación de una vacuna que prevenga la infección [46].
Las perspectivas futuras en cuanto a métodos diagnósticos de malaria, son muy alentadoras, ya que con los métodos moleculares se ha facilitado su progreso a gran velocidad. Entre estos avances, se encuentra la amplificación isotérmica mediada por bucle (LAMP, loop mediated isothermal amplification), su fundamento se basa en la amplificación de un fragmento específico de ADN en un bloque de calor sin la necesidad de un termociclador; a diferencia de la PCR, en la cual éste último es necesario. Cuatro cebadores especialmente diseñados y dos cebadores adicionales que forman bucles, amplificando el ADN diana a través de Bst polimerasa. Una amplificación significativa conduce a la acumulación de pirofosfato de magnesio, que convierte la solución de coloración turbia, lo cual indica positividad de la prueba; dicha turbidez es visible a simple vista o puede medirse con un medidor de turbidez. La sensibilidad y especificidad de esta prueba es 98,1% y 100%, respectivamente, ver Tabla 2 [28]. Por sus múltiples ventajas se proyecta a futuro como un método que puede ser utilizado a nivel mundial, como una alternativa menos costosa y con gran eficacia.
Tabla 2. Propiedades del método LAMP [48]

Tomada de: Sánchez E, Nina M, Aguirre P, Arce M, Toro N, Vilela R. Amplificación isotérmica mediada por LOOP (LAMP) de ácidos nucleicos en el diagnóstico clínico. Revista conciencia 2014; 1 (2) 129.
A través de los años se han implementado diferentes medicamentos con el fin de mejorar eficacia y seguridad del tratamiento de malaria. Actualmente se adelantan proyectos para combatir la resistencia que se presenta a los medicamentos convencionales, principalmente en el continente Africano. Uno de estos medicamentos es carmoficina B, que actúa inhibiendo tanto la etapa sexual como asexual de la infección, siendo la subunidad β5 del proteosoma su blanco molecular [47].
Conclusión
Existen múltiples métodos diagnósticos de malaria, una enfermedad infecciosa muy frecuente a nivel mundial; éstos varían en cuanto a sensibilidad y especificidad; siendo el más sensible la PCR ya que permite la detección de la infección desde 0,002 parásitos/µL de sangre y la presencia de co-infección. A pesar de esto, la gota gruesa continúa siendo el método de referencia por su alta especificidad y su bajo costo. El avance de la ciencia ha permitido la implementación y el desarrollo de nuevos métodos diagnósticos que presenten mayor eficacia, que sean de fácil acceso y uso para los países con alta prevalencia de la enfermedad, que en su mayoría son países en vía de desarrollo.
Conflictos de interés: los autores declaran no tener conflictos de interés.
Fuentes de financiación: este artículo no requirió financiación.
Literatura citada
- Fumandó V, Bassat Q. Estado actual de la malaria (I): diagnóstico y tratamiento. AnPediatricContin2011; 9(3):162-169.
- García M, Fumandó V, González MI; Grupo de Tra- bajo de Enfermedades Tropicales de la Sociedad de Infectología Pediátrica (SEIP). Actualización en el diagnóstico y tratamiento de la malaria. An Pediatr (Barc) 2013; 78(2):124.e1–124.e8.
- Colombia. Ministerio de Salud y Protección Social, Federación Médica Colombiana. Malaria: memo- rias. Bogotá: Federación Médica Colombiana; 2013.
- Ingraham JL, IngrahaM CA, Prentiss H. Introduc- ción a la microbiología. Barcelona: Reverté; 1998.
- Fuller DO, Alimi T, Herrera S, Beier JC, Quiñones ML. Spatial association between malaria vector species richness and malaria in Colombia. Acta Trop 2016; 158:197-200.
- Forero DA, Chaparro PE, Vallejo AF, Benavides Y, Gutiérrez JB, Arévalo-Herrera M, et al. Knowledge, attitudes and practices of malaria in Colombia. Malar J 2014; 13:165.
- Osorio L, Todd J, Bradley DJ. Travel histories as risk factors in the analysis of urban ma- laria in Colombia. AmJ Trop Med Hyg 2004; 71(4):380-6.
- Padilla JC, Chaparro PE, Molina K, Arevalo-Herrera M, Herrera S. Is there malaria transmission in urban settings in Colombia? MalarJ 2015; 14:453
- World Health Organization. World malaria report 2015. Geneva: WHO; 2015.
- World Health Organization. World malaria report 2016. Geneva: WHO; 2016; 2-56.
- Padilla JC, Álvarez G, Montoya R, Chaparro P, Herrera S. Epidemiology and control of malaria in Colombia. Mem Inst Oswaldo Cruz 2011; 106 (Suppl 1):114–122.
- Instituto Nacional de Salud de la República de Colombia. Boletín Epidemiológico. Bogotá DC: Instituto Nacional de Salud. Colombia; 2016.
- Instituto Nacional de Salud. Boletín Epidemio- lógico. Bogotá DC: Instituto Nacional de Salud.Colombia; 2017.
- Organización Mundial de la Salud, Organización Panamericana de la Salud. Washington DC: Alerta Epidemiológica: Aumento de casos de malaria; 2017; 1-6.
- Bousema T, Okell L, Felger I, Drakeley C. As- ymptomatic malaria infections: detectability, transmissibility and public health relevance. Nat Rev Microbiol. 2014; 12:833–40.
- Organización Mundial de la Salud. Estrategia técnica mundial contra la malaria 2016-2030. Ginebra: Organización Mundial de la Salud: OMS; 2016.
- Longo DL, Kasper DL, Jameson JL, Fauci AS, Hausen SL, Loscalzo J. Harrison, principios de medicina interna. 18°ed. México: Mc Graw Hill; 2012. P. 1692-93.
- Montero A. Paludismo. Medicina tropical. Abor- daje práctico e integral. Madrid: Elsevier; 2014. p. 97-114.
- World Health Organization. Guidelines for the treatment of malaria.3 ed. Genova: World Health Organization; 2015.
- Ohashi J, Naka I, Hananantachai H, Patarapotikul J. Association of PECAM1/CD31 polymorphisms with cerebral malaria. Int J Mol Epidemiol Genet 2016; 7(2):87-94.
- Reverchon F, Mortaud S, Sivoyon M, Maillet I, Laugeray A, Palomo J, Montécot C, et al. IL-33 receptor ST2 regulates the cognitive impairments associated with experimental cerebral malaria. PLOS Pathog2017; 13(4): e1006322.
- Holmberg D, Franzén-Röh E, Idro R, Opoka RO, Bangirana P, Sellgren CM, et al. Cerebrospinal fluid kynurenine and kynurenic acid concen- trations are associated with coma duration and long-term neurocognitive impairment in Ugandan children with cerebral malaria. Malar J 2016; 16(1):303.
- Herdman MT, Sriboonvorakul N, Leopold SJ, Douthwaite S, Mohanty S, Hassan MM, et al. The role of previously unmeasured organic acids in the pathogenesis of severe malaria. Crit Care 2015; 19:317.
- Muñoz J, Rojo Marcos G, Ramírez Olivencia G, Salas Coronas J, Treviño B, Perez Arellano JL, et al. Diagnóstico y tratamiento de la malaria impor- tada en España: recomendaciones del Grupo de Trabajo de Malaria de la Sociedad Española de Medicina Tropical y Salud Internacional (SEMT- SI). Enferm Infecc Microbiol Clin 2015; 33(6):e1-e13.
- Val F, Machado K, Barbosa L, Salinas JL, Machado A, Costa MG, Bassat Q, et. al. Complicaciones respiratorias de la malaria por Plasmodium vivax: revisión sistemática y metaanálisis. So- ciedad Americana de Medicina Tropical e Higiene 2017; 733-743.
- Arboleda M, Perez MF, Fernandez D, Usuga LY, Meza M. Clinical and laboratory profile of Plas- modium vivax malaria patients hospitalized in Apartado, Colombia. Biomédica 2012; 32(Suppl 1):58–67
- Wilson ML. Laboratory diagnosis of malaria: conventional and rapid diagnostic methods. ArchPathol Lab Med 2013; 137(6):805-11.
- Mohon AN, Elahi R, Khan WA, Haque R, Sullivan DJ Jr, Alam MS. A new visually improved and sensitive loop mediated isothermal amplification (LAMP) for diagnosis of symptomatic falciparum malaria. Acta Trop 2014; 134:52-7.
- Herrera S, Vallejo AF, Quintero JP, Arévalo-Herrera M, Cancino M, Ferro S. Field evaluation of an automated RDT reader and data management device for Plasmodium falciparum/Plasmodium vivax malaria in endemic areas of Colombia. Malar J 2014; 13:87.
- Doctor SM, Liu Y, Whitesell A, Thwai KL, Taylor SM, Janko M, et al. Malaria surveillance in the Democratic Republic of the Congo: comparison of microscopy, PCR, and rapid diagnostic test. Diagn Microbiol Infect Dis 2016; 85(1):16-8
- Mohon AN, Lee LD-Y, Bayih AG, Folefoc A, Guelig D, Burton RA, et al. NINA-LAMP compared to mi- croscopy, RDT, and nested PCR for the detection of imported malaria. Diagn Microbiol Infect Dis 2016; 85(2):149-53.
- Campuzano Zuluaga G, Blair Trujillo S. Malaria: consideraciones sobre su diagnóstico. Medicina & Laboratorio 2010; 16(7-8):311-354.
- Turrientes MC, López-Vélez R. Aspectos prácticos del diagnóstico de laboratorio y profilaxis de la malaria. Madrid: Unidad de Medicina Tropical y Parasitología Clínica. Hospital Ramón y Cajal; 2000.
- Arroyo-A MI, Maestre-B A, Carmona-Fonseca J, So- sa-V PA, Morales-L GP. Amplificación isotérmica de ácidos nucleicos tipo LAMP para la detección de Plasmodium. Nueva técnica diagnóstica. Med UIS
- Perú. Ministerio de Salud. Manual de procedi- mientos para el diagnóstico de malaria. Lima: Ministerio de Salud; 2003
- Colombia. Ministerio de la Protección Social, Institu- to Nacional de Salud. Guía para atención clínica integral del paciente con malaria. Bogotá DC: Instituto Nacional de Salud; 2010.
- Colombia. Ministerio de la Protección Social, Ins- tituto Nacional de Salud, OPS. Protocolo para la vigilancia en Salud Publica de Malaria. Bogotá: INS, Subdirección de Vigilancia y control en Sale Pública; 2006.
- Koita OA, Doumbo OK, Ouattara A, Tall LK, Konaré A, Diakité M, et al. False-negative rapid diagnos- tic tests for malaria and deletion of the histi- dine-rich repeat region of the hrp2 gene. Am J Trop Med Hyg 2012; 86(2):194-8.
- Isozumi R, Fukui M, Kaneko A, Chan CW, Kawa- moto F, Kimura M. Improved detection malaria cases in island settings of Vanuatu and Kenya by PCR that targets the Plasmodium mitochondrial cytochrome c oxidase III (cox3) gene. Parasitol Int 2015; 64(3):304-8.
- Abkallo HM, Liu W, Hokama S, Ferreira PE, Naka- zawa S, Maeno Y, et al. DNA from pre-erythrocytic stage malaria parasites is detectable by PCR in the faeces and blood of hosts. Int J Parasitol 2014; 44(7):467-73
- White NJ, Breman JG. Malaria. En: Longo DL, Kasper DL, Jameson JL, Fauci AS, Hausen SL, Loscalzo J. Harrison, Principios de medicina interna. 18°ed. México DF: Mc Graw Hill; 2012. p.1703-1705
- Vournad R, Berthod D, Rambaud-Althaus C, D´Acremont V, Genton B. Recommendation for malaria prevention in moderate low risk áreas: travellers choice and risk perception. Malaria J 2015; 14:139.
- Capdevila JA, Icart R. Profilaxis de la malaria en el viajero. Rev Clin Esp. 2010; 210(2):77–832
- Padilla JC, Montoya R. Guía de atención clínica de malaria. Bogotá: Asociación Colombiana de Infectologia; 2011.
- Organización Panamericana de la Salud, OMS. Convenio de Cooperación Técnica con el Minis- terio de la Protección Social Nro. 256 de 2009 y Nro. 237 de 2010 guía para la atención integral del paciente con malaria. Bogotá: Ministerio de Salud y Protección Social de la República de Co- lombia; 2010.
- Thera MA, Doumbo OK, Coulibaly D, Laurens MB,Ouattara A, Kone AK, Guindo AB, et al. A Field Trial to Assess a Blood-Stage Malaria Vaccine. N Engl J Med 2010; 365(11):1000-1013.
- LaMonte GM, Almaliti J, Bibo-Verdugo B, Keller L, Zou BY, Yang J, et al. Development of a Potent Inhibitor of the Plasmodium Proteasome with Reduced Mammalian Toxicity. J Med Chem 2017; 60(15): 6721 - 6732.
- Sánchez E, Nina M, Aguirre P, Arce M, Toro N, Vilela R. Amplificación isotérmica mediada por LOOP (LAMP) de ácidos nucleicos en el diagnóstico clínico. Conciencia2014; 1(2):129. 2008; 21(3):158-175.
![]()