Cafeína y comportamiento animal. Análisis sobre condiciones experimentales
John Faber Morales 1; Francia Restrepo de Mejía 2; Luz Dary Rodríguez Sotelo 3; Jhonny Fernando García 4; Yéssica Paola López 5; Mary Orrego Cardozo 6
1. Licenciado en Biología y Química; Master online en Neurociencias y Biología del Comportamiento. Universidad Autónoma de Manizales. Docente Ciencias Básicas Biológicas; Grupo en Neuroaprendizaje. jmorales@autonoma.edu.co
2. Médica fisiatra; Magister en Investigación y Desarrollo Educativo y Social; Doctora en Ciencias Sociales, Niñez y Juventud. Docente Doctorado en Ciencias Cognitivas. Universidad Autónoma de Manizales. Docente Ciencias Básicas Biológicas; Grupo en Neuroaprendizaje. francia46@gmail.com
3. Fisioterapeuta; Especialista en Neurorehabilitación; Magister en Neurorehabilitación. Docente Ciencias Básicas Biológicas; Grupo en Neuroaprendizaje. luzdary180@gmail.com
4. Médico cirujano. Docente Ciencias Básicas Biológicas; Grupo en Neuroaprendizaje. jofe16@gmail.com
5. Ingeniera Biomédica. Joven Investigadora. Universidad Autónoma de Manizales. Grupo en Neuroaprendizaje. yessipaloe@gmail.com
6. Licenciada en Biología y Química; Magister en Bioquímica y Biología Molecular; Doctora en Bioquímica y Biología Molecular. maryorrego@autonoma.edu.co
Archivos de Medicina (Manizales), Volumen 18 N° 1, Enero-Junio 2018, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Morales J.F.; Restrepo De Mejía F.; Rodríguez Sotelo L.D.; García J.F.; López Y.P.; Orrego Cardozo M.
Recibido para publicación: 29-05-2017 - Versión corregida: 24-03-2018 - Aprobado para publicación: 07-05-2018
Morales JF, Restrepo-de-Mejía F; Rodríguez-Sotelo LD, García JF, López YP, Orrego-Cardozo M. Cafeína y comportamiento animal. Análisis sobre condiciones experimentales. Arch Med (Manizales) 2018; 18(1):152-71. DOI: https://doi.org/10.30554/archmed.18.1.1997.2018.
Resumen
Objetivo: realizar una revisión teórica relacionada con el efecto de la cafeína en el comportamiento animal en estudios que incluyen tareas de aprendizaje, memoria y/o actividad motora, con el fin de analizar algunas condiciones experimentales. Materiales y métodos: búsqueda de artículos publicados entre los años 1995 a 2018 en las bases de datos Pubmed y Scopus por medio de la relación de palabras clave: cafeína, café, ratas, ratones, atención, memoria y aprendizaje. Se revisaron las tareas de aprendizaje y/o actividad motora, el tipo y género de cepas, así como el tratamiento con cafeína. También se incluyeron artículos de revisión de años anteriores al rango de tiempo, con el fin de ampliar el estado del arte de la cafeína y sus efectos. Resultados: mientras algunos estudios indican que la cafeína ejerce un efecto positivo sobre actividades motoras y cognitivas, otros estudios concluyen lo contrario. La variación en las condiciones experimentales de los estudios analizados puede incidir en los resultados obtenidos. Conclusión: el amplio rango de condiciones experimentales en una misma tarea de memoria no permite que se delimite el espectro de variables en los protocolos de investigación con cafeína, por ello no se logra identificar variables biológicamente importantes que, al ser identificadas, pueden convergen hacia un conjunto de procedimientos estandarizados en paradigmas específicos de aprendizaje.
Palabras clave: cafeína, experimentación animal, actividad motora, aprendizaje, memoria, atención.
Caffeine and animal behavior. Analysis of experimental conditions
Summary
Objective: the aim is realize theoretical review related to the effect of caffeine on animal behavior in studies that include task learning, memory and motor activity, with the purpose of study some experimental conditions. Materials and methods: searching of articles published since 1997-2013 in the PubMed and Scopus databases, through the relationship of keywords: caffeine, coffee, rats, mice, attention, memory and learning. The tasks of learning and/or motor activity were reviewed; the type and genus of strains, as well as the treatment with caffeine were analyzed. Results: while some studies indicate that caffeine have a positive effect on motor and cognitive activities, other studies conclude otherwise. The variation in the experimental conditions of the analyzed studies may influence the results obtained. Conclusion: the wide range of experimental conditions in the same memory task does not allow the spectrum of variables to be delineated in the caffeine research protocols, accordingly is not possible to identify biologically important variables that, when identified, may converge towards a Set of standardized procedures in specific learning paradigms.
Key words: caffeine, animal experimentation, motor activity, learning, memory, attention.
Introducción
La cafeína es una de las sustancias psicoactivas más consumidas en el mundo y su ingesta en la dieta, se debe principalmente al consumo de café. El conocimiento actual sobre los efectos de esta sustancia se debe en gran parte a la experimentación animal, principalmente en ratas y ratones, aunque muchos estudios se han realizado en humanos. Los biomodelos han brindado la posibilidad de evaluar con el tiempo respuestas biológicas que son difíciles de seguir en cortos ensayos realizados en humanos, sin embargo, algunos estudios atribuyen efectos positivos y otros negativos de la cafeína en una misma tarea cognitiva o motora y, ante estas diferencias, poco se ha indagado sobre cómo inciden las condiciones experimentales en los resultados de estos estudios. El objetivo de este estudio es realizar una revisión teórica relacionada con el efecto de la cafeína en el comportamiento animal, en estudios que incluyen tareas de aprendizaje, memoria o actividad motora, con el fin de analizar los test y/o aparatos empleados, las tareas de aprendizaje, el tipo y género de cepas, y el tratamiento con cafeína.
1. Experimentación animal
Muchos bioterios alrededor del mundo han implementado la normatividad necesaria para la investigación con modelos animales, y han solucionado aspectos bioéticos exclusivamente pensados en el bienestar animal. A estas comunidades se les otorga validez y relevancia científica, ya que el animal cuenta con un ambiente enriquecido en condiciones óptimas que respaldan los resultados obtenidos en una investigación. Esta consolidación de ambientes enriquecidos logra eliminar el estrés en los animales durante estas investigaciones. Por razones éticas y científicas, los experimentos con animales de laboratorio deben ser adecuadamente diseñados y rigurosamente ejecutados, de modo que puedan ser reportados con suficiente detalle como para reproducir o juzgar críticamente sus hallazgos [1]. El estudio realizado por Kilkenny et al 2009 [2] a solicitud del centro nacional para el reemplazo, refinamiento y reducción de animales en investigación del Reino Unido (NC3Rs, por sus siglas en inglés) evaluó la calidad de las publicaciones de experimentos con animales de laboratorio que habían sido financiados por instituciones de Estados Unidos o del Reino Unido. De acuerdo con los hallazgos del estudio, 87% de los estudios no reportó aleatorización; 86%, enmascaramiento; 41%, hipótesis claras; 30%, métodos estadísticos adecuados, entre otras omisiones.
Los resultados del estudio indican que es difícil evaluar la validez de los experimentos con animales de laboratorio, se aumenta el riesgo de duplicidad y ocurren fallas frecuentes al transferir los resultados de estudios preclínicos a tratamientos de enfermedades humanas [1-3]. El estudio de Kilkenny et al 2009 [2] derivó en las directrices ARRIVE [4] que guía el reporte científico de experimentos con animales de laboratorio, con énfasis en la racionalidad del experimento, la elección de los modelos experimentales, el diseño (grupos, control de sesgos, aleatorización, unidad experimental), los procedimientos (cuánto, cuándo, dónde y por qué), los animales utilizados (características, cepas, crianza), el tamaño de muestra, los efectos experimentales y los métodos estadísticos.
2. Centros de investigación que indagan sobre los efectos de la cafeína
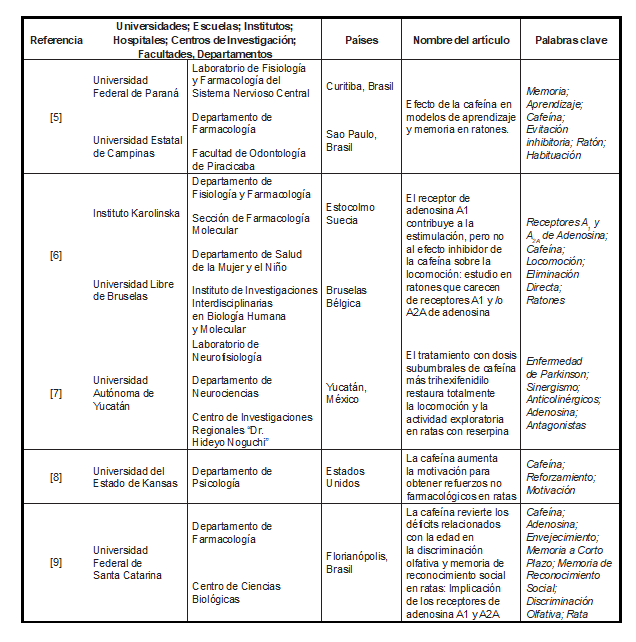
En la búsqueda realizada se encontraron artículos publicados en gran parte por investigadores de Brasil, Estados Unidos, Suecia y Portugal; otros fueron publicados por universidades o centros de investigación de Bélgica, Italia, España, Rusia, China, México, Alemania, Argentina, Bulgaria, Jordania, Francia y Reino Unido (Tabla 1). Algunos estudios se realizaron de manera interinstitucional e interdisciplinaria. Este aspecto es importante ya que puede favorecer el refinamiento de los diseños experimentales siempre y cuando cada centro de investigación genere aportes en el rediseño sobre protocolos y técnicas instrumentales. Además, puede otorgar mayor consenso y discusión sobre resultados obtenidos, al establecerse comunicación personal entre científicos que trabajan sobre un mismo objeto de investigación.
Tabla 1: Países y centros de investigación que evalúan los efectos de la cafeína
3. Análisis de condiciones experimentales en la investigación con cafeína
La medición del comportamiento animal ofrece un vistazo a la actividad neuronal del animal sin los inconvenientes invasivos de insertar electrodos en el cerebro [10]. Es posible observar el movimiento para determinar los ritmos circadianos, el comportamiento exploratorio, la ansiedad, la capacidad y la motivación para aprender un vínculo entre dos señales, la capacidad de navegar en un laberinto y los cambios en el comportamiento locomotor resultante de las manipulaciones farmacológicas [10].
3.1 Pruebas de Comportamiento
La prueba de campo abierto (OFT) es una de las pruebas de comportamiento más utilizada para investigar los efectos de la cafeína en la actividad motora [6,7,11,23] en la memoria de reconocimiento de objetos [20,21,25-29], así como en la memoria de reconocimiento al olor [30]. Algunas de las pruebas de comportamiento comúnmente empleadas en estudios experimentales que evalúan el efecto de la cafeína se resumen en la (Tabla 2).
Tabla 2: Pruebas de comportamiento y aparatos comúnmente empleados en estudios con cafeína
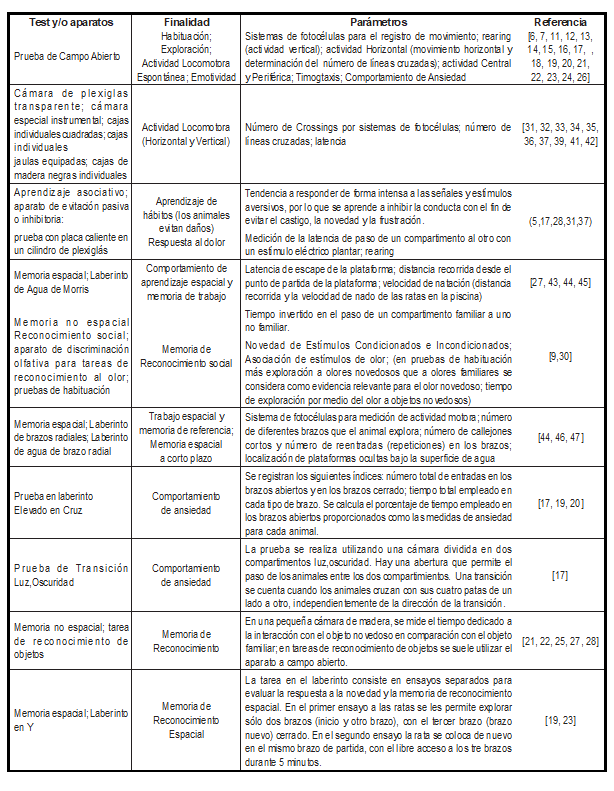

El aparato a campo abierto se compone de una arena grande, de paredes altas que a menudo se utilizan para controlar el comportamiento de ratas [51]. En esta prueba se aprovecha la tendencia natural de las ratas para mostrar tigmotaxis, que se refiere a su preferencia para explorar la periferia de un ambiente nuevo [51]. Las cámaras de plexiglás o cámaras especiales instrumentales también son comúnmente utilizadas para evaluar la actividad motora ante la administración de cafeína [31-42], donde tradicionalmente la actividad horizontal y vertical se evalúa por el número de crossings por un sistemas de fotocélulas, el número de líneas cruzadas y la latencia. La prueba de evitación pasiva también conocida como prueba de evitación inhibitoria, es otra opción que permite estudiar el efecto de la cafeína sobre el aprendizaje adquirido y la memoria [5,17,29,31,37]. La evitación pasiva es una prueba unidireccional en la que el animal se condiciona con un estímulo aversivo y posteriormente se valora si recuerda esa experiencia [52]. La inhibición latente mediante condicionamiento sensorial también se ha estudiado en un paradigma de aversión al sabor [50]. El concepto de inhibición latente hace referencia al retraso que se produce en el condicionamiento a un estímulo cuando ese estímulo ha sido presentado previamente sin ninguna consecuencia [53]. Por otra parte, el laberinto acuático de Morris es una prueba muy usada en el estudio de la memoria espacial, y es ampliamente adaptada en estudios que evalúan el efecto de la cafeína sobre el comportamiento de aprendizaje espacial y la memoria de trabajo [28,43,44,45]. También la exploración preferencial de lugares y objetos novedosos por roedores se ha utilizado para probar los efectos de varias manipulaciones en la memoria de reconocimiento de objetos [54].
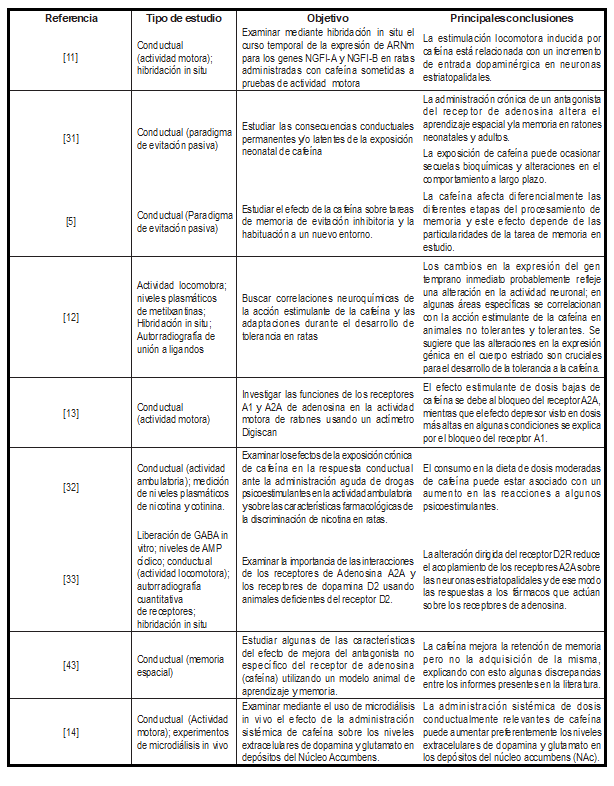
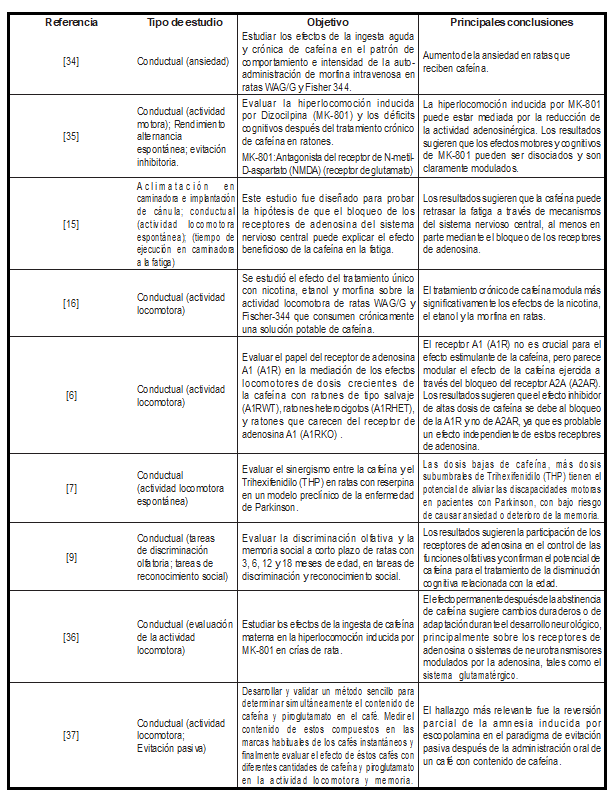
Algunos estudios han evaluado el efecto de la cafeína en la memoria de reconocimiento espacial utilizando un laberinto en Y [19,23], o por medio de pruebas de natación forzada [20,48,49]. También se ha evaluado el efecto de la cafeína sobre la memoria no espacial de reconocimiento social [9,30], la memoria de referencia espacial y a corto plazo en laberinto de brazo radial y laberinto de agua de brazo radial [28,44,46,47], el aprendizaje asociativo en una prueba con placa caliente para evaluar la respuesta al dolor [17], el comportamiento de ansiedad en una laberinto elevado en cruz [17,19,20], y el aprendizaje mediante una prueba de transición luz-oscuridad [17]. En la (tabla 3) se encuentra el tipo de estudio, el objetivo y las principales conclusiones de algunos estudios.
Tabla 3: Tipo de estudios y principales conclusiones
3.2. Tipo de cepa en la investigación con cafeína
Una amplia variedad de cepas están ahora disponibles para la investigación farmacológica, lo que puede plantear problemas sobre cómo las diferencias inherentes entre las cepas pueden afectar la línea base de estudio [55]. La (Tabla 4) resume el tipo de cepas empleadas en investigación con cafeína. En la mayoría de estudios se utilizaron ratas Wistar [7,9,15,18,19,20,21,36,43,45,46,47,48,49,50], seguidas de la cepa Sprague,Dawley [11,12,14,32,37,17,28]. Esto es consistente con el tipo de cepa que se emplea en estudios sobre los efectos de la cafeína en el hipocampo, en el metabolismo y en los parámetros farmacológicos.
Tabla 4: Tipo de cepas en investigación con cafeína

La rata Wistar fue desarrollada en el Wistar Institute en 1906 para fines de investigación biomédica, y se trata de la primera rata empleada como organismo modelo en estudios de comportamiento. Según el estudio realizado por Simpson y Kelly [51], las ratas Sprague,Dawley es la cepa que más se utiliza en estudios farmacológicos para el análisis del comportamiento, aunque en esta revisión es frecuente el uso de la cepa Wistar en estudios con cafeína. Otros estudios emplearon ratas Long Evans [30,31], ratas Swiss [5,13,37], ratas CFI [27,29,35] y Fisher 344 [16,34]. Algunos estudios utilizan varias cepas; en dos estudios realizados por Sudakov et al, [34] y Sudakov et al [16] se evaluó el efecto de la cafeína en la cepa Fisher 344 y en ratas WAG/G. El Yacoubi et al [13] emplearon ratones albinos Swiss CD1 además de ratones que carecen del receptor de adenosina A1 (A1RKO); Halldner et al [6] incluyeron ratones de tipo salvaje (A1RWT), ratones heterocigotos para el receptor de adenosina 1 (A1RHET) y ratones A1RKO. Pires et al [21] utilizan ratas Winstar y ratas espontáneamente hipertensas (SHR); Sousa et al [45] experimentan con ratas Wistar adicional a la cepa C57BL/6J y Pandoldo et al [23] incluyen ratas endogámicas SHR, ratas Winstar Kyoto (WKY) y subcepas NCRL y NicoCrl.
Aunque los estudios suministran información precisa sobre el tipo de cepa empleada, es posible que algunos no indiquen las variantes genéticas de los animales en estudio. En el caso de la cepa Winstar y según los Modelos de Laboratorio Harlan (Harlan Laboratories Models, S.L.) en su documento del 2012: Modelos de Investigación y Servicios [56], existe una serie de ratas consanguíneas como WAG, Wistar Furth y Wistar Kyoto; también ratas no consanguíneas como Wistar; Wistar Han y Wistar Unilever. A pesar de que estas cepas son genéticamente uniformes, las diferencias en consanguinidad y los tamaños morfológicos relativos pueden incidir en el comportamiento ante la administración de cafeína.
3.2.1. Género de cepas
Según Hughes [57], a pesar de la abundante evidencia de las diferencias sexuales en los efectos de las drogas sobre el comportamiento no sexual en ratas y ratones, la mayoría de investigadores continúan usando machos exclusivamente. El estudio de Hughes se realizó durante el período febrero 2005 a septiembre 2006 y hoy en día se sigue investigando principalmente con machos en estudios que miden el comportamiento. En la investigación con cafeína se emplea principalmente ratas macho [5,6,7,9,12,13,14,15,16,18,19,20,24, 25,27,29,30,31,32,34,35,37,39,41,43,45,46,48,49,50,58,59,60], y se utiliza con menos frecuencia ratas hembras [17,22,28,33,36]. Algunos estudios emplean animales de ambos géneros. Zahniser et al [33] utilizan ratones machos y hembras congénicas N5; da Silva et al [36] experimentan con ratas embarazadas Wistar y machos de la misma cepa; Soellner et al [28] emplean ratas hembras y machos Sprague,Dawley para apareamiento así como Abreu et al [22] que usan ratas macho y hembras Wistar. En un estudio reciente, se emplearon ratas espontáneamente hipertensas de ambos géneros para estudiar el efecto de la cafeína suministrada desde la infancia [26].
Según Frye et al [61], la razón principal de la omisión de hembras en estudios que miden el comportamiento, es que su ciclo estral puede tener efectos sobre el comportamiento, además, la inclusión de un grupo de hembras adicional al grupo de machos aumenta al doble el tamaño de la muestra. Así como las diferencias de género en el comportamiento han sido documentadas [62], es importante que en un análisis posterior sobre el tipo de cepa y género se indague sobre el efecto que tienen las variables genéticas y las condiciones morfofisiológicas, así como el efecto en el comportamiento ante la utilización de cepas a diferente edad y los tiempos establecidos para el alojamiento de los animales.
3.3. Tratamientos con cafeína en animales
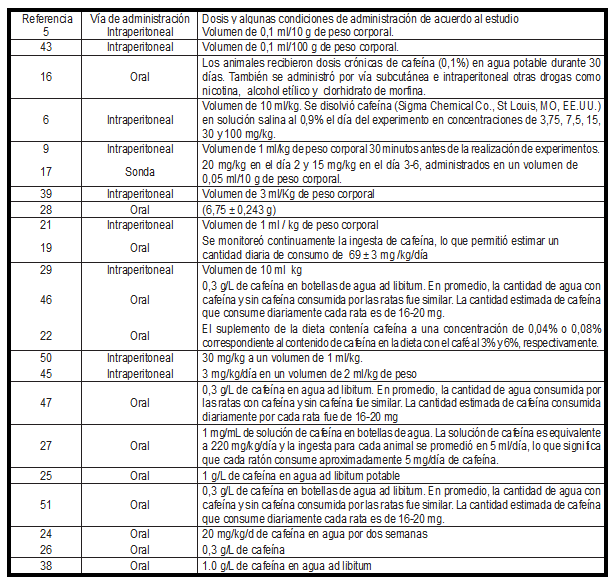
La (Tabla 5) presenta las principales vías de administración de cafeína en estudios de experimentación animal. Es común la administración de este fármaco de forma intraperitoneal [5,6,9,21,29,39,43,45,50], aunque la administración oral también es frecuente debido al tipo de consumo en humanos [16,19,22,25,26,27,28,46,47,51]. En el desarrollo del protocolo sobre la vía de administración farmacológica en biomodelos, es importante manejar adecuadamente las dosis y considerar todas las variables que nacen de factores como el ángulo o profundidad de la jeringa en la inyección peritoneal, o la preparación de suplementos con cafeína en el caso de administración oral. Sin embargo, la medición de las dosis de cafeína intraperitoneal o por vía oral puede que no sean exactas, más cuando se realizan tratamientos frecuentes, ya que dentro de cada fuente de variabilidad la cafeína existe en una cantidad por volumen, adicional al volumen total en cada dosis (o su equivalencia en la concentración por taza en el consumo humano); además, la dosificación por días y semanas puede generar algún tipo de estrés o aversión independiente de si la administración de cafeína es oral o intraperitoneal.
Tabla 5. Vías de administración de cafeína.
Algunos estudios utilizan café como fuente de cafeína en estudios con animales. La preparación y el tiempo de exposición al café (con presencia de cafeína) en el caso de la administración oral, incide en la cantidad de cafeína consumida por los animales; incluso, cuando estas condiciones se mantienen constantes, puede haber variaciones sustanciales en la concentración de cafeína entre raciones. La concentración real puede diferir enormemente de contenidos de cafeína estandarizados [63]. En estudios de auto,administración oral en ratas, la preferencia por solución de cafeína sobre el agua se demostró sólo en concentraciones extremadamente bajas resultando en muy baja ingesta [64]. La preferencia por la cafeína en alta concentración, ingerida en agua potable en cantidades activas, se demostró conductualmente sólo después de un período de 14 días de exposición forzada [65]. La auto,administración oral puede ser aumentada por la privación de alimentos o la exposición crónica de nicotina [64]. El estudio de Shukitt,Hale et al [58] señala que los efectos del consumo de café sobre actividades motoras y cognitivas, no se debe exclusivamente a la presencia de cafeína sino también a la presencia de polifenoles y otros compuestos bioactivos del café. Estos compuestos pueden complementar o sinergizar con la cafeína para producir sus acciones beneficiosas [69]. Los resultados de dicho estudio en ratas indican que el café puede reducir tanto el déficit motor y cognitivo presente durante el envejecimiento, similar a estudios previos con bayas [66,67] y frutos secos [68]. Sin embargo, la presente revisión se concentra en las metodologías que analizan el efecto de la cafeína administrada de forma intraperitoneal o por vía oral en ratas sobre actividades motoras y cognitivas, omitiendo estudios que indagan el efecto de otros compuestos bioactivos presentes en el café.
También sigue siendo tema de debate si el sabor del café y la cafeína pueden influir en su ingesta [70]. Si el agua contiene cafeína y se da de forma crónica a ratas entre 29 y 40 días de vida postnatal, las ratas beben agua con cafeína en mayor cantidad que agua sin cafeína. Asimismo, la administración previa de un agonista de adenosina aumenta la ingesta de cafeína. Por lo tanto, parece que la ingesta de cafeína podría estar al menos en parte relacionada con sus propiedades farmacológicas, aunque la influencia del sabor no puede ser eliminada [71].
Un aspecto importante del uso de cafeína es que el margen para el aumento de dosis puede estar limitado por los efectos bifásicos del fármaco. Las dosis bajas de cafeína causan refuerzo en los animales mientras que las dosis altas producen aversión. Por lo tanto, el refuerzo se puede observar con dosis incluso inferiores a 1 mg/kg, mientras que dosis por encima de 10 a 15 mg/kg son generalmente aversivas. Las dosis que son estimulantes del comportamiento (por ejemplo aumento de la conducta motora) están por debajo de aproximadamente 30 mg/kg y dosis superiores a 50 mg/kg son generalmente depresoras en paradigmas de comportamiento motor. Una curva de dosis-respuesta bifásica similar se observa en humanos, con dosis bajas que se perciben como estimulantes y agradables, mientras que dosis más altas con frecuencia se asocian con disforia o en casos extremos con claros efectos tóxicos [72].
4. Estudios sobre atención y memoria
Investigaciones recientes en humanos y animales relacionan a la cafeína con procesos de atención y memoria. Muchos estudios con ratas indican que la cafeína ejerce un efecto sobre actividades motoras y cognitivas y, aunque su consumo sirve para disminuir el cansancio, aumentar la energía y mejorar el estado de ánimo [73], los resultados en cuanto a su capacidad para mejorar el rendimiento cognitivo son más complejos [3,74], y se cuestiona sobre los reales efectos en las actividades motoras. Los estudios indican que la cafeína influye en procesos de atención y memoria en ratas [5,8,9,19,21,22,23,27,28,29,43,50], en humanos [73,74,75,76,77,78,79,80], incluso en abejas [81]. Angelucci et al [5] indican que la administración de cafeína antes de la sesión de entrenamiento de una tarea de memoria incide sobre el rendimiento, la atención, la adquisición de la memoria y la distinción del proceso [5]. En este sentido, muchos estudios sugieren un efecto positivo sobre la atención y memoria en animales [5,9,21,22,23,25,27,29,30,35,42,43,46,47,58,60,82,83,84,85,86,87,89], mientras otras investigaciones concluyen que la cafeína no influye o altera el rendimiento cognitivo en ratones [17,19,28,31,44,45,88,90,91].
4.1 Efectos positivos de la cafeína en atención y memoria
Si bien los tratamientos con cafeína son en general de tipo crónico, muchos estudios se han efectuado para analizar el efecto agudo de este fármaco sobre la memoria. A menudo se administra cafeína en cantidades de 50,150 mg [72], aunque algunos estudios emplean dosis mayores [92]. Muchas respuestas biológicas a la cafeína presentan una forma de campana, es decir, el efecto va aumentado con la dosis, hasta que, a dosis elevadas, disminuye de manera significativa [72]. Los estudios en roedores realizados por Takahashi et al [93] indican que dosis moderadas de cafeína mejoran la capacidad memorística; las dosis elevadas (30,100 mg/kg), en cambio, interfieren en los procesos de adquisición de memoria. La administración de cafeína con frecuencia provoca una mejora en el rendimiento cognitivo, incluyendo en animales de edad avanzada [9,94]. Se encontró que la sola administración intraperitoneal de cafeína (10 o 30 mg/kg), 30 minutos antes de la realización de las tareas conductuales, invierte los déficits relacionados con la edad en las funciones olfativas y en la memoria de reconocimiento social [9].
Según Costa et al [27] animales de edad avanzada tratados con cafeína muestran un rendimiento similar al de animales adultos en la tarea de nueva preferencia. Abreu et al [22] analizaron la relación entre la edad de roedores, la dosis y las tareas de memoria. Los investigadores indican que la cafeína genera un mejoramiento en los procesos cognitivos medido en varias pruebas, como la memoria espacial, memoria de trabajo y el reconocimiento de objetos [22]. También afirman que la administración de cafeína en ratones adultos impide el deterioro de la memoria de reconocimiento de objetos asociada con la edad. Swenson et al [95] indican que las crías de ratas adultas tratadas con cafeína presentan una mejora significativa en la retención a los 25 días después de la adquisición de la memoria, en comparación con ratas de grupo control. El estudio realizado por Fisher y Guillet [31] señala que la exposición neonatal de cafeína puede alterar el aprendizaje en una forma dependiente de género en un paradigma de evitación pasiva. Ante la administración de 15,20 mg/Kg/día de cafeína, las ratas hembras adultas exhiben un mejoramiento de la retención de memoria a las 24 y 72 h después del entrenamiento, pero los machos exhiben una retención significativamente reducida en ambos períodos de tiempo en el mismo paradigma [31]. Según los investigadores, el mismo tratamiento neonatal con cafeína no causa efectos específicos de género en ratas jóvenes [31].
Entre estos estudios, las evidencias de Angelucci et al [43] indican que la cafeína mejora la retención de la memoria, pero no la adquisición de la misma; según los autores esto explica algunas discrepancias entre los informes en la literatura. Los investigadores sugirieron que la cafeína afecta diferencialmente las diferentes etapas del procesamiento de memoria y que este efecto depende de particularidades en la tarea de estudio [43]. Otros estudios han evaluado el efecto de la cafeína en el tratamiento del trastorno por déficit de atención e hiperactividad (TDAH) en humanos pero también en animales [21]. Algunos resultados sugieren que la cafeína puede representar una importante herramienta terapéutica para el TDAH; se ha demostrado que la administración aguda de cafeína mejora el aprendizaje y varios deterioros de la memoria en tareas de reconocimiento de objetos [21]. Pandolfo et al [23] encontraron mejoría en los déficits de atención y memoria cuando se administró cafeína a ratas en un modelo de TDAH.
Por su parte Botton et al [29] afirman que el tratamiento previo con cafeína es eficaz en la prevención del deterioro de la memoria de corto y largo plazo en tareas de reconocimiento de objetos. Esto confirma el efecto positivo de la administración de cafeína en la tarea de reconocimiento de objetos cuando se evaluó en la memoria a corto plazo [27]. Cognato et al [19] reportan que la cafeína o los antagonistas de adenosina (A2AR) impiden el déficit de memoria causado por citotoxicidad glutamatérgica. Estos hallazgos proporcionan información sobre el potencial de la cafeína frente al deterioro cognitivo completo que muestran las mujeres en el modelo de TDAH. El estudio de Nunes et al [26] revela que la ingesta de cafeína desde la infancia atenúa las alteraciones del comportamiento en un modelo de TDAH asociadas con cambios en los receptores del factor neurotrófico derivado del cerebro (BDNF) y del receptor TrkB en el hipocampo. Según los autores, estos hallazgos proporcionan información sobre el potencial de la cafeína frente al deterioro cognitivo completo que muestran las mujeres en el modelo de TDAH [26]. A pesar de estos hallazgos, algunos estudios afirman que la cafeína no confiere ningún efecto y que incluso puede representar un efecto negativo en la atención y memoria.
4.1.2 Efectos negativos de la cafeína en atención y memoria
El estudio realizado por Loke WH [90] señala que la cafeína no genera un efecto significativo en el desarrollo cognitivo, el aprendizaje y el rendimiento de la memoria. En estudios con ratas adultas Long Evans, se ha afirmado que la administración postnatal de la cafeína deteriora la capacidad espacial de aprendizaje [96]. También se afirma que la administración de 0,03 g/L de cafeína durante la gestación y lactancia, puede generar un déficit en el rendimiento de ratones adultos en un laberinto en Y por medio de tareas de memoria espacial y de reconocimiento de objetos, entre otras tareas de memoria [91]. En otro estudio, se indica que la administración de cafeína a ratas neonatales genera un rendimiento deteriorado de la memoria en tareas de evasión [17].
Soellner et al [28] encontraron que la exposición prenatal crónica de una dosis moderada de cafeína altera el reconocimiento de nuevos objetos y el comportamiento en el laberinto de brazos radiales en ratas machos y hembras adultas; los investigadores también indican que la ingesta oral crónica de cafeína durante toda la gestación puede alterar los procesos cognitivos en ratas adultas. Por su parte Sousa et al [45] afirman que la cafeína provoca alteraciones en el sistema canabinoide en la corteza y el hipocampo, con implicaciones funcionales en la memoria espacial. El estudio de Blaise et al [38] señala que ratas tratadas con cafeína presentan una reducción en la inducción de la potenciación a largo plazo (LTP), significativamente menor en comparación con los controles. Este hallazgo, que revela una disminución en el mecanismo de LTP en ratas tratadas con cafeína, contrasta con un estudio realizado en el 2015 que indicaba que la exposición a la cafeína no alteraba significativamente la LTP [40].
4.1.3 Efectos de la cafeína en la actividad motora.
Hoy en día persiste el debate sobre el efecto de la cafeína en la actividad motora. Algunos estudios señalan que la cafeína aumenta o mejora la actividad motora en animales [7,35,47, 58,60,97] mientras que otros indican lo contrario [22,101]. Marin et al [97] sugieren que la cafeína induce mayor estimulación en la actividad locomotora en ratas adolescentes que en adultas cuando los animales se habitúan al entorno del ensayo; las ratas adolescentes y adultas muestran un efecto locomotor bifásico de estimulación por cafeína, con una mayor actividad locomotora durante la adolescencia y una evidente disminución durante la edad adulta. Dosis pequeñas a moderadas de cafeína generan un aumento en el comportamiento locomotor en ratas adolescentes, mientras que en animales adultos dosis altas no aumenta o disminuye la actividad locomotora [6]. Porciúncula et al [47] también consideran que los animales adultos tratados con bajas dosis de cafeína generan un perfil de hiperlocomocion, mientras que a dosis más altas predomina el estado de hipolocomoción. Según los investigadores, en estudios de actividad motora las crías jóvenes de ratas tratadas con cafeína durante el embarazo a menudo exhiben alteraciones en la actividad locomotora, comparados con sujetos control [47].
En una serie de estudios, la cafeína fue ingerida en agua por parte de ratas durante la gestación o lactancia, o en ambos periodos de tiempo, y la actividad locomotora de la descendencia se evaluó 1, 2, 4 y 6 meses después del nacimiento. Todas las ratas expuestas a cualquiera de las combinaciones de dosis de cafeína durante la gestación y lactancia mostraron menos actividad locomotora [98,96,99]. Hughes y Beveridge [100] sugieren que el efecto de la cafeína depende de la edad. Estos investigadores hallaron que la exposición prenatal de cafeína (20 o 40 mg/kg/día) administrada intraperitonealmente, aumenta la actividad locomotora en el día postnatal 61, aunque no encontraron algún efecto en el día posnatal 145; también reportaron disminución de la actividad motora en el día 188. Sin embargo, Glavin y Krueger [101] no hallaron efecto alguno de (12,5, 25 o 35 mg /kg/día) de cafeína en los días posnatales 48, 68 y 196, a través del consumo en agua potable y con actividades de exploración en un campo abierto.
En esta misma línea de estudio, Tchekalarova et al [102] confirmaron que la cafeína también puede causar diferentes efectos cuando se administra en diferentes días postnatales. La administración de cafeína (10 y 20 mg/kg) entre los días posnatales 7 y 11 genera un estado de hiperlocomoción; cuando se inyecta entre los días posnatales 13 y 17, las ratas fueron menos activas que los controles entre los 25 y 32 días posnatales. En otro estudio, la cafeína fue administra por sonda entre los días postnatales 2 y 6 y la actividad locomotora se incrementó a los 12 días de edad [103], pero no a los 28, 70 o 90 días de edad [104]. Angelucci et al [5] indican que ratas administradas con cafeína incrementan su conducta exploratoria en un campo abierto; sin embargo, mediante una prueba de campo abierto, se encontró que la suplementación de la dieta con cafeína no tuvo efecto sobre las actividades locomotoras y exploratorias de ratas, es decir, la mejora en el rendimiento cognitivo de los animales por la ingestión de cafeína no se acompañó por un aumento de las funciones motoras y sensoriales [22]. Todos los grupos experimentales mostraron menor actividad locomotora y exploratoria en algunas etapas de los experimentos; según los autores, esto demuestra la poca relación de los efectos de la cafeína en la memoria no asociativa (implícita).
Es así como los beneficios cognitivos de la memoria a largo plazo no muestra efectos secundarios significativos en las funciones sensoriales y motoras que se pueden afectar por la administración aguda de cafeína [22]; sin embargo, aunque el estudio de Abreu y colegas comprueba que dosis bajas de cafeína no inciden en el comportamiento locomotor de ratas adultas, los resultados de Angelucci et al [5] parecen indicar lo contrario; esto representa una de varias inconsistencias en la investigación sobre el efecto de la cafeína en la actividad motora. La prueba de campo abierto se emplea con frecuencia en estudios con cafeína; el aparato se usa para registrar actividad motora vertical, horizontal, central y periférica [6,7,11,12,13,14,15], así como para el estudio de la memoria de reconocimiento de objetos [25,27,28,21,22]. Algunos estudios han reportado efectos positivos de la cafeína en la actividad motora [6,7,11,12,13] donde los investigadores han empleado parámetros que de acuerdo con otros estudios, no se modifican o incluso se alteran ante el consumo de cafeína [17,19]. Se han registrado efectos positivos de la cafeína sobre el aprendizaje asociativo usando aparatos de evitación pasiva o inhibitoria [5,37], sin embargo, otros estudios indican bajo parámetros similares en las mismas tareas, efectos nocivos o baja actividad motora [17,28,31]. Finalmente, en un estudio publicado en el 2016, se investigó el efecto de un tratamiento crónico con cafeína en dosis moderadas sobre la actividad motora en ratas Wistar diabéticas [24]. Los resultados indican que la exposición crónica a la cafeína perjudica la actividad locomotora en ratas control pero no en ratas diabéticas [24], resaltando con ello el posible potencial terapéutico de este fármaco sobre el síndrome metabólico relacionado con la diabetes, pero no el impacto de su uso recreativo con fines de mejoras en el rendimiento motor.
Conclusiones
Se evidencian algunos resultados contradictorios en la investigación con cafeína en ratas y faltan estudios concluyentes sobre su efecto en la memoria y el aprendizaje. Los factores bioquímicos relacionados con el mecanismo de acción y la farmacocinética de la cafeína están bien establecidos, pero se requieren más estudios que profundicen sobre el efecto de este fármaco en la neuroanatomía, en tareas de actividad motora y en funciones cognitivas. Esta revisión confirma que no existen procedimientos estandarizados en paradigmas específicos de aprendizaje y esto puede ser una de las causas de los hallazgos contradictorios.
Al parecer, las variables conductuales de ratas sometidas a diferentes tareas de memoria demuestran un efecto en el comportamiento que varía ante el tipo de paradigma empleado, las dosis de cafeína y las condiciones experimentales del estudio. A pesar del creciente interés en investigación con cafeína y memoria, se conoce poco sobre su efecto en el procesamiento de la memoria de reconocimiento de objetos y no se cuenta aún con un conocimiento que sea coherente con la evidencia experimental. Así mismo, los estudios que indagan sobre el efecto de la cafeína en la actividad motora, señalan que ésta incide en un aumento de las funciones locomotrices mientras que otras investigaciones afirman lo contrario.
Conflictos de interés: No presentamos conflictos de interés.
Fuentes de financiación: Financiación propia.
Literatura citada
- Soto-Becerra P, Wong P. El 1, 2, 3… y 4 de la experimentación con animales de laboratorio: las directrices ARRIVE [carta]. Rev Peru Med Exp Salud Publica 2016; 33(4):836-7. DOI: 10.17843/ rpmesp.2016.334.2579.
- Kilkenny C, Parsons N, Kadyszewski E, Festing MFW, Cuthill IC, Fry D, et al. Survey of the quality of experimental design, statistical analysis and re- porting of research using animals. PloS One 2009; 4(11):e7824. DOI: 10.1371/journal.pone.0007824.
- Baker D, Lidster K, Sottomayor A, Amor S. Two years later: journals are not yet enforcing the ARRIVE guidelines on reporting standards for pre-clinical animal studies. PLoS Biol 2014; 12(1):e1001756. DOI: 10.1371/journal.pbio.1001756.
- Kilkenny C, Browne WJ, Cuthill IC, Emerson M, Altman DG. Improving Bioscience Research Re- porting: The ARRIVE Guidelines for Reporting Animal Research. PLOS Biol 2010; 8(6):e1000412. DOI: 10.1371/journal.pbio.1000412.
- Angelucci ME, Vital MA, Cesário C, Zadusky CR, Rosalen PL, Da Cunha C. The effect of caffeine in animal models of learning and memory. Eur J Pharmacol 1999; 373(2-3):135-40. DOI: 10.1016/ S0014-2999(99)00225-3.
- Halldner L, Adén U, Dahlberg V, Johansson B, Ledent C, Fredholm BB. The adenosine A1 re- ceptor contributes to the stimulatory, but not the inhibitory effect of caffeine on locomotion: a study in mice lacking adenosine A1 and/or A2A receptors. Neuropharmacology 2004; 7:1008-17. DOI: 10.1016/j.neuropharm.2004.01.014.
- Moo RE, Villanueva J, Arankowsky G, Alvarez F, Góngora JL. Treatment with subthreshold doses of caffeine plus trihexyphenidyl fully restores locomotion and exploratory activity in reserpin- ized rats. Neurosci Lett 2004; 367(3):327-31. DOI: 10.1016/j.neulet.2004.06.022.
- Sheppard AB, Gross SC, Pavelka SA, Hall MJ, Palmatier MI. Caffeine increases the motivation to obtain non-drug reinforcers in rats. Drug Alco- hol Depend 2012; 124(3):216-222. DOI: 10.1016/j. drugalcdep.2012.01.008.
- Prediger RD, Batista LC, Takahashi RN. Caffeine reverses age-related deficits in olfactory discri- mination and social recognition memory in rats Involvement of adenosine A1 and A2A receptors. Neurobiol Aging 2005; 6:957-64. DOI: 10.1016/j. neurobiolaging.2004.08.012.
- Ramazani R.B,. Krishnan H.R, Bergeson SE, Atkinson NS. Computer automated movement detection for the analysis of behavior. J Neu- rosci Methods 2007; 162:171–179. DOI: 10.1016/j. jneumeth.2007.01.005.
- Svenningsson P, Nomikos GG, Fredholm BB. Bipha- sic changes in locomotor behavior and in ex- pression of mRNA for NGFI-A and NGFI-B in rat striatum following acute caffeine administration. J Neurosci 1995; 15(11):7612-24. DOI: 10.1523/ JNEUROSCI.15-11-07612.1995.
- Svenningsson P, Nomikos GG, Fredholm BB. The stimulatory action and the development of tole- rance to caffeine is associated with alterations in gene expression in specific brain regions. J Neurosci 1999; 19(10):4011-22. DOI: 10.1523/ JNEUROSCI.19-10-04011.1999.
- El Yacoubi M, Ledent C, Ménard JF, Parmentier M, Costentin J, Vaugeois JM. The stimulant effects of caffeine on locomotor behaviour in mice are me- diated through its blockade of adenosine A(2A) receptors. Br J Pharmacol 2000; 129(7):1465-73. DOI 10.1038/sj.bjp.0703170.
- Solinas M, Ferré S, You ZB, Karcz-Kubicha M, Popoli P, Goldberg SR. Caffeine induces dopamine and glutamate release in the shell of the nucleus accumbens. J Neurosci 2002; 22(15):6321-4. DOI: 10.1523/JNEUROSCI.22-15-06321.2002.
- Davis JM, Zhao Z, Stock HS, Mehl KA, Buggy J, Hand GA. Central nervous system effects of caffeine and adenosine on fatigue. Am J Physiol Regul Integr Comp Physiol 2003; 284(2):R399-404. DOI: 10.1152/ajpregu.00386.2002.
- Sudakov SK, Rusakova IV, Medvedeva OF. Effect of chronic caffeine consumption on changes in locomotor activity of WAG/G and Fischer-344 rats induced by nicotine, ethanol, and morphine. Bull Exp Biol Med 2003; 136(6):563-5. DOI: 10.1523/ JNEUROSCI.15-11-07612.1995.
- Pan HZ, Chen HH. Hyperalgesia, low-anxiety, and impairment of avoidance learning in neonatal caffeine-treated rats. Psychopharmacology (Berl) 2007; 191(1):119-25. DOI: 10.1007/s00213-006- 0613-y.
- Boeck CR, Marques VB, Valvassori SS, Cons- tantino LC, Rosa DV, Lima FF, et al. Early long-term exposure with caffeine induces cross-sensitization to methylphenidate with involvement of DARPP-32 in adulthood of rats. Neurochem Int 2009; 55(5):318-22. DOI: 10.1016/j. neuint.2009.03.015.
- Cognato GP, Agostinho PM, Hockemeyer J, Müller CE, Souza DO, Cunha RA. Caffeine and an adenosine A(2A) receptor antagonist prevent memory impairment and synaptotoxicity in adult rats triggered by a convulsive episode in early life. J Neurochem 2010; 112(2):453-62. DOI: 10.1111/j.1471-4159.2009.06465.x.
- Pechlivanova D, Tchekalarova J, Nikolov R, Ya- kimova K. Dose-dependent effects of caffeine on behavior and thermoregulation in a chronic unpredictable stress model of depression in rats. Behav Brain Res 2010; 209(2):205-11. DOI: 10.1016/j.bbr.2010.01.037.
- Pires VA, Pamplona FA, Pandolfo P, Prediger RD, Takahashi RN. Chronic caffeine treatment during prepubertal period confers long-term cognitive benefits in adult spontaneously hypertensive rats (SHR), an animal model of attention deficit hyperactivity disorder (ADHD). Behav Brain Res 2010; 215(1):39-44. DOI: 10.1016/j.bbr.2010.06.022.
- Abreu RV, Silva-Oliveira EM, Moraes MF, Pereira GS, Moraes-Santos T. Chronic coffee and caffeine ingestion effects on the cognitive function and antioxidant system of rat brains. Pharmacol Bio- chem Behav 2011; 99(4):659-64. DOI: 10.1016/j. pbb.2011.06.010.
- Pandolfo P, Machado NJ, Köfalvi A, Takahashi RN, Cunha RA. Caffeine regulates frontocorticostria- tal dopamine transporter density and improves attention and cognitive deficits in an animal model of attention deficit hyperactivity disorder. Eur Neuropsychopharmacol 2013; 23(4):317-28. DOI: 10.1016/j.euroneuro.2012.04.011.
- 24. Bădescu SV, Tătaru CP, Kobylinska L, Georgescu EL, Zahiu DM, Zăgrean AM, et al. Effects of caf- feine on locomotor activity in streptozotocin-in- duced diabetic rats. J Med Life 2016; 9(3):275-279.
- Espinosa J, Rocha A, Nunes F, Costa MS, Schein V, Kazlauckas V, et al. Caffeine consumption prevents memory impairment, neuronal damage, and adenosine A2A receptors upregulation in the hippocampus of a rat model of sporadic de- mentia. J Alzheimers Dis 2013; 34(2):509-18. DOI: 10.3233/JAD-111982.
- Nunes F, Pochmann D, Almeida AS, Marques DM, de Oliveira Porciúncula L. Differential Behavioral and Biochemical Responses to Caffeine in Male and Female Rats from a Validated Model of Attention Deficit and Hyperactivity Disorder. Mol Neurobiol 2018. DOI: 10.1007/s12035-018-1000-5.
- Costa MS, Botton PH, Mioranzza S, Souza DO, Porciúncula LO. Caffeine prevents age-associ- ated recognition memory decline and changes brain-derived neurotrophic factor and tirosine kinase receptor (TrkB) content in mice. Neu- roscience 2008; 153(4):1071-8. DOI: 10.1016/j. neuroscience.2008.03.038.
- Soellner DE, Grandys T, Nuñez JL. Chronic prenatal caffeine exposure impairs novel object recog- nition and radial arm maze behaviors in adult rats. Behav Brain Res 2009; 14; 205(1):191-9. DOI: 10.1016/j.bbr.2009.08.012.
- Botton PH, Costa MS, Ardais AP, Mioranzza S, Souza DO, da Rocha JB, et al. Caffeine prevents disrup- tion of memory consolidation in the inhibitory avoidance and novel object recognition tasks by scopolamine in adult mice. Behav Brain Res 2010; 25; 214(2):254-9.DOI: https://doi.org/10.1016/j. bbr.2010.05.034.
- Spinetta MJ, Woodlee MT, Feinberg LM. Stroud C, Schallert K, Cormack LK, Schallert T. Alcohol-in- duced retrograde memory impairment in rats: prevention by caffeine. Psychopharmacology 2008; 201(3): 361–371.DOI: 10.1007/s00213-008- 1294-5.
- Fisher S, Guillet R. Neonatal caffeine alters pas- sive avoidance retention in rats in an age- and gender-related manner. Brain Res Dev Brain Res 1997; 98(1):145-9 DOI: https://doi.org/10.1016/ S0165-3806(96)00158-7.
- Gasior M, Jaszyna M, Peters J, Goldberg SR. Changes in the Ambulatory Activity and Dis- criminative Stimulus Effects of Psychostimulant Drugs in Rats Chronically Exposed to Caffeine: Effect of Caffeine Dose. J Pharmacol Exp Ther 2000; 295(3):1101-11.
- Zahniser NR, Simosky JK, Mayfield RD, Negri CA, Hanania T, Larson GA, et al. Functional uncoupling of adenosine A(2A) receptors and reduced responseto caffeine in mice lack- ing dopamine D2 receptors. J Neurosci 2000; 20(16):5949-57.DOI: https://doi.org/10.1523/JNEU- ROSCI.20-16-05949.2000.
- Sudakov SK, Papazov IP, Lyupina YV, Medvedeva OF, Figurina IV, Rusakova IV. Effects of acute and chronic caffeine intake on intravenous self-ad- ministration of morphine in two rat strains. Bull Exp Biol Med 2002; 134(4):400-2. DOI: https://doi. org/10.1023/A:1021980919850.
- Dall’Igna OP, Da Silva AL, Dietrich MO, Hoffmann A, de Oliveira RV, Souza DO, et al. Chronic treatment with caffeine blunts the hyperlocomotor but not cognitive effects of the N-methyl-D-aspartate receptor antagonist MK-801 in mice. Psychophar- macology (Berl) 2003; 166(3):258-63. DOI: 10.1007/ s00213-002-1362-1.
- da Silva RS, Hoffman A, de Souza DO, Lara DR, Bonan CD. Maternal caffeine intake impairs MK- 801-induced hyperlocomotion in young rats. Eur J Pharmacol 2005; 509(2-3):155-9. DOI: 10.1016/j. ejphar.2005.01.001.
- Maeso N, del Castillo C, Cornejo L, García-Acicollar M, Alguacil LF, Barbas C. Capillary electrophoresis for caffeine and pyroglutamate determination in coffees Study of the in vivo effect on learn- ing and locomotor activity in mice. J Pharm Biomed Anal 2006; 41(4):1095-100. DOI: 10.1016/j. jpba.2006.01.062.
- Blaise JH, Park JE, Bellas NJ, Gitchell TM, Phan V. Caffeine consumption disrupts hippocampal long-term potentiation in freely behaving rats. Physiol Rep 2018; 6(5): e13632. DOI: 10.14814/ phy2.13632.
- Simola N, Tronci E, Pinna A, Morelli M. Subchron- ic-intermittent caffeine amplifies the motor ef- fects of amphetamine in rats. Amino Acids 2006; 31(4):359-63. DOI: 10.1007/s00726-006-0373-3.
- Alhaider IA, Alkadhi KA. Caffeine treatment pre- vents rapid eye movement sleep deprivation-in- duced impairment of late-phase long-term poten- tiation in the dentate gyrus. Eur J Neurosci 2015; 42(10):2843-50. DOI: 10.1111/ejn.13092.
- Zancheta R, Possi AP, Planeta CS, Marin MT. Re- peated administration of caffeine induces either sensitization or tolerance of locomotor stimula- tion depending on the environmental context. Pharmacol Rep 2012; 64(1):70-7. DOI: 10.1016/ S1734-1140(12)70732-6.
- Moy GA, McNay EC. Caffeine prevents weight gain and cognitive impairment caused by a high-fat diet while elevating hippocampal BDNF. Physiol Behav 2013; 109:69-74. DOI: 10.1016/j. physbeh.2012.11.008.
- Angelucci ME, Cesário C, Hiroi RH, Rosalen PL, Da Cunha C. Effects of caffeine on learning and memory in rats tested in the Morris water maze. Braz J Med Biol Res 2002; 35(10):1201-8.DOI: http:// dx.doi.org/10.1590/S0100-879X2002001000013.
- Giménez-Llort L, Masino SA, Diao L, Fernández- Teruel A, Tobeña A, Halldner L, et al. Mice lacking the adenosine A1 receptor have normal spatial learning and plasticity in the CA1 region of the hippocampus, but they habituate more slowly. Synapse 2005; 57(1):8-16. DOI: 10.1002/ syn.20146.
- Sousa VC, Assaife-Lopes N, Ribeiro JA, Pratt JA, Brett RR, Sebastião AM. Regulation of hippo- campal cannabinoid CB1 receptor actions by adenosine A1 receptors and chronic caffeine administration: implications for the effects of Δ9-tetrahydrocannabinol on spatial memory. Neuropsychopharmacology 2011; 36(2):472-87. DOI:10.1038/npp.2010.179.
- Alhaider IA, Aleisa AM, Tran TT, Alzoubi KH, Alkadhi KA. Chronic caffeine treatment prevents sleep deprivation-induced impairment of cognitive function and synaptic plasticity. Sleep 2010; 33(4):437-44.
- Alzoubi KH, Abdul-Razzak KK, Khabour OF, Al- Tuweiq GM, Alzubi MA, Alkadhi KA. Caffeine pre- vents cognitive impairment induced by chronic psychosocial stress and/or high fat-high carbo- hydrate diet. Behav Brain Res 2013; 237:7-14.DOI: 10.1016/j.bbr.2012.09.018.
- da Costa Santos VB, Ruiz RJ, Vettorato ED, Nakamura FY, Juliani LC, Polito MD, et al. Effects of chronic caffeine intake and low-intensity exercise on skeletal muscle of Wistar rats. Exp Physiol 2011; 96(11):1228-38. DOI: 10.1113/ expphysiol.2011.060483.
- Franco FS, Costa NM, Ferreira SA, Carneiro-Junior MA, Natali AJ. The effects of a high dosage of creatine and caffeine supplementation on the lean body mass composition of rats submitted to vertical jumping training. Journal of the In- ternational Society of Sports Nutrition 2011; 8:3. DOI: 10.1186/1550-2783-8-3.
- de Aguiar MJ1, de Aguiar CR, Guedes RC. Caffeine/nutrition interaction in the rat brain: Influence on latent inhibition and cortical spreading depression. Eur J Pharmacol 2011; 650(1):268-74. DOI: 10.1016/j.ejphar.2010.10.036.
- Simpson J, Kelly JP. The impact of environmental enrichment in laboratory rats--behavioural and neurochemical aspects. Behav Brain Res 2011; 222(1):246-64. DOI: 10.1016/j.bbr.2011.04.002.
- Navarrete F, Pérez-Ortiz JM, Femenía T, García- Gutiérrez MS, García-Payá ME, Leiva-Santana C, et al. Methods to evaluate cognitive dis- orders in animal models. Rev Neurol 2008; 47(3):137-45.
- Lubow RE, De la Casa LG. There is a time and a place for everything: bidirectional modu- lations of latent inhibition by time-induced context differentiation. Psychon Bull Rev 2005; 12(5):806-21.
- Benice TS, Raber J. Object recognition analysis in mice using nose-point digital video tracking. J Neurosci Methods 2008; 168(2):422-30. DOI: 10.1016/j.jneumeth.2007.11.002.
- McDermott C, Kelly JP. Comparison of the be- havioural pharmacology of the Lister-Hooded with 2 commonly utilised albino rat strains. Prog Neuropsychopharmacol Biol Psychiatry 2008; 32(8):1816-23. DOI: https://doi.org/10.1016/j. pnpbp.2008.08.004.
- Klein HJ, Mickelson B, Wineinger A. Tarifa de Precios. Modelos de Investigación y Servi- cios. Indianapolis. Harlan Laboratories Models, S.L. 2012.
- Hughes RN. Sex does matter: comments on the prevalence of male-only investigations of drug effects on rodent behaviour. Behav Pharmacol 2007; 18(7):583-9. DOI: 10.1097/ FBP.0b013e3282eff0e8.
- Shukitt-Hale B, Miller MG, Chu YF, Lyle BJ, Jo- seph JA. Coffee, but not caffeine, has positive effects on cognition and psychomotor behavior in aging. Age (Dordr) 2013; 35(6):2183-92. DOI: 10.1007/s11357-012-9509-4.
- Cechella JL, Leite MR, da Rocha JT, Dobrachinski F, Gai BM, Soares FA. et al. Caffeine suppresses ex- ercise-enhanced long-term and location memory in middle-aged rats: Involvement of hippocampal Akt and CREB signaling. Chem Biol Interact 2014; 223:95-101. DOI: 10.1016/j.cbi.2014.09.001.
- Sandner G, Angst MJ, Guiberteau T, Guignard B, Nehlig A. Effects of caffeine or RX821002 in rats with a neonatal ventral hippocampal lesion. Front Behav Neurosci 2014; 8:15. DOI: 10.3389/ fnbeh.2014.00015.
- Frye CA, Duffy CK, Walf AA. Estrogens and pro- gestins enhance spatial learning of intact and ovariectomized rats in the object placement task. Neurobiol Learn Mem 2007; 88(2):208-16.DOI: https://doi.org/10.1016/j.nlm.2007.04.003.
- Fernandes C, González MI, Wilson CA, File SE. Factor analysis shows that female rat behaviour is characterized primarily by activity, male rats are driven by sex and anxiety. Pharmacol Bio- chem Behav 1999; 64(4):731-8. DOI: https://doi. org/10.1016/S0091-3057(99)00139-2.
- Bracken MB, Triche E, Grosso L, Hellenbrand K, Belanger K, Leaderer BP. Heterogeneity in assess- ing self-reports of caffeine exposure: implica- tions for studies of health effects. Epidemiology 2002; 13(2):165-71.
- Heppner CC, Kemble ED, Cox WM. Effects of food deprivation on caffeine consumption in male and female rats. Pharmacol Biochem Behav 1986; 24(6):1555-9. DOI: https://doi.org/10.1016/0091- 3057(86)90484-3.
- Vitiello MV, Woods SC. Evidence for withdrawal from caffeine by rats. Pharmacol Biochem Behav 1977; 6(5):553-5.DOI: https://doi.org/10.1016/0091- 3057(77)90116-2.
- Joseph JA, Shukitt-Hale B, Denisova NA, Bielinski D, Martin A, McEwen JJ, Bickford PC. Reversals of agerelated declines in neuronal signal trans- duction, cognitive, and motor behavioral deficits with blueberry, spinach, or strawberry dietary sup- plementation. J Neurosci 1999; 19(18):8114–8121.
- Shukitt-Hale B, Cheng V, Joseph JA. Effects of blackberries on motor and cognitive function in aged rats. Nutr Neurosci 2009; 12(3):135–140. DOI: 10.1179/147683009X423292.
- Willis LM, Shukitt-Hale B, Cheng V, Joseph JA. Dose dependent effects of walnuts on motor and cognitive function in aged rats. Br J Nutr 2009; 101:1140–1144. DOI: 10.1017/S0007114508059369.
- Cao C, Wang L, Lin X, Mamcarz M, Zhang C, Bai G, et al. Caffeine synergizes with another coffee component to increase plasma GCSF: linkage to cognitive benefits in Alzheimer’s mice. J Al- zheimers Dis 2011; 25(2):323–335. DOI: 10.3233/ JAD-2011-110110.
- Nehlig A. Are we dependent upon coffee and caffeine? A review on human and animal data. Neurosci Biobehav Rev 1999; 23(4):563-76. DOI: 10.1016/S0149-7634(98)00050.
- Newland MC, Brown K. Oral caffeine consumption by rats: the role of flavor history, concentration, concurrent food, and an adenosine agonist. Phar- macol Biochem Behav 1992; 42:651–659.
- Fredholm BB, Bättig K, Holmén J, Nehlig A, Zvartau EE. Actions of caffeine in the brain with special reference to factors that contribute to its wides- pread use. Pharmacol Rev 1999; 51(1):83-133.
- Herz RS. Caffeine efects on mood and memory.Behav Res Ther 1999; 37: 869-879. DOI: https://doi. org/10.1016/S0005-7967(98)00190-9.
- Klaassen EB, de Groot RH, Evers EA, Snel J, Veerman EC, Ligtenberg AJ, et al. The effect of caffeine on working memory load-related brain activation in middle-aged males.Neuropharmacol- ogy 2013; 64:160-7. DOI: https://doi.org/10.1016/j. neuropharm.2012.06.026.
- Brunyé TT, Mahoney CR, Lieberman HR, Giles GE, Taylor HA. Acute caffeine consumption enhances the executive control of visual attention in ha- bitual consumers. Brain Cogn 2010; 74(3):186-92. DOI: 10.1016/j.bandc.2010.07.006.
- Foxe JJ, Morie KP, Laud PJ, Rowson MJ, de Bruin EA, Kelly SP. Assessing the effects of caffeine and theanine on the maintenance of vigilance during a sustained attention task. Neurophar- macology 2012; 62(7):2320-7 DOI: https://doi. org/10.1016/j.neuropharm.2012.01.020.
- Osada JE, Rojas MO, Rosales CE, Vega J. Con- sumo de cafeína en estudiantes de medicina y su coexistencia con sintomatología ansiosa y depresiva. Rev Med Hered 2008; 19 (3):102-107. DOI: https://doi.org/10.20453/rmh.v19i3.964.
- Giles GE, Mahoney CR, Brunyé TT, Gardony AL, Tay- lor HA, Kanarek RB. Differential cognitive effects of energy drink ingredients: Caffeine, taurine, and glucose. Pharmacol Biochem Behav 2012; 102(4):569-77. DOI: 10.1016/j.pbb.2012.07.004.
- Calev A Neuropsychology and ECT: past and future research trends. Psychopharmacol Bull 1994; 30(3):461-9.
- Mednick SC, Cai DJ, Kanady J, Drummond SP. Comparing the benefits of Caffeine, Naps and Placebo on Verbal, Motor and Perceptual Me- mory. Behav Brain Res 2008; 193(1):79–86. DOI: 10.1016/j.bbr.2008.04.028.
- Mustard JA, Dews L, Brugato A, Dey K, Wright GA. Consumption of an acute dose of caffeine re- duces acquisition but not memory in the honey bee. Behav Brain Res 2012; 232(1):217-24. DOI: 10.1016/j.bbr.2012.04.014.
- Molinengo L, Orsetti M, Pastorello B, Scordo I, Ghi P. Habituation of exploratory activity in rats: action of N6phenylisopropyladenosine, caffeine and their combination. Prog Neuropsychopharmacol Biol Psychiatry 1995; 19(7):1189-200.
- Cestari V, Castellano C. Caffeine and cocaine interaction on memory consolidation in mice. A Arch Int Pharmacodyn Ther 1996; 331(1):94-104.
- Howell LL, Coffin VL, Spealman RD. Behavioral and physiological effects of xanthines in non- human primates. Psychopharmacology (Berl) 1997; 129(1):1-14. DOI: 10.1007/s002130050155.
- Smith A, Maben A, Brockman P. Effects of evening meals and caffeine on cognitive performance, mood and cardiovascular functioning. Appetite 1994; 22(1):57-65. DOI: 10.1006/appe.1994.1005.
- Green JM, Olenick A, Eastep C, Winchester L. Caffeine influences cadence at lower but not higher intensity RPE-regulated cycling. Physiol Behav 2017; 169:46-51. DOI: 10.1016/j.phys- beh.2016.11.007.
- Wilhelmus MM, Hay JL, Zuiker RG, Okkerse P, Per- drieu C, Sauser J, et al. Effects of a single, oral 60 mg caffeine dose on attention in healthy adult subjects. J Psychopharmacol 2017; 31(2):222-232. DOI: 10.1177/026988111666859.
- Furusawa K. Drug effects on cognitive function in mice determined by the non-matching to sample task using a 4-arm maze. Jpn J Pharmacol 1991, 56(4): 483-93.
- Han K, Jia N, Li J, Yang L, Min LQ. Chronic ca- ffeine treatment reverses memory impairment and the expression of brain BNDF and TrkB in the PS1/APP double transgenic mouse model of Alzheimer’s disease. Mol Med Rep 2013; 8(3):737- 40. DOI: 10.3892/mmr.2013.1601.
- Loke WH. Effects of caffeine on mood and me- mory. Physiol Behav 1988; 44(3):367-72. DOI: https://doi.org/10.1016/0031-9384(88)90039-X.
- Silva CG, Métin C, Fazeli W, Machado NJ, Darmopil S, Launay PS, et al. Adenosine receptor antagonists including caffeine alter fetal brain development in mice. Sci Transl Med 2013; 5(197):197ra104. DOI: 10.1126/scitranslmed.3006258.
- Cunha RA. Cafeína, receptores de adenosina, memoria y enfermedad de Alzheimer. Med Clin (Barc) 2008; 131(20):790-5. DOI: 10.1016/S0025- 7753(08)75506-4.
- Takahashi RN, Pamplona FA, Prediger RD. Ade- nosine receptor antagonists for cognitive dys- function: a review of animal studies. Front Biosci 2008; 13:2614-32.
- Higgins GA, Grzelak ME, Pond AJ, Cohen-Williams ME, Hodgson RA, Varty GB. The effect of caffeine to increase reaction time in the rat during a test of attention is mediated through antagonism of adenosine A2A receptors. Behav Brain Res 2007; 185(1):32-42. DOI: 10.1016/j.bbr.2007.07.013.
- Swenson RR, Beckwith BE, Lamberty KJ, Krebs SJ, Tinius TP. Prenatal exposure to AVP or caf- feine but not oxytocin alters learning in female rats. Peptides 1990. 11(5):927-32. DOI: https://doi. org/10.1016/0196-9781(90)90011-S.
- Zimmerberg B, Carr KL, Scott A, Lee HH, Weider JM. The effects of postnatal caffeine exposure on growth, activity and learning in rats. Pharma- col Biochem Behav 1991; 39(4):883-8. DOI: https:// doi.org/10.1016/0091-3057(91)90048-7.
- Marin MT, Zancheta R, Paro AH, Possi AP, Cruz FC, Planeta CS. Comparison of caffeine-induced locomotor activity between adolescent and adult rats. Eur J Pharmacol 2011; 660(2-3):363-7. DOI: https://doi.org/10.1016/j.ejphar.2011.03.052.
- Concannon JT, Braughler JM, Schechter MD. Pre- and postnatal effects of caffeine on brain bio- genic amines, cyclic nucleotides and behavior in developing rats. J Pharmacol Exp Ther 1983; 226(3):673-9.
- Hughes RN, Beveridge IJ. Behavioral effects of exposure to caffeine during gestation, lactation or both. Neurotoxicol Teratol 1991; 13(6):641-7. DOI: https://doi.org/10.1016/0892- 0362(91)90048-2.
- Hughes RN, Beveridge IJ. Sex-and age-depen- dent effects of prenatal exposure to caffeine on open-field behavior, emergence latency and ad- renal weights in rats. Life Sci 1990; 47(22):2075- 88. DOI: 10.1016/0024-3205(90)90443-U.
- Glavin GB, Krueger H. Effects of prenatal caf- feine administration on offspring mortality, open-field behavior and adult gastric ulcer susceptibility. Neurobehav Toxicol Teratol 1985; 7(1):29-32.
- Tchekalarova J, Kubova H, Mares P. Postnatal caffeine exposure: effects on motor skills and locomotor activity during ontogenesis. Behav Brain Res 2005; 160(1):99-106. DOI: https://doi. org/10.1016/j.bbr.2004.11.018.
- Guillet R. Neonatal caffeine exposure alters adenosine receptor control of locomotor activity in the developing rat. Dev Pharma- col Ther 1990; 15(2):94-100. DOI: https://doi. org/10.1159/000457627.
- Fisher S, Guillet R. Neonatal caffeine alters pas- sive avoidance retention in rats in an age- and gender-related manner. Brain Res Dev Brain Res 1997; 98(1):145-9. DOI: https://doi.org/10.1016/ S0165-3806(96)00158-7.
