Artículo de Revisión
Miocarditis en la infección viral del dengue en pediatría
Silvia Catalina Corrales 1, Doris Martha Cecilia Salgado 2
1 MD, Residente de Segundo año, Pediatría, Facultad de Salud, Universidad Surcolombiana. Neiva, Colombia. catalinasc.corrales@gmail.com
2 MD Pediatra, Departamento Infectologia Pediátrica, Facultad de Salud, Universidad Surcolombiana. Neiva, Colombia. dpanqueba@gmail.com
Archivos de Medicina (Manizales), Volumen 17 N° 1, Enero-Junio 2017, ISSN versión impresa 1657-320X, ISSN versión en línea 2339-3874. Corrales S.C.; Salgado D.M.C.
Recibido para publicación: 28-03-2017 - Versión corregida: 03-04-2017 - Aprobado para publicación: 01-05-2017
Resumen
Objetivo: realizar una revisión sistemática sobre la infección del virus del dengue (DENV), con compromiso cardiovascular, en la población pediátrica, con la finalidad de describir y establecer criterios útiles para el diagnóstico y manejo. Métodos: en una búsqueda en bases de datos, Embase, Medline, PubMed, The Cochrane Library y LILACS. Con límites y palabras claves que incluyeron ensayos clínicos aleatorizados y compromiso cardiovascular en la infección viral por DENV. Conclusiones: la infección por el DENV con compromiso miocárdico, en pediatría, es un gran desafío clínico, se presenta con múltiples manifestaciones, donde la sospecha clínica, la diferente evolución y curso de la enfermedad sumado al uso e interpretación de pruebas diagnósticas diferentes a la biopsia, pueden arrojar pistas o desviar la atención de la verdadera afectación de órgano observada. La fisiopatología del compromiso miocárdico más allá del choque en el paciente pediátrico, debe entenderse, con el fin de realizar su evaluación. La posibilidad de miocardiopatía dilatada debe tenerse en cuenta en DENV y choque refractario, asociado a signos y síntomas de insuficiencia cardíaca congestiva. La detección temprana, la reanimación inmediata, el ingreso en la unidad de cuidado intensivo, evitando la terapia agresiva con líquidos intravenosos, son medidas cruciales para salvar vidas y puede mejorar la supervivencia de los pacientes. Adecuados criterios de clasificación y diagnóstico definen el manejo esencial de soporte, evitando resultados fatales.
Palabras claves: biomarcadores, choque, dengue, miocarditis, ultrasonido.
Corrales SC, Salgado DMC. Miocarditis en la infección viral del dengue en pediatría. Arch Med (Manizales) 2017; 17(1):160-72.
Myocarditis in viral infection of dengue in pediatrics
Summary
Objective: to perform a systematic review on dengue virus infection (DENV), with cardiovascular involvement, in the pediatric population, in order to describe and establish useful criteria for diagnosis and management. Methods: in a database search, Embase, Medline, PubMed, The Cochrane Library and LILACS. With limits and keywords that included randomized clinical trials and cardiovascular involvement in viral infection by DENV. Conclusions: DENV infection with myocardial compromise in pediatrics is a great clinical challenge. It presents multiple manifestations, where clinical suspicion, the different evolution and course of the disease together with the use and interpretation of diagnostic tests different from Biopsy, may throw clues or divert attention from the actual organ involvement observed. The pathophysiology of myocardial compromise beyond shock in the pediatric patient should be understood in order to perform its evaluation. The possibility of dilated cardiomyopathy should be taken into account in DENV and refractory shock, associated with signs and symptoms of congestive heart failure. Early detection, immediate resuscitation, entry into the intensive care unit, and avoidance of aggressive intravenous fluid therapy are crucial life-saving measures and can improve patient survival. Adequate classification and diagnostic criteria define the essential management of support, avoiding fatal results.
Keywords: biomarkers, shock, dengue, myocarditis, ultrasonics.
Introducción
El dengue es actualmente una de las enfermedades infecciosas emergentes más importantes que existen, con compromiso cardiovascular altamente demostrado [1]. Ha evolucionado de una enfermedad esporádica, a un importante problema de salud pública con efecto social y económico sustancial, debido al aumento de la extensión geográfica, el gran número de casos asociado a mayor gravedad de la enfermedad [2]. Fenómenos globales como la urbanización y los viajes internacionales son factores claves que han facilitado la propagación de la enfermedad.
Desde el primer aislamiento del virus del denge (DENV) en 1943 se han reconocido cuatro diferentes serotipos, cada uno con patrones de propagación, hiperendemicidad y gravedad [3]. DENV se ha identificado como un virus del género Flavivirus perteneciente al tipo o familia Flaviviridae, tipo ARN con envoltura de cadena simple, con cuatro serotipos denominados DENV 1 al 4. Los cuatro tienen diferencias genéticas y comparten del 60 al 75% de aminoácidos. En el mismo serotipo tienen diferencias de cerca del 3% en aminoácidos y del 6% en nucleótidos. Filogenéticamente están divididos en genotipos y clados [4]. Estas variaciones genéticas entre serotipos y subtipos son importantes determinantes de los factores de virulencia, el potencial de replicación, la endemicidad y la capacidad de desarrollar la enfermedad. Ya que cada serotipo o clado se asocia con diferente gravedad, manifestaciones clínicas y desenlaces de la enfermedad [2]. Distintos estudios han examinado la propagación de estos a nivel regional y locales, determinando relaciones filogeográficas, demostrando la expansión hiperendemica de la enfermedad, cada vez más importante en la salud pública mundial. A pesar de la poca información geográfica y estadística en muchos lugares del mundo, tema que necesita ser abordado con urgencia [3].
Los pacientes que han sido infectados con un serotipo denominado DENV primario; a largo plazo desarrollan inmunidad protectora contra el mismo serotipo. Sin embargo, el mismo individuo puede ser infectado hasta cuatro veces por los serotipos de virus heterólogos al no existir inmunidad cruzada. Estos niños y adultos que experimentan una segunda infección por DENV tienen un riesgo mucho mayor de desarrollar formas graves de la enfermedad [5], evento denominado infección secundaria por un serotipo heterólogo, que se produce con frecuencia en zonas endémicas y es el factor de riesgo más importante para la enfermedad grave [6]. Durante la infección secundaria el desarrollo de DENV grave puede ser relativamente raro y sólo del 0,5% al 1% de los pacientes evolucionan hacia el choque [7].
La infección secundaria con otro serotipo del virus del dengue puede formar un complejo virus-anticuerpo con el anticuerpo existente por la infección anterior. Potenciando la respuesta inmune. No está clara la fisiopatología de cómo se producen la hemorragia y el choque en estos casos. Es probable que la respuesta inmune juegue un papel importante. Dado que la producción de complejos inmunes, promueve el crecimiento del virus en células mononucleares, activando el sistema del complemento. Los cambios genéticos en el virus aumentan la replicación, la virulencia y el potencial epidemiológico del virus, ocasionando mayor daño y aumento de la permeabilidad capilar [8]. Con mayor efectividad para producir infecciones por DENV, con signos de alarma y grave que son endémicos.
Epidemiologia
La enfermedad se encuentra distribuida en áreas de 2200 metros sobre el nivel del mar (msnm), en áreas tropicales y subtropicales, con circulación activa de los cuatro serotipos y el vector Aedes [9].
Antes de 1970, solo nueve países habían sufrido epidemias de dengue grave. Sin embargo, en la última década la enfermedad es endémica en más de 100 países de las regiones de África, las Américas, el Mediterráneo Oriental, Asia Sudoriental y el Pacífico Occidental [2,10]. En la década de los 90 se presentaba una incidencia anual cercana a los 40 millones de casos con 500 000 hospitalizaciones por dengue grave o choque. El 90% de los casos en menores de 15 años con 24 000 muertes anuales para una tasa promedio del 5% por ésta enfermedad.
En Colombia en el año 2010 la notificación alcanzo 1,6 millones de casos dentro de los cuales 50 235 fueron casos graves y 1 185 muertes, una disminución del 39% en la morbilidad y un 40% en la mortalidad fue alcanzada en el 2011. El 76,1% de los casos son reportados en Departamentos del territorio nacional como Antioquia, Cesar, Cundinamarca, Huila, Meta, Putumayo, Norte de Santander, Santander, Tolima y Valle [9]. En la semana epidemiológica 22 del 2015, se registraron 159 muertes probables por dengue, con una muerte en el Huila [11]. En los últimos 10 años se notificaron cerca de 29 muertes anuales. El 77,5% de los casos, son de habitantes de entidades territoriales comunes a los Departamentos reportados. El 60% de los casos de dengue grave está concentrado en Tolima, Meta, Valle del Cauca, Santander, Huila, Antioquia y Norte de Santander [12].
La enfermedad se debe sospechar en cualquier paciente que viva en países donde la infección es endémica y en los que viajaban a dichas áreas dentro de las últimas dos semanas. El inicio de los síntomas después del período de incubación suele ser brusco. La fiebre es característica de la infección y es a menudo de inicio abrupto con picos altos de 39,4 a 40,5 °C. También puede ser bifásica con un patrón remitente o ser de baja intensidad, por lo general tiene una duración de cinco a siete días.
En los niños pequeños la fiebre puede causar convulsiones febriles o delirio [13]. Los dolores y molestias, sobre todo en la espalda, artralgias y mialgias, son comunes. La cefalea también es típica, generalmente es constante de predominio frontal. Suele mejorar a los pocos días. El dolor retro-orbital severo con el movimiento ocular o con un poco de presión aplicada al globo ocular también es usual. Algunos síntomas gastrointestinales como anorexia, náuseas, vómitos, epigastralgia, también hacen parte del cuadro, síntomas neurológicos como letargo o inquietud, colapso, o mareos también pueden estar presentes. Los síntomas gastrointestinales, debilidad y mareos pueden ser más evidentes cuando existe mayor compromiso del paciente [13], con la presencia o no de signos de alarma, ampliamente descritos y demostrados con datos epidemiológicamente significativos, estableciéndolos como norma protocolizada en el que clasifican la enfermedad, como lo muestra la Tabla 1 [14].
Tabla 1. Signos de alarma de dengue asociado a gravedad en niños [14]
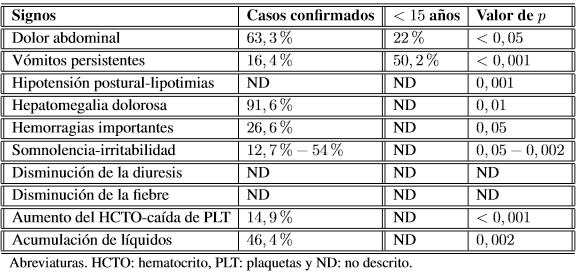
Fuente: Tang KF, Ooi EE. Diagnosis of dengue: an update. Expert Rev Anti Infect Ther 2012; 10: 895–907.
Previa a la clasificación del 2009, el DENV se reportaba como fiebre del dengue (DF) y la fiebre hemorrágica del dengue (FHD) y síndrome de choque (DSS) clasificándolo en grados del I al IV. Sin embargo, como el dengue se extendió por todo el mundo de manera apresurada, esta clasificación no era de aplicación universal, pues no permitía la designación directa de opciones terapéuticas [15], fin principal para designar un tipo de clasificación a una patología en curso en nuestro paciente. La gravedad de la infección y el plan de tratamiento más usado en la práctica médica, se hace con la clasificación revisada de la Organización Mundial de la Salud (OMS) en tres grupos (Tabla 2), dependiendo de la presentación clínica y se basa en la gravedad de infección [16].
Para diferenciar la severidad del DENV, sus manifestaciones más graves como el síndrome de choque dengue, la revisión de la OMS permite, que los pacientes se clasifiquen actualmente en DENV con o sin signos de alarma o en DENV grave [16]. Siendo esta clasificación más acertada, pues permite la intervención del clínico, con la identificación temprana y optima de casos graves.
La enfermedad no grave incluye el DENV con o sin signos de alarma. A menudo tiene un comportamiento asintomático, pero puede convertirse en una amplia gama de manifestaciones clínicas, desde fiebre leve o fuga plasmática, hasta el síndrome de choque, cuadro potencialmente fatal.
Tabla 2. Guía de manejo según la gravedad de la infección [16].
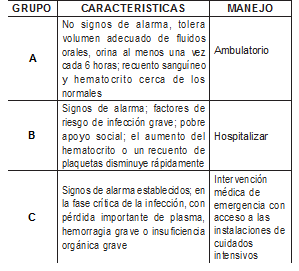
El riesgo de enfermedad grave varía según la edad. La edad parece influir en el fenotipo clínico de la enfermedad, pues el choque ocurre con más frecuencia en los niños, la presencia de hemorragias y deterioro de órganos es más común en adultos [1]. En los lactantes estas manifestaciones tienen una mayor frecuencia, principalmente los dados por fuga plasmática y choque, en comparación con el cuadro clínico de niños mayores [17].
Aunque la gran mayoría de eventos son asintomáticos o leves, del 1 al 5% de los pacientes pueden desarrollar complicaciones, con mayor prevalencia en segundos episodios, con mayor respuesta inmune, generando falla multiorgánica, sangrados y fuga capilar masiva. En los casos graves, la fuga plasmática puede hacer colapsar el sistema cardiovascular desencadenando consecuencias potencialmente fatales, y DSS [1].
En la población pediátrica se debe optimizar el manejo durante el curso clínico de la enfermedad. Varios estudios han demostrado un mayor riesgo de fuga vascular y desarrollo de DSS en los niños en comparación con los adultos, [18,19,20], probablemente relacionado con la mayor permeabilidad intrínseca de los pacientes más jóvenes, por lo tanto una mayor gravedad se suma a menor capacidad de compensación, con presentación de otros marcadores de gravedad de la fuga, como un mayor aumento del hematocrito y del compromiso hemodinámico severo en la presentación. Con valores de las AST como factores de riesgo para el desarrollo de gravedad. El sexo femenino se ha identificado como un predictor dependiente de mortalidad en niños con DSS, posiblemente reflejando una mayor permeabilidad intrínseca vascular, y por lo tanto una mayor susceptibilidad al síndrome de fuga capilar, en las mujeres que en los hombres. Existe asociación bien establecida entre la fuga vascular y trombocitopenia, aunque es probable que la trombocitopenia ya presente en el inicio del choque enmascare otras manifestaciones graves [18].
Etapas clínicas de la enfermedad
La OMS reconoce tres fases del curso clínico de la infección, primero la febril, posteriormente la fase crítica y por ultimo una fase de recuperación. Tres fases con distintas manifestaciones reconocibles.
La fase febril va de los primeros 3 a 4 días, durante los cuales el paciente normalmente experimenta fiebre alta de forma súbita, cefalea con o sin dolor retrocular, mialgias, artralgias, emesis, malestar general y erupción maculopapular o petequial. Aunque los niños por lo general sufren de fiebre alta, son generalmente menos sintomáticos que los adultos durante esta fase, con manifestaciones hemorrágicas menores como petequias o sangrado de mucosas. Posteriormente de esta etapa la mayoría de pacientes se recuperan sin complicaciones adicionales. Una menor proporción de pacientes desarrollan un síndrome de fuga vascular sistémico, que se hace evidente en el momento de la desaparición de la fiebre o defervescencia. Periodo denominado como fase crítica, con una duración de 2 a 3 días, cerca de la desaparición de la fiebre, durante la cual se pueden evidenciar manifestaciones clínicas severas. Se caracteriza por leucopenia progresiva asociado a disminución en el recuento de plaquetas, manifestaciones hemorrágicas, derrames pleurales, ascitis e hipoproteinemia.
El choque ocurre cuando existe una pérdida de volumen de manera crítica, por fuga de plasma masiva, evento frecuente y más grave en niños que en adultos. Los sangrados son clínicamente significativos en la fase crítica y en los niños se producen en asociación sólo con choque profundo y prolongado. Esta alteración de la permeabilidad vascular se resuelve espontáneamente después de 48 a 72 horas en la fase de recuperación [15], en los últimos 2 a 5 días de enfermedad la mejoría clínica se asocia a la reabsorción del líquido extravascular [1], a la recuperación del estado hemodinámico y diuresis.
Durante el curso de cada fase, el hematocrito comienza siendo normal y va ascendiendo al mismo tiempo que los estudios radiológicos de tórax muestran derrame pleural derecho o bilateral y la ultrasonografía abdominal evidencia ascitis, coincidiendo la máxima elevación del hematocrito con la fuga y el choque. El recuento plaquetario muestra un descenso progresivo hasta llegar a las cifras más bajas durante el día del choque para después ascender rápidamente y normalizarse en pocos días.
El choque se presenta en una frecuencia de 4 o 5 veces mayor en el momento de la caída de la fiebre o en las primeras 24 horas de la desaparición de ésta que durante la etapa febril, y cuando se desarrolla se manifiesta por fuga capilar severa como una patología prolongada o recurrente, donde la mayoría de pacientes fallecen por causa directa o secundaria a complicaciones tales como hemorragias masivas, coagulación intravascular diseminada, edema pulmonar no cardiogénico, fallo múltiple de órganos, como signos del síndrome de hipoperfusión y reperfusión [14], lo que caracteriza los casos de DENV grave.
Además del choque existen formas clínicas con compromiso intenso de un órgano o sistema como la encefalopatía, miocardiopatía, hepatopatía, compromiso renal con insuficiencia renal aguda, pancreatitis, coagulación intravascular diseminada que se asocian a mayor mortalidad, siendo las manifestaciones más frecuentes hepáticas y neurológicas en la población pediátrica, especialmente en edad escolar que en menor proporción presentan complicaciones renales, cardíacas, pulmonares, síndrome hemofagocítico, pancreatitis y abdomen agudo [9]. Estos pacientes necesitan un mayor volumen de líquidos desde las primeras etapas de la enfermedad; en el tercer día de fiebre con aumento en el requerimiento del quinto al séptimo día en comparación con el grupo que no desarrolla manifestaciones graves [21].
A pesar de esta directriz, no hay manera de predecir el curso natural de la enfermedad terminando los primeros dos días de fiebre, al iniciar la pérdida de plasma puede progresar a choque, que de ser prolongado puede conducir a hipoperfusión de órganos con disfunción progresiva de ellos, acidosis metabólica y coagulación intravascular diseminada con sangrados graves [22].
Manifestaciones cardiovasculares del dengue
La principal característica distintiva del DSS es una la mayor permeabilidad vascular producida, que conduce a pérdida plasmática en el nivel microvascular de las cavidades pleurales y abdominales.
Debido a las dificultades para estudiar la progresión de la enfermedad en los pacientes y la falta de un modelo fiable, la mayoría en datos in vivo se derivan de muestras de sangre y autopsias post-mortem. Por lo tanto, el grado en que la célula endotelial desarrolla el choque sigue siendo debatible [23]. El aumento de la permeabilidad capilar que se produce en algunos pacientes, puede causar hipovolemia y choque [1]. Generando compromiso del sistema cardiovascular. Asociado a esto, diversas manifestaciones cardiacas se han descrito.
La función miocárdica, de forma regional, en DENV grave no se ha informado de forma exhaustiva para evaluar las propiedades de deformación del ventrículo izquierdo. El paciente con DENV tiene parámetros de deformación significativamente más bajos en las fibras miocárdicas longitudinales, dichas fibras han demostrado ser particularmente vulnerables a la isquemia, lo que lleva a una disminución dominante en la fracción de acortamiento. Además, una reducción significativa de la tensión circunferencial es evidente sólo en la región subepicárdica en diferentes fases de la enfermedad. Este fenómeno puede ser útil para explicar el mecanismo de compensación producida por fibras circunferenciales y radiales para mantener la función sistólica del ventrículo izquierdo [24]. En miocarditis se describe una alteración difusa de la tensión longitudinal y una reducción irregular en la tensión circunferencial epicárdica [25]. De forma escasa se presentan miocarditis fulminante, son más comunes, las relacionadas con el deterioro funcional miocárdico, con manifestaciones clínicas dadas por infarto o arritmias. La miocarditis ha sido incluida en la definición de dengue grave adoptada en el 2009 por la OMS. Su verdadera incidencia sigue siendo desconocida debido a la falta de la detección [1].
La miocarditis por DENV, resulta de la infección por un virus cardiotrópico seguido por la destrucción inflamatoria del miocardio. Que también puede extenderse al pericardio y endocardio. Es posible que la actividad inflamatoria secundaria tenga un papel fundamental en la fisiopatología de la enfermedad cardíaca, y la lesión miocárdica se presente como un evento mediado por la respuesta inmune con depresión de la función miocárdica informada en las formas graves del DENV [26], demostrando infección directa en las células musculares con evidencia de que el DENV infecta y altera el almacenamiento de calcio en las células del músculo esquelético in vitro, apoyando la hipótesis que la disfunción del músculo cardíaco y esquelético está asociada directamente al DENV [27]. La infección directa del virus en las fibras cardíacas puede ser responsable al menos en parte de la disfunción. Además del efecto citotóxico directo del virus en las fibras cardíacas, la exacerbación de la respuesta inmune del huésped conduce a una mayor expresión de citoquinas que pueden contribuir a los daños tisulares observados. Las lesiones también parecen implicar apoptosis con la presencia de núcleos picnóticos en los miocitos y la pérdida de la integridad mitocondrial [28]. En la literatura las autopsias de 5 pacientes que murieron a causa de complicaciones por DENV, mostraron evidencia histopatológica de miocarditis dados por edema intersticial, infiltración de células inflamatorias, necrosis e infarto de fibras miocárdicas, con un caso asociado a pericarditis [29]. Una intensa infección de células mononucleares es observada en inmunohistoquímica (IHC) [26], lo que confirma la liberación de mediadores inflamatorios como principal mecanismo de daño miocárdico en la infección por DENV [30], asociado a la acción directa del virus en la célula cardíaca [31].
Serotipos como el DENV 1 se describen como infectante en miotúbulos sin destrucción de la célula miocárdica, sin correlaciones específicas de otros serotipos [27]. Como entidad, la caracterización de la miocarditis tiene presentaciones clínicas y etiologías diversas [32]. La miocarditis y la consecuente miocardiopatía que pudiera ocurrir, es causada por agentes infecciosos y no infecciosos e incluso medicamentos cardiotóxicos. Como hallazgos clínicos se encuentran ciertos grados de disfunción cardiaca, desde leves efectos subclínicos como arritmias, insuficiencia cardiaca, shock cardiogénico, y muerte súbita. Con base en el compromiso cardiaco, la miocarditis, se puede clasificar en tres categorías clínicas, aguda, fulminante y crónica. Los casos subclínicos más leves pueden tener resolución espontánea y pasar desapercibidos. Caso contrario en la enfermedad fulminante, que produce en los pacientes, choque cardiogénico. Los casos crónicos pueden progresar a miocardiopatía dilatada [33].
En las últimas cuatro décadas, la infección viral cada vez ha sido reconocido como la etiología más común, con el uso de la reacción en cadena de la polimerasa y técnicas de hibridación in situ el ARN y el ADN viral se ha identificado en el miocardio de pacientes afectados [32]. La depresión de la función miocárdica se ha informado asociada al DENV en las formas graves. Al demostrar la infección directa en las células musculares. Existe evidencia de que el DENV infecta y altera el almacenamiento de calcio en las células del músculo esquelético in vitro. Respaldando algunas hipótesis de la disfunción del músculo cardíaco y esquelético asociada directamente al DENV. El daño miocárdico leve o severo, clínicamente se manifiesta de formas diversas como bradicardia, taquicardia, derrame pericárdico o disfunción diastólica. Otros hallazgos reportados son los trastornos de la conducción auriculoventricular, arritmias supraventriculares, miocarditis, fracciones de eyección (FEVI) de menos del 50%, hipocinesia ventricular difusa [27]. Aunque hay algunos informes de miocarditis como complicación, la correlación directa ha sido poco investigada. Otras manifestaciones clínicas cardiovasculares, varían desde una leve elevación de biomarcadores, sin alteración estructural, hasta la miocarditis o pericarditis, complicaciones que pueden ser subdiagnosticadas y contribuyen a la mortalidad de la infección por DENV [26].
La identificación del tropismo tisular de DENV, por medio de IHC e hibridación in situ se realiza sobre muestras de tejido y sangre de pacientes con infección confirmada serológicamente o virológicamente [23]. El antígeno viral es detectado en el hígado, en la célula de Kupffer y endotelial sinusoidal, en macrófagos y células linfoides en el bazo, en macrófagos y endotelio vascular en el pulmón, en los túbulos renales, monocitos y linfocitos [34]. En un estudio realizado en los tejidos de niños que murieron por la infección, no se detectaron antígenos DENV en las células endoteliales [35]. Por el contrario, las muestras de tejido de cuatro casos fatales en Brasil, mostraron replicación DENV-3 en las células mencionadas además en los hepatocitos, neumocitos tipo II, fibras cardiacas, y células endoteliales [23]. En el corazón se evidencian áreas focales con infiltrados de células mononucleares. Y se observa algún grado de degeneración de las fibras cardíacas, con ausencia de su núcleo y la pérdida de estrías, como resultado de un edema intersticial, que sugiere miocarditis. Estos hallazgos sugieren que la infección directa del virus en las fibras cardiacas puede ser responsable, al menos en parte, de la disfunción. Sin embargo, además del efecto citotóxico directo del virus en las fibras cardiacas, la exacerbación de la respuesta inmune del huésped, conduce a una mayor expresión de citoquinas, que pueden contribuir a los daños tisulares observados. Las lesiones también parecen implicar apoptosis, con la presencia de núcleos picnóticos en los miocitos y la pérdida de la integridad mitocondrial [28].
La elevación de biomarcadores, es significativa en los pacientes con DENV, especialmente los marcadores de daño miocárdico que están presentes en cerca del 25% de los pacientes, ejemplo de ellos son la mioglobina, creatinin quinasa fracción MB (CK-MB), y troponina T. Otros con menor especificidad que también se pueden elevar son el fragmento N terminal del péptido natriurético tipo B (NT-proBNP), los ácidos grasos de unión a proteínas de tipo cardíaco (h-FABP). Predominando la elevación de mioglobina o CK-MB, sin ser biomarcadores específicos de la lesión miocárdica. En otros estudios se observó elevación de la troponina I en el 7% y del NT-proBNP en el 10%, de los pacientes. En los pacientes con biomarcadores elevados se demostró mayor actividad inflamatoria, mayor conteo leucocitario y niveles de proteína C reactiva (PCR).
A pesar de la actividad inflamatoria, la carga viral fue más baja, lo que sugiere que no hay asociación entre la carga viral y la lesión cardiaca. Es posible que la actividad inflamatoria secundaria tenga un papel fundamental en la fisiopatología de la enfermedad cardíaca y la lesión miocárdica como evento mediado por la respuesta inmune. Otras manifestaciones cardiovasculares de la enfermedad descritas en pocos informes, es la insuficiencia cardíaca aguda [26].
En la evaluación, de una serie de 17 pacientes, se encontró, una FEVI <40% e hipocinesia global, en 7 y 12 casos, respectivamente. Con seguimiento ecocardiográfico tres semanas después, se observó que todas las alteraciones se resolvieron [36]. En nuestro medio, un estudio de 102 niños diagnosticados con DENV hemorrágico, 10 pacientes presentaron miocarditis aguda, requiriendo el uso de fármacos inotrópicos para mejorar a la insuficiencia cardíaca aguda [37].
Otros reportes incluyen el desarrollo de síntomas concordantes con insuficiencia cardíaca aguda, en 4 pacientes de una serie de 81, con disminución de la FEVI y alteración del movimiento de la pared miocárdica en 3 pacientes. Con desarrollo de choque en 3 pacientes y muerte en 2 pacientes. En estos últimos se descartó una importante pérdida de plasma asociada a sangrado o hemoconcentración, con niveles de hemoglobina y de hematocrito normal. Considerando la etiología del choque, a la afectación cardíaca, con choque cardiogénico secundario [26]. En la literatura, autopsias de 5 pacientes, que murieron a causa de complicaciones por DENV, mostraron evidencia histopatológica de miocarditis, dados por edema intersticial, infiltración de células inflamatorias, necrosis e infarto de fibras miocárdicas, con un caso asociado a pericarditis [29]. Una intensa infección de células mononucleares es observada en IHC, lo que confirmaría como principal mecanismo de daño miocárdico, en la infección por DENV, la liberación de mediadores inflamatorios [30] y no sólo la acción directa del virus en la célula cardiaca [31]. Serotipos como el DENV 1 se describen como infectante en miotúbulos sin destrucción de la célula miocárdica [27].
El tratamiento de la miocarditis sigue siendo en gran medida de apoyo sintomático. El manejo inmunosupresor puede ser favorable en pacientes con miocarditis de células gigantes y sarcoidosis. El uso de la terapia inmunomoduladora y antiviral permanece en gran parte en investigación en este momento. Se necesitan ensayos grandes, aleatorizados controlados para determinar su papel en el tratamiento de la cardiopatía inflamatoria [32]. Además, no hay ni vacuna ni tratamiento antiviral eficaz disponible para el dengue [38].
Conclusiones
Los factores responsables del resurgimiento del DENV en los últimos cincuenta años como un problema de salud pública son complejos y se encuentran estrechamente asociados a cambios socio-demográficos, al aumento de la población de mosquitos en áreas urbanas tropicales y la ausencia de un control efectivo del mosquito en donde el DENV es endémico [39].
Para el manejo de la enfermedad, el clínico debe clasificar de forma correcta a cada paciente tanto en la etapa en curso como el grado de compromiso, para diferenciar las manifestaciones leves del choque, que conlleva a desenlaces fatales. La característica patognomónica de la vasculopatía asociada al DENV grave es el incremento de la permeabilidad vascular que provoca un síndrome de fuga capilar transitoria. La descompensación cardiovascular se produce cuando las pérdidas de plasma exceden la capacidad de regulación [18]. Y no son suficientes los mecanismos de compensación normales que mantienen el volumen plasmático dentro del límite del sistema vascular [40]. Varios estudios han demostrado un mayor riesgo de fuga vascular y desarrollo de choque en los niños en comparación con los adultos [20,41], con una probable relación entre una mayor permeabilidad vascular, con una menor edad y gravedad del choque [42].
En la literatura, la frecuencia del curso del choque también disminuye al aumentar la edad. Con excepción de la hipotensión, todos los signos y síntomas asociados al choque, son significativos en la presentación de la enfermedad en lactantes, que en los niños mayores o adultos [19]. En lugar de la hipotensión establecida, la presión del pulso estrecha, que precede a la hipotensión en los niños, es por lo tanto una de las primeras manifestaciones del choque [43], predominado como el signo principal en los lactantes. Otro signo, es el llenado capilar lento, documentado hasta en dos tercios de los pacientes con choque [19]. La hipotensión y disminución de la función cardíaca, pueden relacionarse durante el curso de la enfermedad, y podrían ser atribuibles a fuga capilar con la consecuente reducción del volumen intravascular, que conduce a la inestabilidad hemodinámica en estos pacientes [1]. La hipotensión persistente, con la característica de no responder a los líquidos de reanimación y el requerimiento de soporte inotrópico para mantener una presión arterial adecuada, debe hacer sospecha diagnostica de compromiso cardiaco.
La instauración de compromiso cardiaco se describe en la literatura con datos desde el 9 al 80% de casos reportados, de los cuales se han informado resultados fatales, con requerimientos de ventilación mecánica, medicamentos vasoactivos y soporte inotrópico, en el curso de choque cardiogénico [44]. La variedad estadística y clínica de este compromiso, explica que la respuesta inmune a la infección viral y la cascada de mediadores inflamatorios resultantes, como factor de necrosis tumoral y quimiocinas, juegan un papel clave en el daño miocárdico [45]. Investigación vitro ha demostrado que el virus altera las señales de calcio intracelular, en el miocardio, lo que conlleva a la apertura de poros de la membrana mitocondrial y la activación de la vía intrínseca apoptótica [46].
Las manifestaciones de DENV, que afectan el miocardio, se han informado, aunque como raras complicaciones [45]. Dado que la clínica varía, existen pacientes completamente asintomáticos, otros con sintomatología muy leve, o algunos pueden sufrir daño miocárdico severo, con disfunción ventricular, hipocinesia global y choque cardiogénico [31]. Este compromiso variable, probablemente es debido al hecho de que se trata de una enfermedad, cuyo espectro puede ir desde fiebre, manifestaciones atípicas o hemorrágicas, hasta el choque [44]. Los niños requieren volúmenes de líquidos endovenosos muy específicos para la reanimación, ya que son propensos a diferentes procesos superpuestos como estados de sobrecarga de volumen, edema pulmonar o infecciones [36]. En estas circunstancias es necesario aumentar el índice de sospecha de casos con miocarditis como una causa primaria, lo que permite cambiar su enfoque en lugar de buscar la fluidoterapia vigorosa, que podría ser perjudicial para el niño [31].
El efecto de la miocarditis no sólo se limita al funcionamiento mecánico del corazón, también implica su conducción eléctrica [44]. Esta inflamación miocárdica predispone arritmias, por medio de tres mecanismos. Primero, los procesos inflamatorios de los miocitos y el intersticio, pueden conducir a alteraciones en el potencial de membrana. En segundo lugar, cambios en los parámetros de la dinámica ventriculares, mayor tensión de la pared y el consumo de oxígeno del miocardio también aumentan el potencial de arritmias. Finalmente, la fibrosis y atrofia secundaria de la célula miocárdica, pueden favorecer el desarrollo de marcapasos ectópico. Es probable que los dos primeros mecanismos jueguen un papel predominante en arritmias asociadas a la miocarditis del DENV, como un trastorno agudo y reversible [47].
La miocarditis como enfermedad inflamatoria del miocardio, por esta amplia presentación clínica y las dificultades en el diagnóstico, produce un subregistro en la incidencia. Los signos clínicos de miocarditis pueden variar desde un cuadro asintomático con hallazgos en biomarcadores o cambios en el electrocardiograma (ECG), a una clínica más severa con signos y síntomas claros como disnea repentina y dolor precordial [1]. En la atención del paciente la clasificación clínica para el manejo de DENV, la miocarditis hace parte del grupo de DENV grave, con daño en órgano, en este caso del corazón. Lo que amplía el abordaje en el seguimiento de los signos de choque, y califica al paciente como categoría C, y requieren tratamiento urgente y remisión a una unidad de cuidados intensivos.
Se hace prioridad el seguimiento estricto y monitoreo de los signos de alarma, balance hídrico hasta que se supere la fase crítica de la enfermedad [14]. Periodo en el cual se presentan los desenlaces fatales. La miocarditis ha sido descrita, utilizando diversos criterios diagnósticos. En la población pediátrica es indispensable la clasificación inicial, ya que el paso de las horas de enfermedad, implica una reacción dinámica del personal de salud. Sin embargo, muy pocos pacientes con dengue tienen una evaluación cardiaca de rutina, por lo que la frecuencia de miocarditis subclínica y su relación con la inestabilidad hemodinámica, en DENV grave, queda sin ser demostrada. La disfunción miocárdica en el DENV ha sido documentada en varios estudios utilizando diferentes técnicas. Dicha disfunción puede comportarse como un cuadro transitorio, pero en algunos casos, se desarrolla miocarditis fulminante fatal. En la mayoría de los pacientes la función miocárdica se encuentra conservada, normal o recuperada al final de la fase crítica. En la literatura no hay estudios a largo plazo que respalde alguna evidencia de progresión a miocardiopatía dilatada.
Epidemias descritas, con una alta incidencia de manifestaciones cardiacas, han planteado la existencia de un cardiotropismo de determinados serotipos o genotipos de DENV, que en las últimas décadas ha aumentado. Los serotipos 1 y 3 han sido identificados, el 4 no tiene aún reportes [1]. Diversas alteraciones del ritmo cardiaco se han observado en niños y adultos, con infección por el DENV. Estos incluyen bradicardia sinusal, bloqueo cardíaco de primer grado, del tipo Mobitz I, bloqueo cardíaco de segundo grado (Wenckebach), extrasístoles ventriculares y fibrilación auricular [48].
Se requieren estudios para mejorar la capacidad de predecir qué pacientes son propensos a desarrollar clínicamente una fuga capilar masiva, e investigar nuevas técnicas para monitorizar el volumen intravascular, que demuestren la infección viral directa de los miocitos, o la lesión inmunomediada, desencadenando la afectación cardíaca. Los estudios paraclínicos deben realizarse para aumentar la sensibilidad y especificidad diagnóstica en miocarditis [1]. Se deben sumar estudios, pues el diagnostico conclusivo de miocarditis sigue siendo histopatológico siguiendo los criterios descritos como Dallas, que definen la miocarditis aguda, como la presencia de infiltrados linfocitarios en asociación a necrosis de los miocitos. La miocarditis borderline, se caracteriza por infiltrados inflamatorios sin evidencia de necrosis de miocitos. Los criterios de Dallas están limitados por la alta variabilidad del observador y la interpretación de las muestras de biopsia, en especial con la miocarditis borderline, debido a procesos inflamatorios que no pueden ser detectados sin IHC, que está ganando mayor aceptación en el diagnóstico de la miocarditis [49].
Dado que DENV es capaz de involucrar a múltiples sistemas y órganos simultáneamente o de forma aislada. Manifestaciones atípicas como la miocarditis y arritmias cardíacas suelen ser leves o incluso asintomática, con graves consecuencias en el paciente [44]. Algunas manifestaciones cardíacas de DENV descritas como atípicas, son la miocarditis, taquicardia paroxística supraventricular, bradicardia sinusal, derrame pericárdico y latidos ventriculares ectópicos. La mayoría de los pacientes tienen una resolución espontánea con tratamiento sintomático de soporte. La asociación entre las alteraciones del ritmo cardiaco y el DENV, se han atribuido a miocarditis [50]. La posibilidad de miocardiopatía dilatada inducida por DENV debe siempre tenerse en cuenta si un paciente tiene DENV y choque refractario, asociado a signos y síntomas de insuficiencia cardíaca congestiva. Se debe enfatizar de nuevo en que la detección temprana, la reanimación inmediata, la clasificación del paciente, evitando la sobrecarga con líquidos intravenosos, son medidas cruciales para salvar vidas y puede mejorar la supervivencia de los pacientes [51]. Debe generarse conciencia, sospecha y atención de apoyo en la consecución de resultados positivos y benignos en estos pacientes [44].
Conflictos de interés: los autores declaran no tener ningún conflicto de intereses.
Fuentes de financiación: esta investigación no fue financiada por ninguna entidad.
Literatura citada
.
- Yacoub S, Wertheim H, Simmons CP, Screaton G, Wills B. Cardiovascular manifestations of the emerging dengue pandemic. Nat Rev Cardiol 2014; 11:335–45.
- Guzman MG, Harris E. Dengue. Lancet 2015; 385:453–65.
- Messina JP, Brady OJ, Scott TW, Zou C, Pigott DM, Duda KA, et al. Global spread of dengue virus types : mapping the 70 year history. Trends Mi- crobiol 2014; 22:138–46.
- Kuhn RJ, Zhang W, Rossmann MG, Pletnev SV, Corver J, Lenches E, et al. Structure of dengue virus: Implications for flavivirus organization, maturation, and fusion. Cell 2002; 108:717–25.
- Martina BEE, Koraka P, Osterhaus ADME. Dengue virus pathogenesis: An integrated view. Clin Mi- crobiol Rev 2009; 22:564–81.
- Halstead SB. Dengue. Lancet 2007; 370:1644–52.
- Diamond MS, Pierson TC. Molecular Insight into Dengue Virus Pathogenesis and Its Implications for Disease Control. Cell 2015; 162:488–92.
- Panpanich R, Sornchai P, Kanjanaratanakorn K. Cor- ticosteroids for treating dengue shock syndrome. Cochrane Database Syst Rev 2006; 3:CD003488.
- Zambrano P, Mercado M. Protocolo de Vigilancia en Salud Pública: Dengue. Bogota: Instituto Nacio- nal de Salud; 2014.
- Searo W. Comprehensive guidelines for preven- tion and control of dengue and dengue haemorr- hagic fever, Revised and expanded edition. New Delhi: World Health Organization; 2011.
- Blandón AM, Alarcón A. Boletin epidemiologico semanal. Semana epidemiològica nùmero 21. Bogota: Instituto Nacional de Salud; 2015.
- Maldonado JE, Maldonado ML, Mendez P, Villa MP. Curso Virtual en Enfermedades Transmitidas por Vectores. Bogota: Ministerio de Salud; 2015.
- Kularatne, SA. Dengue fever. Bmj 2015; 351:1–10.
- Rojas DP, Guía Para La Atención Clínica Integral Del Paciente Con Dengue. Bogota: Instituto Nacio- nal de Salud; 2012.
- Verhagen LM, De Groot R. Dengue in children. J Infect 2014; 69:S77–86.
- World Health Organization. Dengue: guidelines for diagnosis, treatment, prevention and control. Geneva: World Health Organization; 2009.
- World Health Organization. Dengue haemorrhagic fever. Diagnosis, treatment, prevention and con- trol. Geneva: Ed 2; 1997.
- Lam PK, Tam DT, Dung NM, Tien NT, Kieu NT, Simmons C, et al. A Prognostic Model for De- velopment of Profound Shock among Children Presenting with Dengue Shock Syndrome. PloS one 2015; 10:e0126134.
- Hammond SN, Balmaseda A, Pérez L, Tellez Y, Sa- borío SI, Mercado JC, et al. Differences in dengue severity in infants, children, and adults in a 3-year hospital-based study in Nicaragua. Am J Trop Med Hyg 2005; 73:1063–70.
- Anders KL, Nguyet NM, Van-Vinh-Chau N, Hung NT, Thuy TT, Lien LB, et al. Epidemiological Factors Associated with Dengue Shock Syndrome and Mortality in Hospitalized Dengue Patients in Ho Chi Minh City, Vietnam. Am J Trop Med Hyg 2011; 84:127–34.
- Kularatne SA, Weerakoon KG, Munasinghe R, Ralap- anawa UK, Pathirage M. Trends of fluid require- ment in dengue fever and dengue haemorrhagic fever: a single centre experience in Sri Lanka. BMC 2015; 8:130.
- Dalrymple N, Mackow ER. Endothelial Cells Elicit Immune-Enhancing Responses to Dengue Virus Infection. J Virol 2012; 86:6408–15.
- Wen YM, Wang YX. Biological features of hepatitis B virus isolates from patients based on full-length genomic analysis. Rev Med Virol 2009; 19:57–64.
- Sengupta SP, Nugurwar A, Jaju R, Khandheria BK. Left ventricular myocardial performance in pa- tients with dengue hemorrhagic fever and throm- bocytopenia as assessed by two-dimensional speckle tracking echocardiography. Indian Heart J 2013; 65:276–82.
- Bella GD, Gaeta M, Pingitore A, Oreto G, Zito C, Minutoli F, et al. Myocardial Deformation in Acute Myocarditis With Normal Left Ventricular Wall Motion. Circ J 2010; 74:1205–13.
- Miranda CH, Borges MDC, Matsuno AK, Vilar FC, Gali LG, Volpe GJ, et al. Evaluation of Cardiac Involvement During Dengue Viral Infection. Clin Infect Dis 2013; 57:812–9.
- Salgado DM, Eltit JM, Mansfield K, Pamqueba C, Castro D, Vega MR, et al. Heart and skeletal Mus- cle are targets of dengue virus infection. Pediatr Infect J 2010; 29:238–42.
- Póvoa TF, Alves AMB, Oliveira CAB, Nuovo GJ, Chagas VLA, Paes MV. The Pathology of Severe Dengue in Multiple Organs of Human Fatal Cases: Histopathology, Ultrastructure and Virus Replica- tion. PLoS One 2014; 9:e83386.
- Weerakoon KGAD, Kularatne SAM, Edussuriya DH, Kodikara SKA , Gunatilake LPG, Pinto VG, et al. His- topathological diagnosis of myocarditis in a dengue outbreak in Sri Lanka. BMC Res Notes 2009; 4:1–6.
- Cooper, Leslie T J. Myocarditis. Medical Progress.N Engl J Med 2009; 360:1526–38.
- Miranda CH, Borges MDC, Pazin-filho A, Rossi MA. A case presentation of a fatal dengue myocardi- tis showing evidence for dengue virus-induced lesion. Eur Heart J 2013; 2:127–30.
- Pollack A, Kontorovich AR, Fuster V, Dec GW. Viral myo- carditis—diagnosis, treatment options, and current controversies. Nat Rev Cardiol 2015; 12:670-680.
- Durani Y, Giordano K, Goudie BW. Myocarditis and pericarditis in children. Pediatr Clin North Am 2010; 57:1281–303.
- Jessie K, Fong MY, Devi S, Lam SK, Wong KT. Lo- calization of dengue virus in naturally infected human tissues, by immunohistochemistry and in situ hybridization. J Infect Dis 2004; 189:1411–8.
- Aye KS, Charngkaew K, Win N, Wai KZ, Moe K, Punyadee N, et al. Pathologic highlights of den- gue hemorrhagic fever in 13 autopsy cases from Myanmar. Hum Pathol 2014; 45:1221–33.
- Wali JP, Biswas A, Chandra S, Malhotra A, Aggarwal P, Handa R, et al. Cardiac involvement in Dengue Haemorrhagic Fever. Int J Cardiol 1998; 64:31–6.
- Salgado DM, Panqueba CA, Castro D, Vega MR. Miocarditis en Niños con Fiebre por Dengue Hemorrágico en un Hospital Universitario de Colombia. Rev salud pùblica 2009; 11:591–600.
- Noble CG, Chen YL, Dong H, Gu F, Lim SP, Schul W, et al. Strategies for development of dengue virus inhibitors. Antiviral Res 2010; 85:450–62.
- Reyes SZ, Zambrano LI, Sierra M. Caracterización clínica y hematológica de pacientes pediátricos con Dengue en Honduras. Rev Med Risaralda 2014; 20:95–100.
- Trung DT, Wills B. Systemic Vascular Leakage Associated with Dengue Infections – The Clinical Perspective. Dengue Virus 2010; 57-66.
- Guzman MG, Valdes L, Bravo J. Effect of age on outcome of secondary dengue 2 infections. Interna- tional journal of infectious diseases 2002; 6:118-124.
- Gamble J, Bethell D, Day NPJ, Loc PP, Phu NH, Gartside IB, et al. Age-related changes in micro- vascular permeability : a significant factor in the susceptibility of children to shock ? Clinical Science 2000; 98:211-216.
- Nhan NT, Phuong CXT, Kneen R, Wills B, Van My N, Phuong NTQ, et al. Acute Management of Dengue Shock Syndrome: A Randomized Double-Blind Com- parison of 4 Intravenous Fluid Regimens in the First Hour. Clinical Infectious Diseases 2001; 32:204-213.
- Aslam M, Aleem NA, Zahid MF, Rahman AJ. Unusual Presentation of Dengue Fever: A child with acute myocarditis. Sultan Qaboos Univ Med J 2016; 16:101–4.
- Gulati S, Maheshwari A. Atypical manifestations of dengue. Trop Med Int Heal 2007; 12:1087–95.
- Szalai G, Krishnamurthy R, Hajnóczky G. Apoptosis driven by IP3-linked mitochondrial calcium sig- nals. EMBO journal 1999; 18:6349–61.
- de Mel S, Mowjood R, Kapuruge L, de Mel C, Path D. Mobitz type I atrio-ventricular block in dengue myocarditis, requiring temporary pacing. IDCases 2015; 2:99–101.
- La-Orkhun V, Supachokchaiwattana P, Lertsap- charoen P, Khongphatthanayothin A. Spectrum of cardiac rhythm abnormalities and heart rate va- riability during the convalescent stage of dengue virus infection: a Holter study. Ann Trop Paediatr 2011; 31:123–8.
- Kindermann I, Barth C, Mahfoud F, Ukena C, Lenski M, Yilmaz A, et al. Update on myocarditis. J Am Coll Cardiol 2012; 59:779–92.
- Pothapregada S, Kamalakannan B, Thulasingam M. Clinical Profile of Atypical Manifestations of Dengue Fever. Indian J Pediatr 2016; 83:493-499.
- Tahir H, Daruwalla V, Hayat S. Myocarditis Leading to Severe Dilated Cardiomyopathy in a Patient with Dengue Fever. Case Reports Cardiol 2015; 2015:0-0.
